Clear Sky Science · it
Coefficienti delle funzioni di Miller–Ross e tecnica di miglioramento delle tomografie computerizzate basata su kernel
Tomografie cerebrali più nitide per risposte più chiare
Le tomografie computerizzate (TC) sono fondamentali per la diagnosi di patologie cerebrali, ma le immagini grezze possono essere rumorose, sfuocate o a basso contrasto — specialmente quando i medici cercano di ridurre la dose di radiazioni. Questo articolo esplora un approccio guidato matematicamente per rendere più nitide le immagini TC cerebrali prima che siano analizzate da radiologi o algoritmi. Invece di fare affidamento su grandi reti neurali, gli autori utilizzano un filtro immagine 3 × 3 progettato con cura, costruito a partire da una famiglia speciale di funzioni matematiche, con l’obiettivo di evidenziare meglio la struttura e la visibilità dei dettagli fini nelle scansioni mediche.
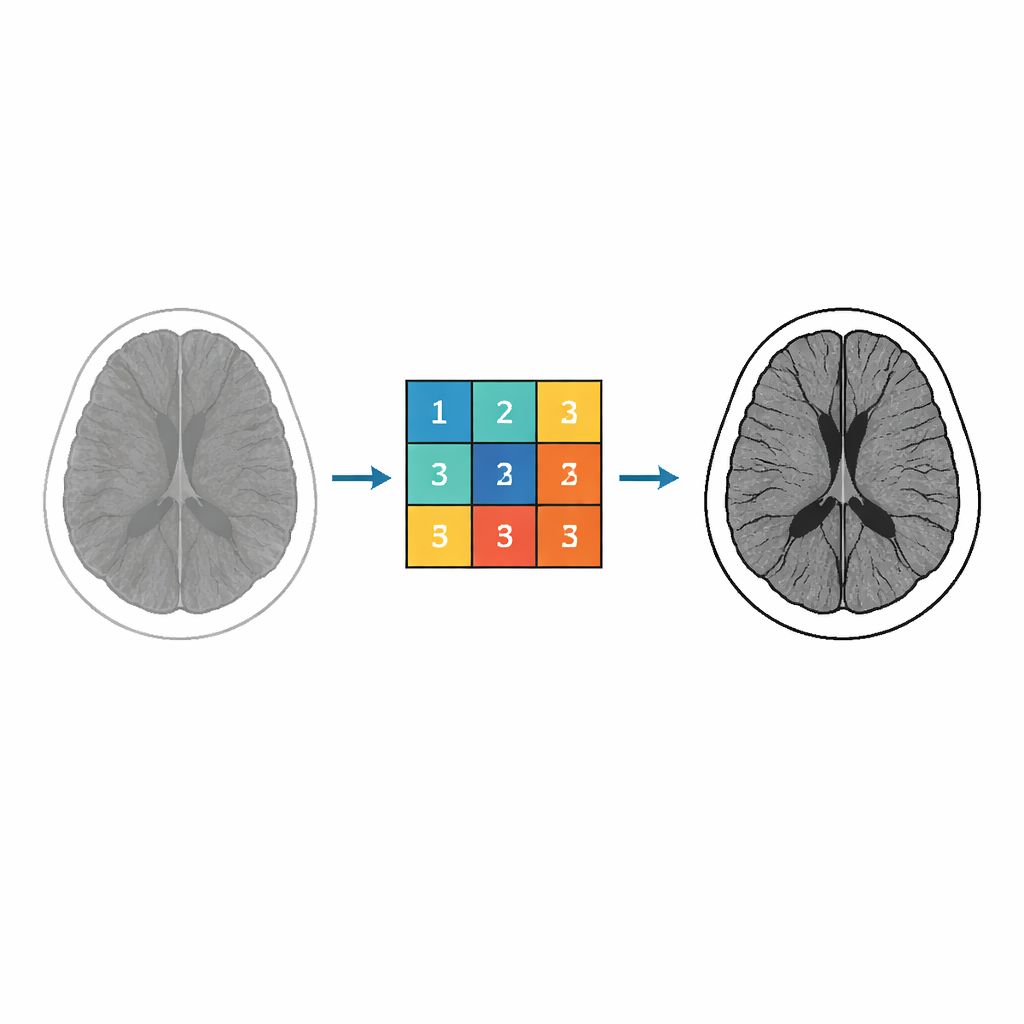
Dalla matematica astratta ai filtri per immagini
Al centro del lavoro c’è una classe di funzioni a valori complessi note come funzioni di Miller–Ross, sviluppate originariamente per risolvere equazioni differenziali frazionarie. I matematici studiano queste funzioni per le loro proprietà geometriche, come la capacità di mappare una regione del piano complesso su un’altra senza sovrapposizioni. Gli autori sfruttano queste proprietà per controllare come vengono trasformate le intensità dei pixel in un’immagine. Analizzando e limitando i coefficienti nell’espansione in serie di queste funzioni, ricavano valori numerici espliciti che possono essere usati come pesi in un filtro per immagini. Questi pesi sono poi assemblati in un kernel 3 × 3 — una piccola griglia che scorre sull’immagine combinando i valori dei pixel vicini per migliorare la struttura locale.
Costruire un kernel di miglioramento regolabile
L’idea chiave è trasformare diversi parametri astratti presenti nel quadro di Miller–Ross in manopole che determinano il comportamento del filtro. Parametri differenti influenzano quanto vengono enfatizzati i contorni, quanto viene soppresso il rumore e come vengono trattati i dettagli fini. Usando le disuguaglianze che dimostrano per i coefficienti delle funzioni, gli autori generano nove numeri che popolano il kernel 3 × 3. Si concentrano in particolare su un parametro frazionario che incide fortemente su come vengono messi in evidenza strutture sottili nel cervello — come i confini dei tessuti e piccole lesioni. Regolando questo parametro e gli altri, è possibile passare da un miglioramento più delicato a uno più aggressivo rimanendo entro limiti matematicamente controllati.

Mettere alla prova il metodo su dati TC reali
Per valutare l’approccio, i ricercatori applicano questi kernel basati su Miller–Ross a 155 immagini TC cerebrali infette tratte da un dataset pubblico. Progettano tre scenari sperimentali principali, ognuno dei quali fissa la maggior parte dei parametri variando una quantità chiave: nel primo regolano un parametro analogabile al contrasto; nel secondo e nel terzo variano un altro parametro frazionario in due impostazioni differenti. Per ogni immagine TC cercano il valore del parametro che dà il miglior miglioramento. La qualità delle immagini enhance è misurata usando due metriche standard: il rapporto segnale‑rumore di picco (PSNR), che valuta quanto l’immagine differisce da un riferimento, e l’indice di similarità strutturale (SSIM), che riflette quanto bene vengono preservati pattern e strutture importanti. Nei casi migliori il metodo produce valori di PSNR e SSIM notevolmente alti, con alcune immagini che raggiungono SSIM prossimi a 0,99, indicando una fedeltà strutturale molto elevata.
Confronto con metodi AI moderni
Gli autori confrontano quindi i loro risultati con una serie di tecniche consolidate di miglioramento e denoising per TC, comprese popolari architetture di deep learning come reti neurali convoluzionali, reti antagoniste generative e reti residuali, oltre ad approcci classici come il non‑local means e il filtraggio BM3D. In media, questi modelli deep ottengono ancora punteggi PSNR e SSIM più alti e più stabili, a conferma della loro efficacia quando sono addestrati su grandi dataset. Tuttavia, il nuovo approccio basato su Miller–Ross mostra un’ampia variabilità di prestazioni: mentre alcune immagini risultano meno convincenti, altre superano i migliori punteggi riportati dai filtri tradizionali e si avvicinano a quelli di sistemi più complessi. Questa variabilità sottolinea la sensibilità del metodo alle scelte dei parametri, ma anche il suo potenziale quando tali scelte sono ben ottimizzate.
Promesse e limiti pratici
Lo studio conclude che la tecnica di miglioramento basata su kernel proposta non supera ancora in modo sistematico i metodi di deep learning di fascia alta, ma offre vantaggi importanti. Poiché il filtro è costruito direttamente da formule matematiche trasparenti, clinici e ingegneri possono comprendere e controllare come ogni parametro influisce sul risultato — cosa che spesso è difficile con reti neurali “scatola nera”. Il metodo è particolarmente efficace nell’evidenziare dettagli strutturali fini che possono aiutare la diagnosi, anche quando i punteggi di qualità globali non aumentano sempre. Gli autori segnalano limitazioni, tra cui la dipendenza da un dataset ridotto, l’affidamento solo su metriche numeriche e la necessità di una taratura accurata dei parametri, e auspicano lavori futuri che includano feedback clinico e studi su larga scala. Ciononostante, l’approccio illustra come idee di matematica pura possano essere tradotte in strumenti pratici per rendere immagini salvavita più chiare e informative.
Citazione: Murugusundaramoorthy, G., Nalliah, M. Miller–Ross-functions coefficients and kernel-based CT-scan enhancement technique. Sci Rep 16, 13527 (2026). https://doi.org/10.1038/s41598-026-41609-w
Parole chiave: miglioramento immagine TC, imaging cerebrale, filtraggio delle immagini, calcolo frazionario, elaborazione di immagini medicali