Clear Sky Science · de
Miller–Ross-Funktionskoeffizienten und kernelbasierte CT-Scan-Verbesserungstechnik
Scharfere Gehirnscans für klarere Antworten
Computertomographie (CT)-Scans sind zentral für die Diagnose von Hirnerkrankungen, doch die Rohaufnahmen können verrauscht, unscharf oder kontrastarm sein – besonders wenn Ärzte die Strahlendosis verringern wollen. Diese Arbeit untersucht einen mathematisch fundierten Ansatz, um Gehirn-CT-Bilder vor der Analyse durch Radiologen oder Computeralgorithmen zu schärfen. Anstatt auf große neuronale Netze zu setzen, verwenden die Autorinnen und Autoren einen sorgfältig entworfenen 3 × 3-Bildfilter, der aus einer speziellen Familie mathematischer Funktionen aufgebaut ist, mit dem Ziel, die Struktur zu klären und feine Details in medizinischen Aufnahmen besser sichtbar zu machen.
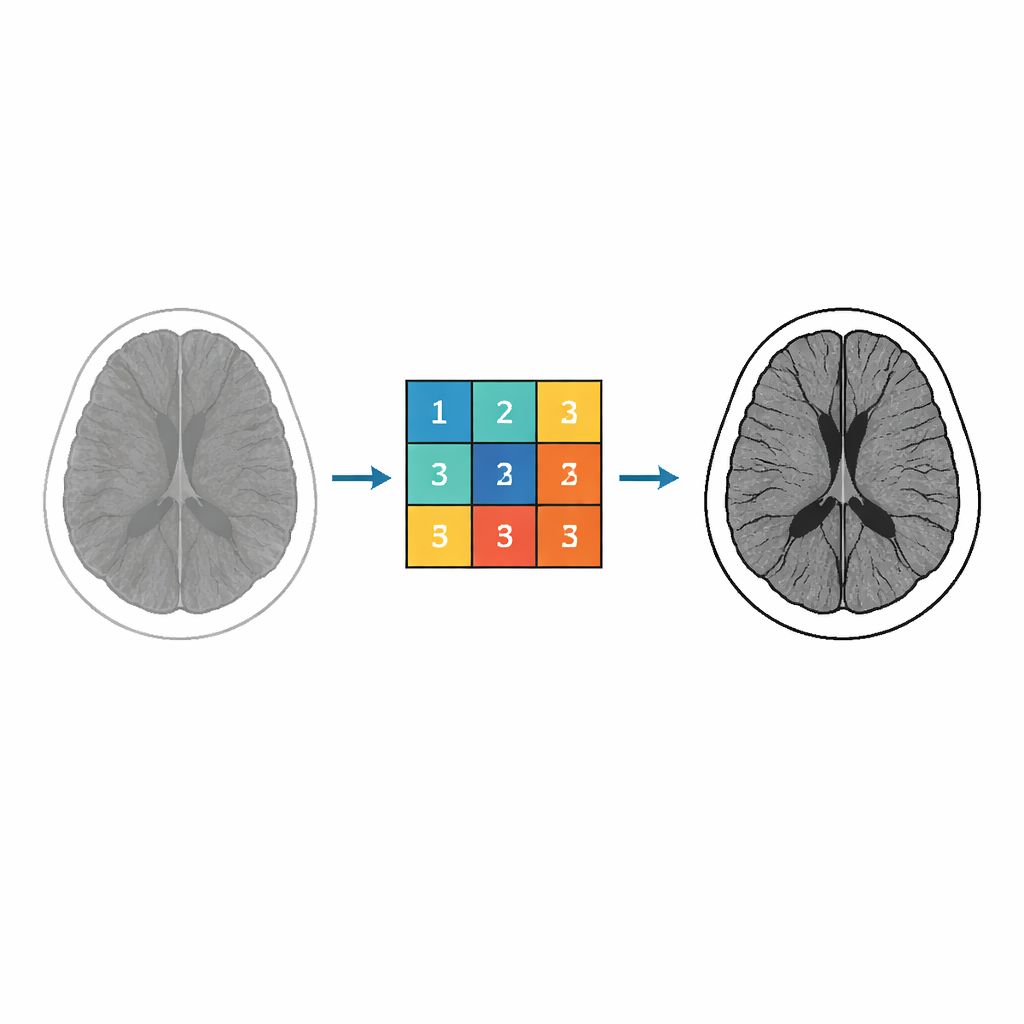
Von abstrakter Mathematik zu Bildfiltern
Im Zentrum der Arbeit steht eine Klasse komplexwertiger Funktionen, bekannt als Miller–Ross-Funktionen, ursprünglich entwickelt zur Lösung fraktionaler Differentialgleichungen. Mathematiker untersuchen diese Funktionen wegen ihrer geometrischen Eigenschaften, etwa wie sie Bereiche der komplexen Ebene ohne Überlappungen aufeinander abbilden. Die Autorinnen und Autoren nutzen diese Eigenschaften, um zu steuern, wie Pixelintensitäten in einem Bild transformiert werden. Durch die Analyse und Abschätzung der Koeffizienten in der Reihenentwicklung dieser Funktionen leiten sie explizite numerische Werte ab, die als Gewichte in einem Bildfilter verwendet werden können. Diese Gewichte werden dann zu einem 3 × 3-Kernel zusammengesetzt – ein kleines Gitter, das über das Bild gleitet und benachbarte Pixelwerte kombiniert, um lokale Strukturen zu verstärken.
Entwurf eines einstellbaren Verstärkungskernels
Die zentrale Idee besteht darin, mehrere abstrakte Parameter aus dem Miller–Ross-Rahmen in Regelgrößen zu verwandeln, die das Verhalten des Filters bestimmen. Verschiedene Parameter beeinflussen, wie stark Kanten betont, wieviel Rauschen unterdrückt und wie feine Details behandelt werden. Mit Hilfe von Ungleichungen, die sie für die Funktionskoeffizienten beweisen, erzeugen die Autorinnen und Autoren neun Zahlen, die das 3 × 3-Kernel füllen. Besonders im Fokus steht ein fraktionaler Parameter, der stark beeinflusst, wie subtile Strukturen im Gehirn – etwa Gewebegrenzen und kleine Läsionen – hervorgehoben werden. Durch Anpassung dieses und anderer Parameter können sie zwischen sanfterer und aggressiverer Verstärkung wechseln, während sie innerhalb mathematisch kontrollierter Grenzen bleiben.

Erprobung der Methode an realen CT-Daten
Zur Bewertung ihres Ansatzes wenden die Forschenden diese Miller–Ross-basierten Kerne auf 155 infizierte Gehirn-CT-Aufnahmen aus einem öffentlichen Datensatz an. Sie entwerfen drei Hauptversuchsszenarien, in denen jeweils die meisten Parameter fixiert sind und eine wichtige Größe variiert wird: Im ersten stimmen sie einen kontrastähnlichen Parameter ab; im zweiten und dritten variieren sie einen weiteren fraktionalen Parameter unter zwei unterschiedlichen Einstellungen. Für jedes CT-Bild suchen sie den Parameterwert, der die beste Verbesserung erzielt. Die Qualität der verbesserten Bilder wird mit zwei standardisierten Metriken gemessen: Peak Signal-to-Noise Ratio (PSNR), das misst, wie stark sich das Bild von einer Referenz unterscheidet, und Structural Similarity Index (SSIM), das widerspiegelt, wie gut wichtige Muster und Strukturen erhalten bleiben. In den besten Fällen liefert die Methode bemerkenswert hohe PSNR- und SSIM-Werte, wobei einige Bilder SSIM-Werte nahe 0,99 erreichen, was auf eine sehr starke strukturelle Treue hindeutet.
Vergleich mit modernen KI-Verfahren
Die Autorinnen und Autoren stellen ihre Ergebnisse dann neben eine Reihe etablierter CT-Verbesserungs- und Rauschunterdrückungstechniken, darunter verbreitete Deep-Learning-Modelle wie Convolutional Neural Networks, Generative Adversarial Networks und Residual Networks sowie klassische Ansätze wie Non-Local Means und BM3D-Filterung. Im Durchschnitt erzielen diese Deep-Modelle weiterhin höhere und stabilere PSNR- und SSIM-Werte, was ihre Stärke bei Training auf großen Datensätzen widerspiegelt. Der neue Miller–Ross-basierte Ansatz zeigt jedoch eine große Leistungsspanne: Während einige Bilder weniger beeindruckend sind, übertreffen andere die besten berichteten Werte traditioneller Filter und kommen mit komplexeren Systemen in Konkurrenz. Diese Variabilität unterstreicht die Sensitivität der Methode gegenüber Parameterwahl, aber auch ihr Potenzial, wenn diese Wahl gut getroffen wird.
Versprechen und praktische Grenzen
Die Studie schlussfolgert, dass die vorgeschlagene kernelbasierte Verstärkungstechnik noch nicht durchgängig die erstklassigen Deep-Learning-Methoden übertrifft, sie jedoch wichtige Vorteile bietet. Da der Filter direkt aus transparenten mathematischen Formeln aufgebaut ist, können Kliniker und Ingenieure nachvollziehen und steuern, wie jeder Parameter das Ergebnis beeinflusst – etwas, das bei Black-Box-Neuronalen-Netzen oft schwierig ist. Die Methode eignet sich besonders gut dazu, feine Strukturdetails hervorzuheben, die bei der Diagnose helfen können, selbst wenn sich globale Qualitätskennzahlen nicht immer erhöhen. Die Autorinnen und Autoren weisen auf Einschränkungen hin, darunter die Abhängigkeit von einem kleinen Datensatz, die ausschließliche Orientierung an numerischen Metriken und der Bedarf an sorgfältiger Parametereinstellung, und sie fordern weitere Arbeiten mit klinischem Feedback und größeren Studien. Dennoch zeigt der Ansatz, wie Ideen aus der reinen Mathematik in praktische Werkzeuge übersetzt werden können, um lebenswichtige Bilder klarer und informativer zu machen.
Zitation: Murugusundaramoorthy, G., Nalliah, M. Miller–Ross-functions coefficients and kernel-based CT-scan enhancement technique. Sci Rep 16, 13527 (2026). https://doi.org/10.1038/s41598-026-41609-w
Schlüsselwörter: CT-Bildverbesserung, Gehirnbildgebung, Bildfilterung, fraktionale Analysis, medizinische Bildverarbeitung