Clear Sky Science · nl
Data-gedreven verklaarbare detectie van chronische nierziekte met RF-gebaseerde data-imputatie en meta-ensemble leren
Waarom dit belangrijk is voor alledaagse gezondheid
Chronische nierziekte sluipt vaak stilletjes binnen en beschadigt het lichaam lang voordat symptomen zichtbaar zijn. Voor veel mensen, vooral in omgevingen met beperkte middelen, zijn eenvoudige bloed- en urinetests beschikbaar, maar artsen beschikken niet altijd over hulpmiddelen die optimaal gebruikmaken van die informatie. Deze studie laat zien hoe een zorgvuldig ontworpen kunstmatig intelligentiesysteem routine-labgegevens kan omzetten in een vroegwaarschuwingssignaal voor nierproblemen, terwijl het toch mogelijk blijft voor clinici om te begrijpen waarom de computer een patiënt markeert.
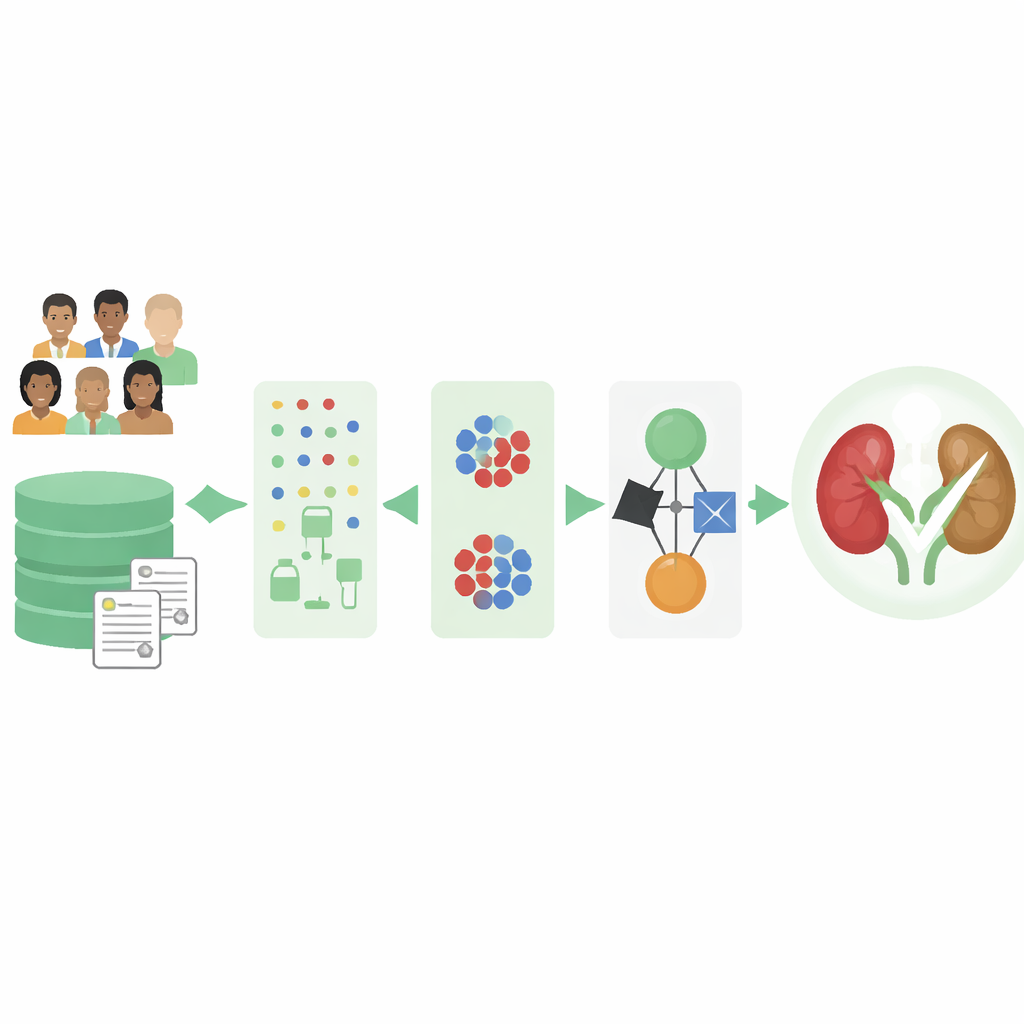
Rommelige klinische dossiers omzetten in bruikbare aanwijzingen
Medische dossiers uit de praktijk zijn zelden compleet. Labuitslagen kunnen ontbreken en sommige patiënttypen worden veel vaker vastgelegd dan andere. De auteurs werkten met een bekend openbaar dataset van 400 personen, ieder beschreven met 25 basismetingen zoals leeftijd, bloeddruk, bloedwaarden en niergerelateerde chemische markers. Veel invoer had lacunes en er waren meer mensen zonder nierziekte dan met, wat computer modellen kan vertekenen. Om dit te corrigeren bouwde het team eerst een slimme schoonmaakstap die patronen leert uit de bestaande gegevens om ontbrekende waarden in te vullen in plaats van onvolledige records weg te gooien of grove gemiddelden te gebruiken.
De balans herstellen tussen zieke en gezonde
Aangezien de dataset meer gevallen zonder nierziekte bevatte, zou een model dat naïef is getraind er verstandig aan kunnen doen vaak “gezond” te voorspellen en toch een misleidend hoge score te behalen. Om deze ongelijkheid tegen te gaan, gebruikten de onderzoekers een methode die realistische synthetische voorbeelden van de ondervertegenwoordigde groep creëert. In wezen bestudeert het patiënten met chronische nierziekte en genereert nieuwe, licht gevarieerde gevallen die op hen lijken. Na deze stap ziet de computer een meer gebalanceerd beeld van zieke en gezonde individuen, wat helpt om aandacht te besteden aan die vroege, gemakkelijk te missen waarschuwingssignalen.
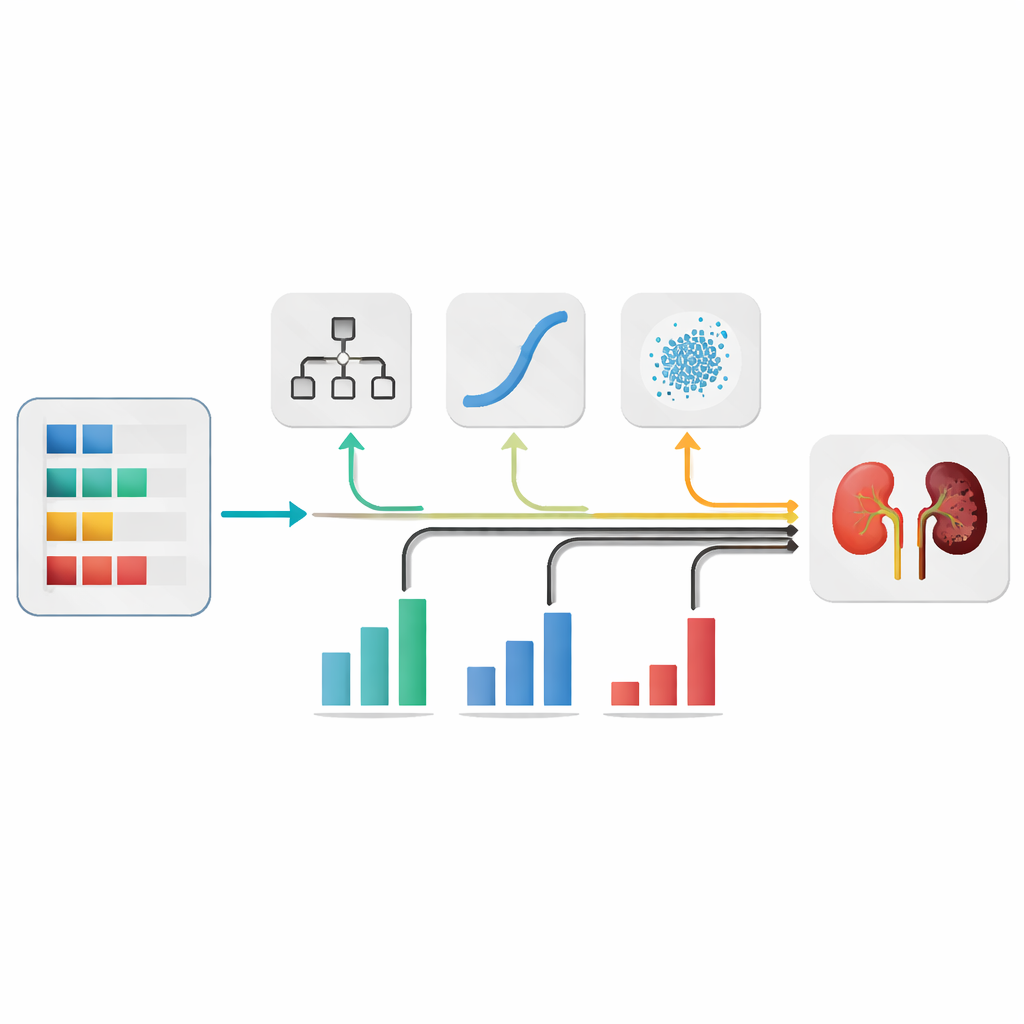
Veel eenvoudige geesten die samenwerken
In plaats van te wedden op één type algoritme, stelden de auteurs verschillende bekende machine-learningmodellen samen die elk dezelfde patiëntgegevens op verschillende manieren bekijken. Ze evalueerden vijf kanshebbers en kozen er drie die het beste presteerden: een beslissingsboom, een logistisch model en een eenvoudige probabilistische classifier. Deze modellen werden vervolgens gecombineerd in een “ensemble”, waarbij elk zijn eigen oordeel geeft over de vraag of een patiënt waarschijnlijk nierziekte heeft. De uiteindelijke beslissing is een gewogen mix van hun uitkomsten, vergelijkbaar met het raadplegen van meerdere artsen waarvan de meningen niet gelijk worden gewogen maar afhankelijk van hoe betrouwbaar ze zijn.
Een digitale roedel wolven het beste mengsel laten kiezen
Het kiezen hoeveel vertrouwen aan elk model in het ensemble wordt gegeven is cruciaal. In plaats van te gokken, gebruikten de auteurs een optimalisatietechniek geïnspireerd op het jachtgedrag van grijze wolven. Dit algoritme verkent vele combinaties van gewichten en beweegt geleidelijk naar de mix die de hoogste nauwkeurigheid oplevert op gehouden aparte data. Met deze afgestelde combinatie classificeerde het systeem bijna 99 van de 100 gevallen correct in cross-validatie en behield het een zeer laag percentage gemiste nierziektepatiënten, een bijzonder belangrijk doel bij screening.
De zwarte doos openen voor clinici
Een grote zorg bij AI in de geneeskunde is dat beslissingen ondoorzichtig kunnen lijken. Om dit aan te pakken pasten de onderzoekers verklaarbaarheidstools toe die laten zien welke labkenmerken een voorspelling per patiënt naar nierziekte toe of ervan af duwen. Ze vonden dat metingen zoals albumine in urine, rode bloedcellen, bloeddruk, diabetesstatus en niergerelateerde bloedmarkers sterk van invloed waren op de oordelen van het model. Deze patronen komen overeen met medische kennis, wat suggereert dat het systeem klinisch zinvolle regels leert in plaats van obscure statistische toevalligheden.
Wat dit voor patiënten zou kunnen betekenen
Kort gezegd toont dit werk aan dat een zorgvuldig voorbereide en verklaarde AI-assistent routine-labgegevens kan omzetten in een zeer betrouwbare vroege detector van chronische nierziekte. Door ontbrekende informatie schoon te maken, ongelijkheden in de data te corrigeren, meerdere eenvoudige modellen te combineren en vervolgens te verhelderen hoe beslissingen worden genomen, bereikt het raamwerk hoge nauwkeurigheid zonder een mysterieuze zwarte doos te worden. Hoewel het nog op grotere en meer diverse patiëntengroepen getest moet worden voordat het aan het bed gebruikt kan worden, wijst het op een toekomst waarin goedkope tests, gecombineerd met transparante AI, artsen helpen nierproblemen eerder te herkennen en zorg met meer vertrouwen aan te passen.
Bronvermelding: Gupta, R., Gambhir, S., Krejcar, O. et al. Data-driven explainable chronic kidney disease detection using RF based data imputation and meta-ensemble learning. Sci Rep 16, 12679 (2026). https://doi.org/10.1038/s41598-026-41425-2
Trefwoorden: chronische nierziekte, medische AI, ensemble learning, voorbewerking van gezondheidsgegevens, verklaarbare AI