Clear Sky Science · de
Datengetriebene erklärbare Erkennung chronischer Nierenerkrankungen mittels RF-basierter Datenimputation und Meta-Ensemble-Learning
Warum das für die alltägliche Gesundheit wichtig ist
Chronische Nierenerkrankungen schleichen sich oft still und leise an und schädigen den Körper lange bevor Symptome auftreten. Für viele Menschen, insbesondere in ressourcenarmen Umgebungen, sind einfache Blut- und Urintests verfügbar, doch Ärztinnen und Ärzte verfügen nicht immer über Werkzeuge, die diese Informationen optimal nutzen. Diese Studie zeigt, wie ein sorgfältig gestaltetes System der künstlichen Intelligenz (KI) Routinelabordaten in ein Frühwarnsignal für Nierenprobleme verwandeln kann, und zwar so, dass Klinikerinnen und Kliniker weiterhin verstehen können, warum der Rechner einen Patienten markiert.
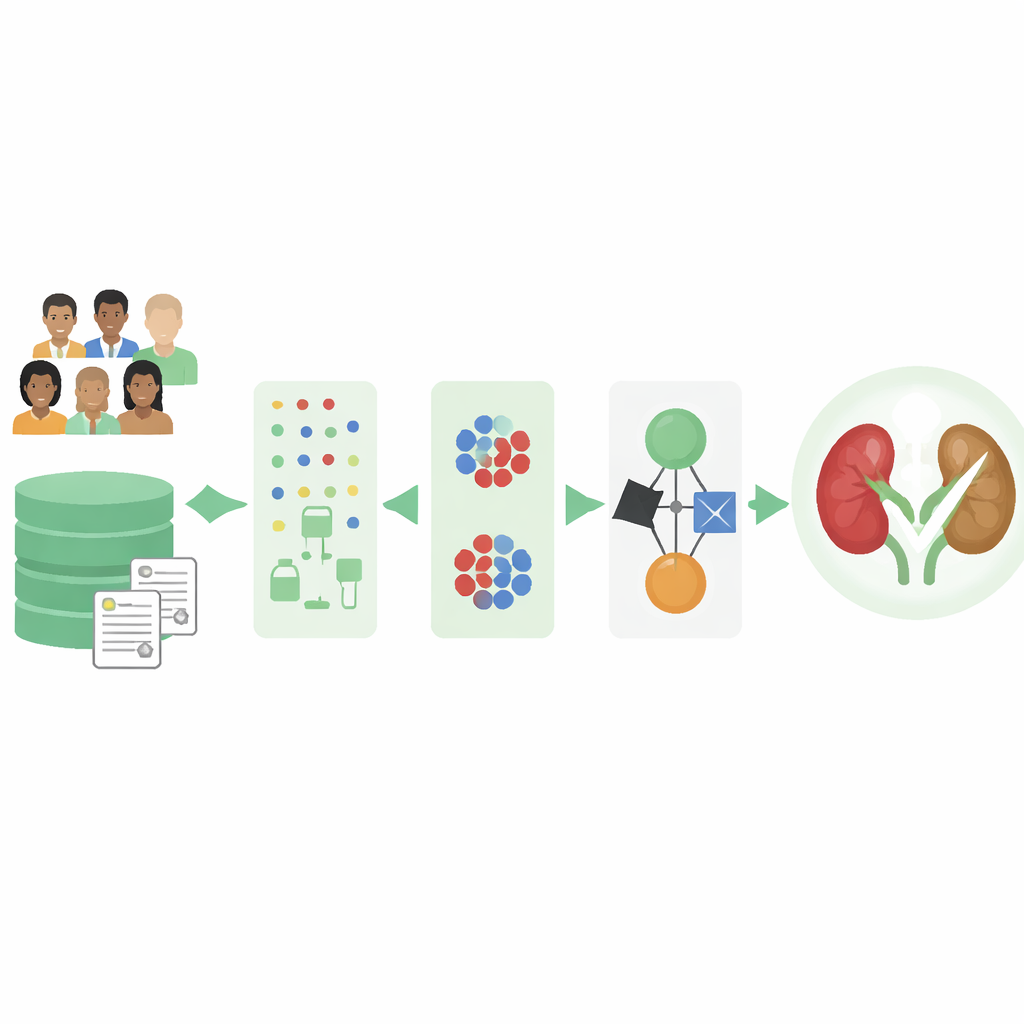
Unordentliche Klinikakten in verwertbare Hinweise verwandeln
Medizinische Realweltakten sind selten vollständig. Laborergebnisse können fehlen, und bestimmte Patientengruppen werden möglicherweise deutlich häufiger erfasst als andere. Die Autorinnen und Autoren arbeiteten mit einem bekannten öffentlichen Datensatz von 400 Personen, die jeweils durch 25 Basiswerte wie Alter, Blutdruck, Blutbilder und nierenspezifische Stoffe beschrieben sind. Viele Einträge wiesen Lücken auf, und es gab mehr Menschen ohne Nierenerkrankung als mit, was Computermodelle verzerren kann. Um das zu beheben, baute das Team zunächst einen intelligenten Reinigungsschritt, der Muster aus den vorhandenen Daten lernt, um fehlende Werte zu füllen, anstatt unvollständige Datensätze einfach zu verwerfen oder grobe Mittelwerte zu verwenden.
Die Balance zwischen krank und gesund herstellen
Da der Datensatz mehr Fälle ohne Nierenerkrankung enthielt, könnte ein naiv trainiertes Modell dazu neigen, auf "gesund" zu setzen und dennoch eine scheinbar hohe Bewertung zu erzielen. Um dieses Ungleichgewicht auszugleichen, verwendeten die Forschenden eine Methode, die realistische synthetische Beispiele der unterrepräsentierten Gruppe erzeugt. Im Kern analysiert sie Patienten mit chronischer Nierenerkrankung und generiert neue, leicht variierte Fälle, die diesen ähneln. Nach diesem Schritt sieht der Rechner ein ausgewogeneres Bild von kranken und gesunden Personen, was ihm hilft, auf frühe, leicht zu übersehende Warnzeichen zu achten.
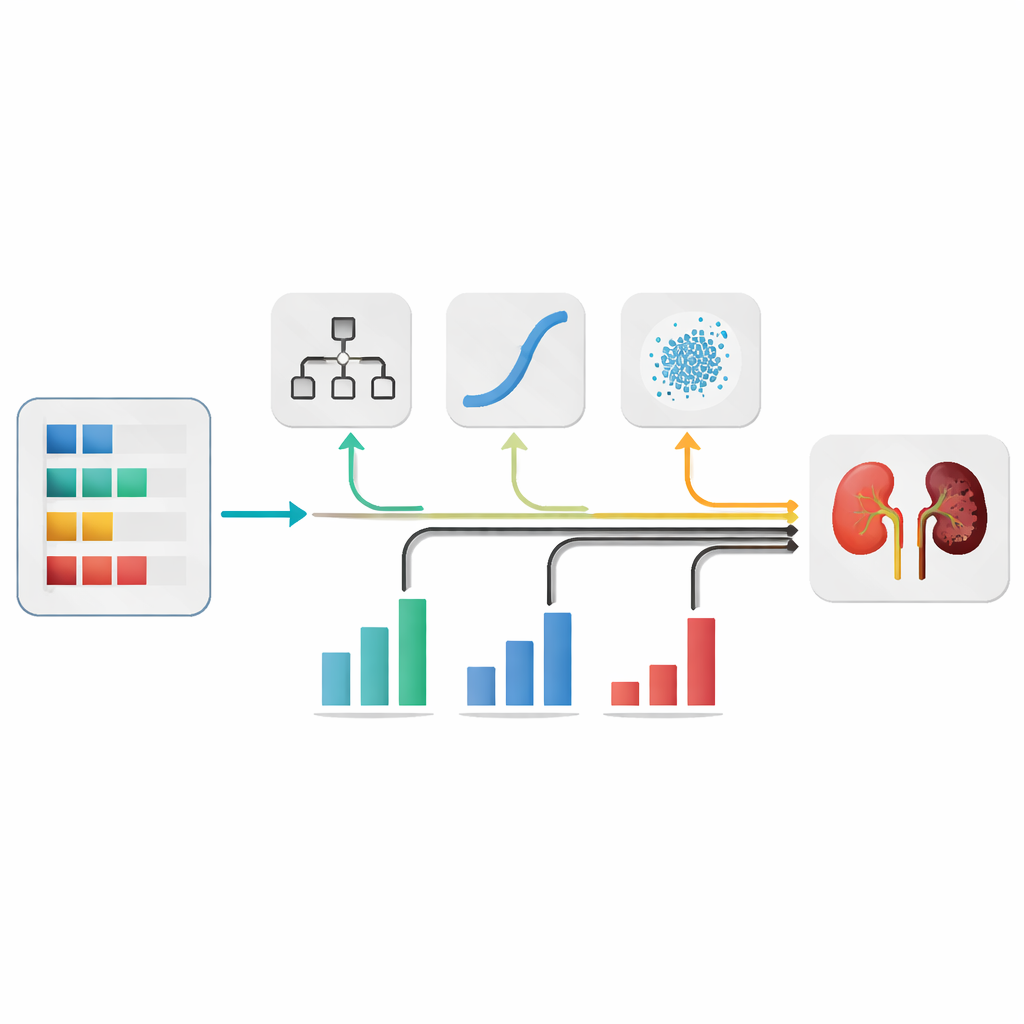
Viele einfache Modelle, die zusammenarbeiten
Anstatt auf einen einzelnen Algorithmus zu setzen, stellten die Autorinnen und Autoren mehrere bekannte Machine‑Learning‑Modelle zusammen, die dieselben Patientendaten auf unterschiedliche Weise betrachten. Sie bewerteten fünf Kandidaten und wählten drei aus, die die beste Leistung zeigten: einen Entscheidungsbaum, ein logistisches Modell und einen einfachen probabilistischen Klassifikator. Diese Modelle wurden dann zu einem „Ensemble“ kombiniert, bei dem jedes seine eigene Einschätzung dazu abgibt, ob ein Patient wahrscheinlich eine Nierenerkrankung hat. Die endgültige Entscheidung ist eine gewichtete Mischung ihrer Ausgaben, vergleichbar mit der Konsultation mehrerer Ärztinnen und Ärzte, deren Meinungen nicht gleich gewichtet, sondern nach ihrer Zuverlässigkeit berücksichtigt werden.
Eine digitale Wolfsrudel‑Optimierung wählt die beste Mischung
Die Frage, wie viel Vertrauen jedem Modell im Ensemble geschenkt wird, ist entscheidend. Statt zu raten, verwendeten die Autorinnen und Autoren eine Optimierungstechnik, die vom Jagdverhalten der Grauen Wölfe inspiriert ist. Dieser Algorithmus durchsucht viele Kombinationen von Gewichten und bewegt sich schrittweise auf die Mischung zu, die die höchste Genauigkeit auf zurückgehaltenen Daten liefert. Mit dieser feinabgestimmten Kombination klassifizierte das System in der Kreuzvalidierung fast 99 von 100 Fällen korrekt und hielt eine sehr niedrige Rate an übersehenen Nierenerkrankungsfällen, was für das Screening besonders wichtig ist.
Die Black Box für Kliniker öffnen
Ein zentrales Problem bei KI in der Medizin ist, dass ihre Entscheidungen undurchsichtig erscheinen können. Um dem zu begegnen, setzten die Forschenden Erklärbarkeitswerkzeuge ein, die zeigen, welche Labormerkmale eine Vorhersage für einen einzelnen Patienten in Richtung oder weg von einer Nierenerkrankung treiben. Sie stellten fest, dass Messgrößen wie Albumin im Urin, rote Blutkörperchen, Blutdruck, Diabetesstatus und nierenspezifische Blutmarker die Urteile des Modells stark beeinflussten. Diese Muster stimmen mit medizinischem Wissen überein und deuten darauf hin, dass das System klinisch sinnvolle Regeln lernt und nicht nur obskure statistische Zufälligkeiten.
Was das für Patientinnen und Patienten bedeuten könnte
Einfach gesagt zeigt diese Arbeit, dass ein sorgfältig vorbereitetes und erklärtes KI‑Assistenzsystem Routinelabordaten in einen hochzuverlässigen Frühdetektor für chronische Nierenerkrankungen verwandeln kann. Durch das Bereinigen fehlender Informationen, das Korrigieren von Datenungleichgewichten, das Zusammenführen mehrerer einfacher Modelle und das Offenlegen der Entscheidungsgrundlagen erzielt das Framework hohe Genauigkeit, ohne zu einer geheimnisvollen Black Box zu werden. Obwohl es noch an größeren und vielfältigeren Patientengruppen geprüft werden muss, bevor es am Krankenbett eingesetzt wird, weist es in Richtung einer Zukunft, in der kostengünstige Tests kombiniert mit transparenter KI Ärztinnen und Ärzten helfen, Nierenprobleme früher zu erkennen und die Versorgung sicherer zu individualisieren.
Zitation: Gupta, R., Gambhir, S., Krejcar, O. et al. Data-driven explainable chronic kidney disease detection using RF based data imputation and meta-ensemble learning. Sci Rep 16, 12679 (2026). https://doi.org/10.1038/s41598-026-41425-2
Schlüsselwörter: chronische Nierenerkrankung, medizinische KI, Ensemble-Learning, Vorverarbeitung von Gesundheitsdaten, erklärbare KI