Clear Sky Science · nl
Deep learning voor vaatssegmentatie en stroomanalyse om clusters te identificeren die samenhangen met nadelige uitkomsten in een Fontan-patiëntenregister
Waarom het bestuderen van hartstroom bij kinderen belangrijk is
Kinderen die met slechts één werkende harthelft geboren worden, ondergaan vaak een complexe ingreep genaamd de Fontan-procedure om te kunnen overleven tot in de volwassenheid. Deze patiënten kunnen jarenlang stabiel lijken, maar sommige ontwikkelen later ernstige problemen die hart en lever aantasten. Artsen verzamelen al gedetailleerde MRI-scans die vastleggen hoe bloed zich daadwerkelijk door hart en vaten beweegt in de tijd, maar het merendeel van deze rijke bewegingsdata wordt vrijwel nooit benut. Deze studie laat zien hoe moderne kunstmatige intelligentie die verborgen informatie op schaal kan ontsluiten en zo stromingspatronen onthult die samenhangen met betere of slechtere lange termijngezondheid.
Duizenden scans omzetten in bruikbare gegevens
De onderzoekers werkten met het FORCE-register, een grote internationale verzameling van cardiale MRI-onderzoeken van meer dan 3.000 mensen met Fontan-circulatie. Elk onderzoek bevat gespecialiseerde films die bijhouden hoe snel bloed door belangrijke bloedvaten stroomt bij elke hartslag. Om van deze scans te leren, moest het team eerst de vaten op elk afbeeldingsframe afbakenen en de stroom in de tijd meten — een tijdrovende handmatige taak die naar schatting een jaar onafgebroken expertswerk zou vergen. In plaats daarvan bouwden ze een deep learning-model dat zowel kan herkennen welk vat in beeld is als automatisch de vatgrens kan tekenen voor vijf belangrijke trajecten: de aorta en vier grote aders en slagaders die naar en van de longen lopen.
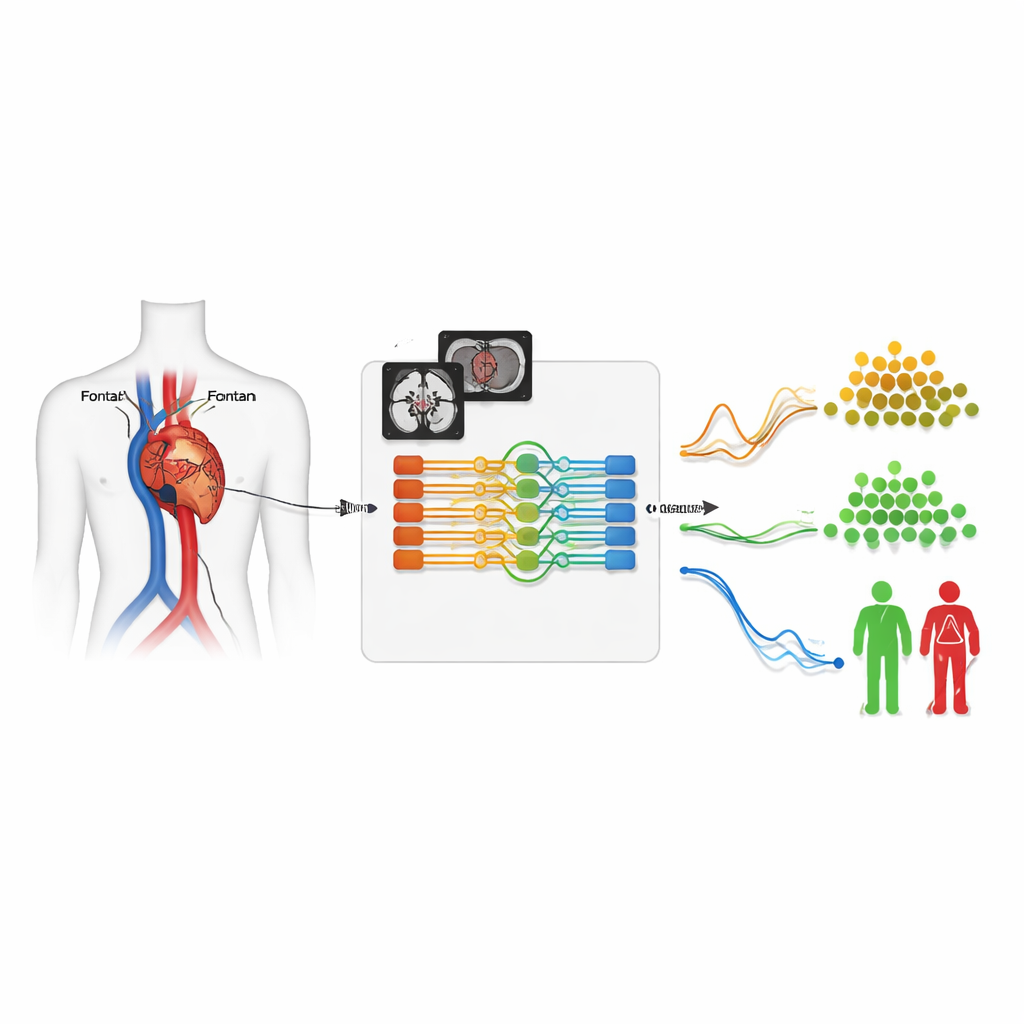
Hoe het slimme segmentatiesysteem werkt
De kern van het systeem is een neuraal netwerk dat elke film analyseert als een kort 3D-blok: twee ruimtelijke dimensies plus tijd. Het verwerkt twee versies van het MRI-signaal — de ene die de anatomie toont, de andere die bewegend bloed benadrukt — en is getraind op 260 onderzoeken waarin experts de vaten al met de hand hadden getraceerd. Het model beperkt zich niet tot het omlijnen van structuren; het leert ook welk vat welk is, geholpen door informatie die de scanneroperator tijdens het maken van de beelden intypte. Met dit gecombineerde classificatie-en-segmentatieontwerp behaalde het systeem een zeer hoge overlap met menselijke traceringen en herkende het juist het vattype in bijna alle testgevallen, ondanks de uitzonderlijk gedraaide en variabele anatomie die vaak voorkomt bij Fontan-patiënten.
Opschalen naar een compleet internationaal register
Nadat het was gevalideerd, werd het model in een geautomatiseerde cloudpijplijn geplaatst en losgelaten op meer dan 4.500 registeronderzoeken. Voor elke scan selecteerde het de stroomfilmpjes, segmenteerde de vijf doelvaten en genereerde voor elke hartslag een stroom‑tegen‑tijd‑curve, geheel zonder menselijke tussenkomst. Experts controleerden later deze resultaten en vonden dat ongeveer 90% van de segmentaties goed genoeg was voor klinisch gebruik wanneer alle vijf vaten aanwezig waren. Het systeem presteerde iets minder goed bij patiënten met bijzonder ongebruikelijke anatomieën, zoals gedupliceerde aders, maar leverde toch een enorme, voorheen onbereikbare dataset van schone, tijdsvariërende bloedstroommetingen.

Verborgen stroomtypes vinden die samenhangen met uitkomsten
Met duizenden stroomcurves in handen zocht het tweede deep learning-model van het team naar natuurlijke groeperingen van patiënten, uitsluitend gebaseerd op hoe bloed zich in de tijd door hun vaten bewoog. Dit model comprimeerde elk paar curves — ofwel van de longslagaders ofwel van de grote aders — tot een compacte interne representatie en groepeerde patiënten vervolgens in verschillende stroom-«fenotypen». Sommige groepen hadden gebalanceerde, normaalgrote stromen; andere toonden verminderde totale flow, dominante flow naar één long, of flow die verschoven was naar de ontspanningsfase van de hartcyclus. De onderzoekers volgden daarna de patiënten in de tijd en ontdekten dat bepaalde stroompatronen samenhingen met hogere risico’s op overlijden, harttransplantatie of leverziekte, zelfs nadat werd gecorrigeerd voor leeftijd, hartpompfunctie en andere gangbare maatstaven.
Wat dit kan betekenen voor toekomstige zorg
In eenvoudige woorden toont de studie aan dat hoe bloed door de Fontan-circulatie beweegt — welke vaten meer of minder flow dragen en op welk moment in de hartcyclus — essentiële aanwijzingen bevat over welke patiënten waarschijnlijk ernstige complicaties zullen krijgen. De auteurs laten zien dat kunstmatige intelligentie grote archieven van rauwe MRI-films kan omzetten in betekenisvolle stroomprofielen en risicogroepen, zonder handmatig traceren of handgemaakte regels. In de toekomst zou een systeem als dit automatisch kunnen draaien direct na de MRI van een kind, en diegenen signaleren wiens stroompatronen lijken op hogere-risicogroepen, zodat artsen vervolgafspraken, onderzoeken of zelfs chirurgische planning kunnen afstemmen. Buiten Fontan-patiënten kan dezelfde benadering worden aangepast aan andere hartaandoeningen, bewegingsvolgscans of zelfs alledaagse signalen zoals ECG’s, waardoor beter gebruik wordt gemaakt van informatie die ziekenhuizen al verzamelen maar zelden grondig analyseren.
Bronvermelding: Yao, T., Clair, N.S., Gong, M. et al. Deep learning for vessel segmentation and flow analysis to identify clusters associated with adverse outcomes in a fontan patient registry. Sci Rep 16, 11956 (2026). https://doi.org/10.1038/s41598-026-40738-6
Trefwoorden: Fontan-circulatie, cardiale MRI, deep learning, bloedstroompatronen, patiëntrisicostratificatie