Clear Sky Science · de
Tiefes Lernen für Gefäßsegmentierung und Flussanalyse zur Identifizierung von Clustern, die mit ungünstigen Outcomes in einem Fontan-Patientenregister assoziiert sind
Warum es wichtig ist, den Herzfluss bei Kindern zu untersuchen
Kinder, die nur mit einer funktionierenden Herzkammer geboren werden, durchlaufen häufig einen komplexen Eingriff namens Fontan-Operation, damit sie bis ins Erwachsenenalter überleben können. Diese Patienten können jahrelang stabil erscheinen, entwickeln später jedoch bei manchen ernsthafte Probleme von Herz und Leber. Ärztinnen und Ärzte erfassen bereits detaillierte MRT-Aufnahmen, die zeigen, wie sich das Blut im Zeitverlauf durch Herz und Gefäße bewegt, doch ein Großteil dieser reichen Bewegungsdaten bleibt ungenutzt. Diese Studie zeigt, wie moderne künstliche Intelligenz diese verborgenen Informationen in großem Maßstab erschließen kann und welche Blutflussmuster mit besserer oder schlechterer Langzeitgesundheit verbunden sind.
Aus Tausenden von Scans verwertbare Daten machen
Die Forschenden arbeiteten mit dem FORCE-Register, einer großen internationalen Sammlung von kardialen MRT-Untersuchungen von mehr als 3.000 Menschen mit Fontan-Zirkulation. Jede Untersuchung enthält spezielle Filme, die verfolgen, wie schnell das Blut mit jedem Herzschlag durch wichtige Gefäße fließt. Um aus diesen Aufnahmen zu lernen, musste das Team zunächst in jedem Bildframe die Gefäße umreißen und den Fluss über die Zeit messen – eine mühsame manuelle Aufgabe, die schätzungsweise ein Jahr ununterbrochener Expertenarbeit erfordert hätte. Stattdessen entwickelten sie ein Deep-Learning-Modell, das sowohl erkennen kann, welches Gefäß abgebildet ist, als auch automatisch die Gefäßgrenze für fünf wichtige Bahnen zeichnet: die Aorta und vier große Venen und Arterien, die zu und von den Lungen führen.
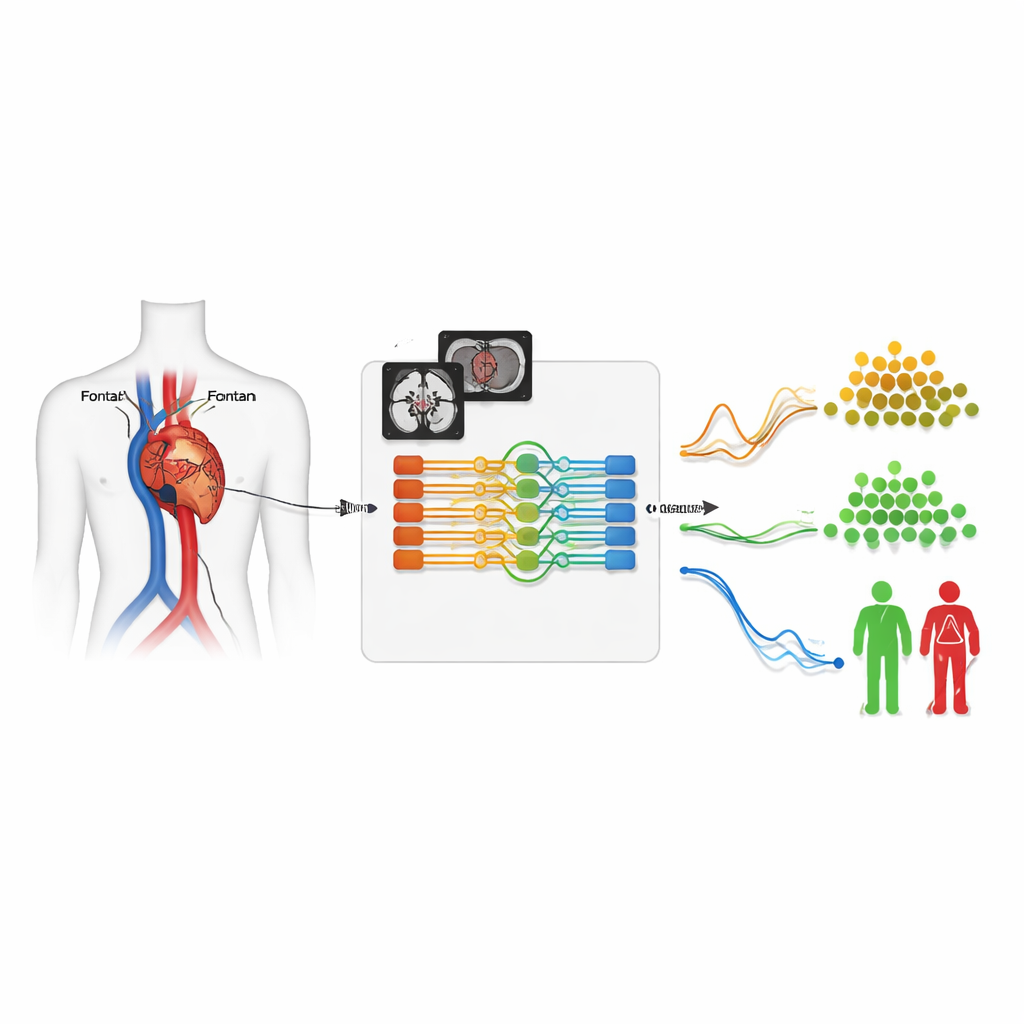
Wie das intelligente Segmentierungssystem funktioniert
Kern des Systems ist ein neuronales Netz, das jeden Film als kurzen 3D-Block analysiert: zwei räumliche Dimensionen plus Zeit. Es verarbeitet zwei Versionen des MRT-Signals – eine, die die Anatomie zeigt, und eine, die das bewegte Blut hervorhebt – und wurde an 260 Untersuchungen trainiert, in denen Expertinnen und Experten die Gefäße bereits von Hand nachgezeichnet hatten. Das Modell umreißt nicht nur Strukturen; es lernt auch, welches Gefäß welches ist, unterstützt durch Informationen, die der Bediener des Scanners bei der Aufnahme eingegeben hatte. Durch dieses kombinierte Klassifikations‑und‑Segmentierungs‑Design erreichte das System eine sehr hohe Übereinstimmung mit menschlichen Nachzeichnungen und identifizierte den Gefäßtyp in nahezu allen Testfällen korrekt, trotz der ungewöhnlich verdrehten und variablen Anatomie, die bei Fontan-Patienten häufig vorkommt.
Hochskalierung auf ein gesamtes internationales Register
Nach der Validierung wurde das Modell in eine automatisierte Cloud-Pipeline eingebettet und auf mehr als 4.500 Registeruntersuchungen angewendet. Für jeden Scan filterte es die Flussfilme heraus, segmentierte die fünf Zielgefäße und erzeugte für jeden Herzschlag eine Fluss‑gegen‑Zeit-Kurve – alles ohne menschliches Eingreifen. Expertinnen und Experten überprüften diese Ergebnisse später und stellten fest, dass etwa 90 % der Segmentierungen ausreichend für die klinische Nutzung waren, wenn alle fünf Gefäße vorhanden waren. Das System arbeitete in Patientinnen und Patienten mit besonders ungewöhnlicher Anatomie, wie etwa duplizierten Venen, etwas weniger zuverlässig, lieferte aber dennoch einen riesigen, zuvor unerreichbaren Datensatz sauberer, zeitlich variabler Blutflussmessungen.

Verborgene Flusstypen finden, die mit Outcomes verknüpft sind
Mit Tausenden von Flusskurven suchte das zweite Deep-Learning-Modell des Teams nach natürlichen Gruppen von Patientinnen und Patienten, allein basierend darauf, wie sich das Blut im Zeitverlauf durch ihre Gefäße bewegte. Dieses Modell komprimierte jedes Kurvenpaar – entweder aus den Lungenarterien oder den großen Venen – zu einer kompakten internen Darstellung und gruppierte dann die Patientinnen und Patienten in unterschiedliche Fluss‑„Phänotypen“. Einige Gruppen zeigten ausgewogene, normal große Flüsse; andere wiesen insgesamt reduzierte Flüsse, dominanten Fluss zu einer Lunge oder Flussverschiebung hin zur Entspannungsphase des Herzschlags auf. Die Forschenden verfolgten die Patientinnen und Patienten anschließend über die Zeit und entdeckten, dass bestimmte Flussmuster mit einem höheren Risiko für Tod, Herztransplantation oder Lebererkrankung assoziiert waren – selbst nach Anpassung für Alter, Pumpfunktion des Herzens und andere Standardparameter.
Was das für die zukünftige Versorgung bedeuten könnte
Vereinfacht gesagt zeigt die Studie, dass die Art und Weise, wie Blut durch die Fontan-Zirkulation fließt – welche Gefäße mehr oder weniger Durchfluss führen und zu welchem Zeitpunkt im Herzzyklus – entscheidende Hinweise darauf enthält, welche Patientinnen und Patienten wahrscheinlich schwerwiegende Komplikationen entwickeln. Die Autorinnen und Autoren zeigen, dass künstliche Intelligenz große Archive von Roh‑MRT‑Filmen in aussagekräftige Flussprofile und Risikogruppen verwandeln kann, ohne manuelle Nachzeichnungen oder handgefertigte Regeln. Zukünftig könnte ein solches System direkt nach einer MRT-Untersuchung eines Kindes automatisch laufen, diejenigen markieren, deren Flussmuster Risikogruppen ähneln, und Ärztinnen und Ärzten helfen, Nachsorge, Tests oder sogar operative Planungen besser zu gestalten. Über Fontan-Patienten hinaus ließe sich derselbe Ansatz auf andere Herzkrankheiten, bewegungsverfolgende Bildgebung oder sogar alltägliche Signale wie EKGs übertragen und so Informationen nutzbar machen, die Krankenhäuser bereits sammeln, aber selten tiefgehend auswerten.
Zitation: Yao, T., Clair, N.S., Gong, M. et al. Deep learning for vessel segmentation and flow analysis to identify clusters associated with adverse outcomes in a fontan patient registry. Sci Rep 16, 11956 (2026). https://doi.org/10.1038/s41598-026-40738-6
Schlüsselwörter: Fontan-Zirkulation, Herz-MRT, Deep Learning, Blutflussmuster, Risikostratifizierung von Patienten