Clear Sky Science · it
Apprendimento profondo per la segmentazione dei vasi e l'analisi del flusso per identificare raggruppamenti associati a esiti avversi in un registro di pazienti Fontan
Perché studiare il flusso cardiaco nei bambini è importante
I bambini nati con un solo ventricolo funzionante spesso vengono sottoposti a un intervento complesso chiamato procedura di Fontan per poter sopravvivere fino all’età adulta. Questi pazienti possono apparire stabili per anni, ma alcuni sviluppano in seguito problemi seri che interessano cuore e fegato. I medici raccolgono già esami MRI dettagliati che catturano come il sangue si muove realmente attraverso cuore e vasi nel tempo, ma la maggior parte di questi ricchi dati di movimento non viene mai utilizzata. Questo studio dimostra come l’intelligenza artificiale moderna possa sbloccare a scala queste informazioni nascoste, rivelando schemi di flusso sanguigno collegati a esiti a lungo termine migliori o peggiori.
Trasformare migliaia di scansioni in dati utilizzabili
I ricercatori hanno lavorato con il registro FORCE, una grande raccolta internazionale di esami di risonanza magnetica cardiaca di oltre 3.000 persone con circolazione Fontan. Ogni esame include filmati specializzati che tracciano la velocità del flusso sanguigno attraverso vasi chiave a ogni battito cardiaco. Per apprendere da queste scansioni, il team ha prima dovuto delineare i vasi in ogni fotogramma dell’immagine e misurare il flusso nel tempo — un compito manuale tedioso che avrebbe richiesto, secondo le stime, un anno di lavoro esperto ininterrotto. Invece hanno costruito un modello di deep learning in grado sia di riconoscere quale vaso era ripreso sia di tracciare automaticamente il bordo del vaso per cinque vie principali: l’aorta e quattro grandi vene e arterie dirette verso e dai polmoni.
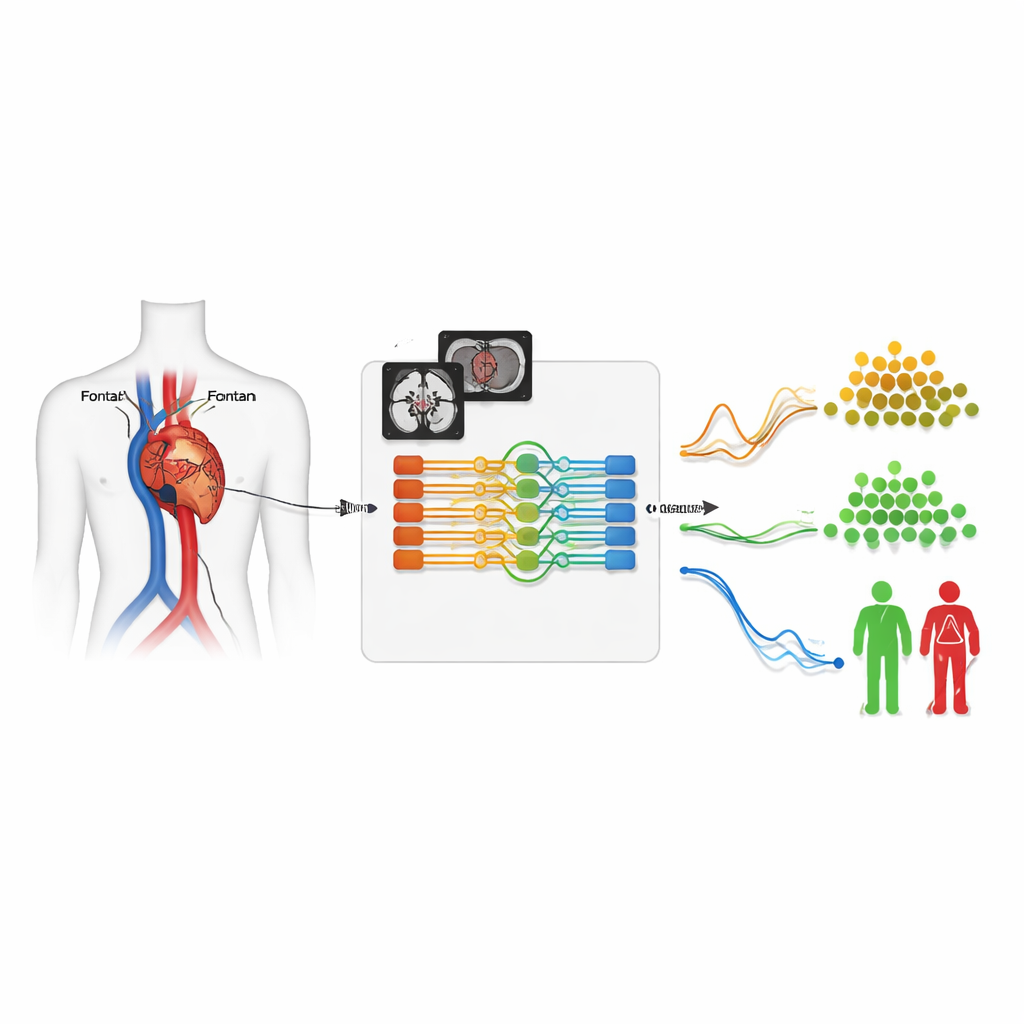
Come funziona il sistema di segmentazione intelligente
Il nucleo del sistema è una rete neurale che analizza ogni filmato come un breve blocco 3D: due dimensioni spaziali più il tempo. Riceve in ingresso due versioni del segnale MRI—una che mostra l’anatomia e l’altra che evidenzia il sangue in movimento—ed è stata addestrata su 260 esami in cui gli esperti avevano già tracciato manualmente i vasi. Il modello non si limita a delineare le strutture; impara anche a identificare quale vaso sia, aiutato dalle informazioni digitate dall’operatore dello scanner al momento dell’acquisizione. Con questo design combinato di classificazione e segmentazione, il sistema ha raggiunto un’elevata sovrapposizione con i tracciati umani e ha identificato correttamente il tipo di vaso in quasi tutti i casi di test, nonostante l’anatomia spesso tortuosa e altamente variabile tipica dei pazienti Fontan.
Scalare all’intero registro internazionale
Una volta validato, il modello è stato inserito in una pipeline automatizzata in cloud e applicato a oltre 4.500 esami del registro. Per ogni scansione, ha individuato i filmati di flusso, segmentato i cinque vasi target e generato una curva flusso‑tempo per ogni battito cardiaco, tutto senza intervento umano. Gli esperti hanno poi verificato questi risultati e hanno riscontrato che circa il 90% delle segmentazioni era sufficientemente valido per uso clinico quando erano presenti tutti e cinque i vasi. Il sistema ha reso leggermente meno bene nei pazienti con anatomie particolarmente insolite, come vene duplicate, ma ha comunque fornito un vasto set di dati precedentemente irraggiungibile di misurazioni pulite e variabili nel tempo del flusso sanguigno.

Trovare tipi di flusso nascosti legati agli esiti
Con migliaia di curve di flusso a disposizione, il secondo modello di deep learning del team ha cercato raggruppamenti naturali di pazienti basandosi esclusivamente su come il sangue si muoveva attraverso i loro vasi nel tempo. Questo modello ha compresso ogni coppia di curve—o dalle arterie polmonari o dalle grandi vene—in una rappresentazione interna compatta e poi ha raggruppato i pazienti in distinti “fenotipi” di flusso. Alcuni gruppi avevano flussi equilibrati e di dimensioni normali; altri mostravano un flusso complessivamente ridotto, un flusso dominante verso un polmone o un flusso spostato verso la fase di rilassamento del battito cardiaco. I ricercatori hanno quindi seguito i pazienti nel tempo e scoperto che certi schemi di flusso erano associati a rischi più elevati di morte, trapianto cardiaco o malattia epatica, anche tenendo conto dell’età, della forza di pompaggio del cuore e di altre misure standard.
Cosa potrebbe significare per le cure future
In termini semplici, lo studio dimostra che il modo in cui il sangue scorre nella circolazione Fontan—quali vasi portano più o meno flusso e in quale momento del battito—contiene indizi vitali su quali pazienti siano più propensi ad affrontare complicazioni serie. Gli autori mostrano che l’intelligenza artificiale può trasformare grandi archivi di filmati MRI grezzi in profili di flusso e gruppi di rischio significativi, senza tracciature manuali o regole costruite a mano. In futuro, un sistema come questo potrebbe funzionare automaticamente subito dopo la risonanza di un bambino, segnalando quelli i cui schemi di flusso somigliano ai gruppi a rischio più elevato e aiutando i medici a personalizzare follow‑up, accertamenti o persino la pianificazione chirurgica. Oltre ai pazienti Fontan, lo stesso approccio potrebbe essere adattato ad altre condizioni cardiache, a esami di tracciamento del movimento o perfino a segnali di uso comune come l’ECG, sfruttando in modo più completo le informazioni che gli ospedali già raccolgono ma raramente approfondiscono.
Citazione: Yao, T., Clair, N.S., Gong, M. et al. Deep learning for vessel segmentation and flow analysis to identify clusters associated with adverse outcomes in a fontan patient registry. Sci Rep 16, 11956 (2026). https://doi.org/10.1038/s41598-026-40738-6
Parole chiave: Circolazione Fontan, risonanza magnetica cardiaca, apprendimento profondo, schemi di flusso sanguigno, stratificazione del rischio del paziente