Clear Sky Science · nl
Computationele modellering van het reconstrueren en dempen van aanvallen via modelreferentie‑controle
Waarom het kalmeren van aanvallen met slimme computers ertoe doet
Epileptische aanvallen kunnen plotseling optreden, het dagelijks leven verstoren en in ernstige gevallen de veiligheid in gevaar brengen. Artsen gebruiken al elektrische stimulatie om sommige patiënten te helpen, maar de exacte instellingen — hoe sterk, hoe vaak en in welk patroon te stimuleren — worden nog grotendeels door proef en fout gekozen. Dit artikel onderzoekt een nieuwe manier om computers en echte hersenopnames te gebruiken om eerst op virtuele aanvallen te «oefenen», zodat men leert hoe die op scherm verzwakt kunnen worden voordat er enige stroom bij een patiënt wordt toegepast.
Patronen zien in onrustige hersengolven
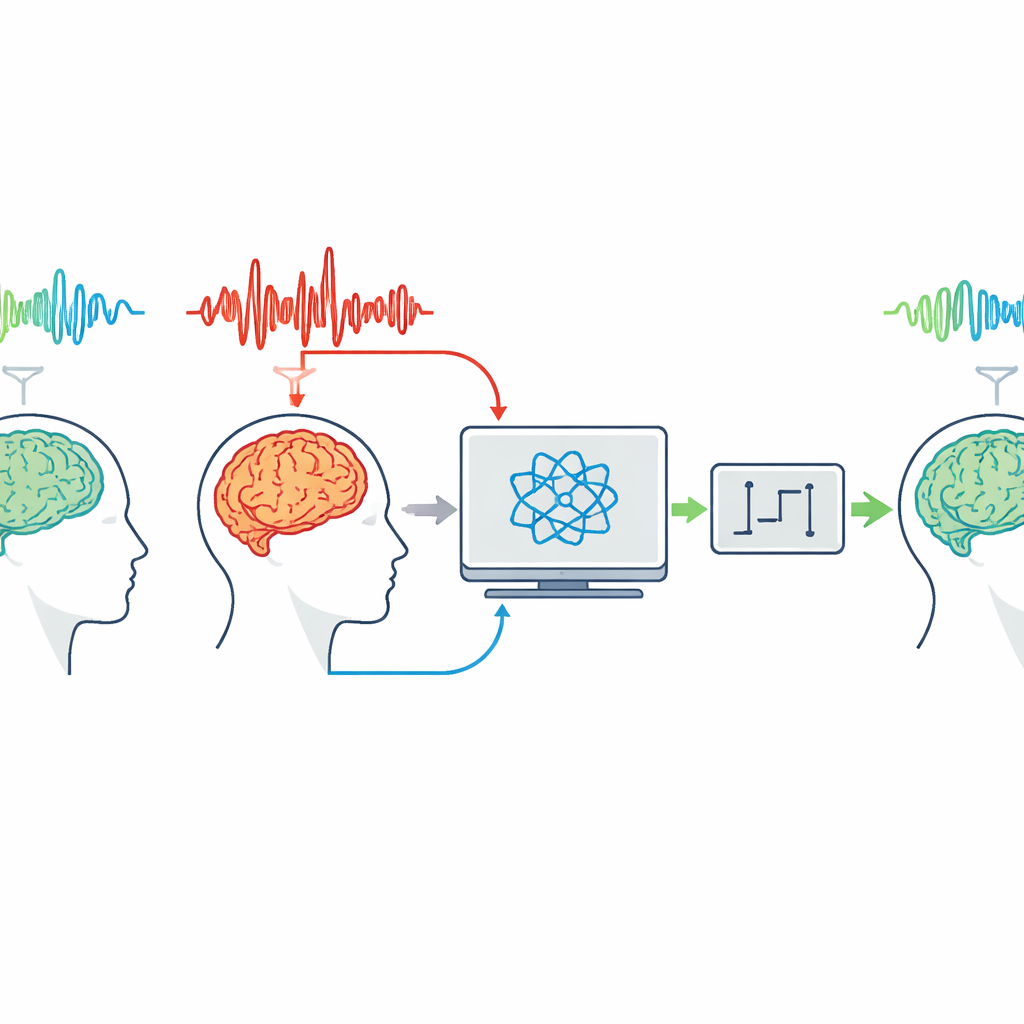
De auteurs vertrekken van het idee dat aanval- en niet‑aanval‑hersenenactiviteit elk hun eigen herkenbare elektrische handtekening hebben. Met behulp van scalp‑EEG en intracraniële EEG van mensen met gegeneraliseerde tonisch‑clonische aanvallen vergelijken ze hersengolven tijdens rustige periodes en tijdens volledige aanvallen. Zelfs zonder zware filtering vertonen aanvallen veel grotere uitslagen en meer regelmatige, laagfrequente pulsen dan de meer onregelmatige, lagere amplitude achtergrondactiviteit. In het frequentiedomein dragen aanvallen extra energie bij lage frequenties en rekruteren ze in de loop van de tijd bredere banden, wat erop wijst dat enkele dominante ritmes de abnormale activiteit helpen aandrijven.
Vereenvoudigde representaties van complexe hersenen bouwen
In plaats van te proberen elk detail van de hersenen te reproduceren, bouwen de onderzoekers zeer eenvoudige ‘‘stand‑in’’ modellen die zich gedragen als één trillend systeem — vergelijkbaar met een massa aan een veer of een basaal elektrisch circuit. Ze identificeren deze modellen direct uit opgenomen EEG‑ en iEEG‑signalen met wiskundige hulpmiddelen gebaseerd op orthogonale functies (in de praktijk Fourier‑achtige bouwstenen). Eén model wordt passend gemaakt op niet‑aanvalgegevens en een ander op aanvalgegevens. Op zichzelf zijn deze modellen ruw, maar wanneer ze in een terugkoppelingslus worden geplaatst die continu de uitvoer van het model naar de echte opname bijstuurt, volgt de gesimuleerde activiteit het werkelijke aanval‑ of niet‑aanvalsignaal nauwkeurig. Een belangrijke afstelschakelaar, de verval‑snelheid, bepaalt hoe snel het model naar de data wordt gedwongen te volgen — en hoe sterk de vereiste input moet zijn.
Het model leren aanvallen terug naar normaal te duwen
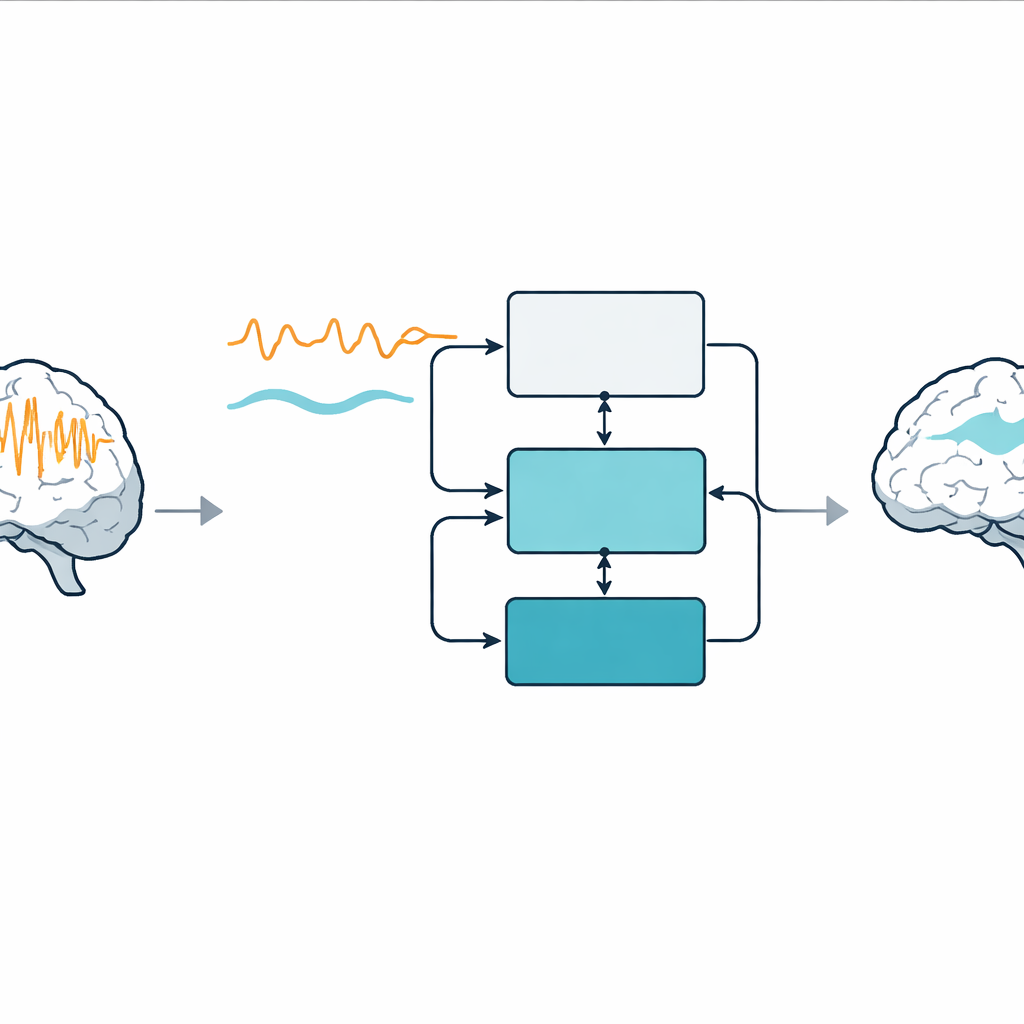
Zodra een aanvalmodel de aanval van een patiënt betrouwbaar kan herhalen, voegen de auteurs een tweede terugkoppelingslus toe waarvan de taak is de aanvalachtige activiteit meer op het niet‑aanvalpatroon te laten lijken. Dit staat bekend als modelreferentie‑controle: het niet‑aanvalmodel definieert het gewenste gedrag en de regelaar berekent een elektrische stimulatie die het aanvalmodel naar die referentie stuurt. Twee versies worden getest. In de adaptieve versie veranderen de versterkingen van de regelaar in de tijd op basis van hoe goed deze presteert, wat burst‑achtige pulsen oplevert die de aanval over de hele opname ruwweg met een derde in vermogen verzwakken. In de vaste‑versterkingversie hergebruikt de regelaar een versterking die oorspronkelijk was ontworpen om niet‑aanvalactiviteit te reconstrueren; met geschikte afstemming kan deze eenvoudigere optie het aanvalvermogen met meer dan 80% terugbrengen terwijl relatief bescheiden stimulussterktes worden gebruikt.
Realistische stimulatierecepten vinden
De studie onderzoekt ook hoe ontwerpskeuzes zowel effectiviteit als veiligheid beïnvloeden. Hogere verval‑snelheden laten de modellen beter bij de data passen maar vragen sterkere stimulatie en kunnen de procentuele onderdrukking van de aanval zelfs verminderen. Er is een duidelijk compromis: een betere beschrijving van de aanval vraagt om intensere pulsen om deze te temmen. Door parameters aan te passen en doelbewust de maximale uitgang te limiteren, houden de auteurs de gesimuleerde spanningen overwegend binnen ongeveer 5 tot 18 volt en frequenties van ruwweg 2 tot 80 hertz — bereiken die overlappen met wat al in klinische hersenstimulatie voor epilepsie en andere aandoeningen wordt gebruikt. Ze laten zien dat methoden zoals het verzadigen van de uitgang of het aan‑ en uitzetten van de regelaar de intensiteit verder kunnen begrenzen terwijl er toch sprake is van betekenisvolle demping.
Van virtuele regelslussen naar hulpmiddelen aan het bed
Hoewel deze experimenten volledig computationeel zijn, schetsen ze een praktisch stappenplan. In dagelijks toezicht zouden lange periodes van niet‑aanval‑EEG kunnen worden gebruikt om een eenvoudige referentiemodel en zijn regelaar bij te werken. Wanneer een aanval wordt gedetecteerd, zou dezelfde regelaar — ontworpen zonder die aanval vooraf te hoeven zien — een open‑loop stimulator kunnen aansturen die pulsen levert met vormen, frequenties en amplitude geïnformeerd door de virtuele experimenten. Een afzonderlijk monitoringssysteem zou beoordelen of de echte aanval afneemt en de input dienovereenkomstig aanpassen of beperken. Simpel gezegd suggereert dit werk dat computers kunnen oefenen hoe aanvallen het beste te kalmeren met behulp van eerdere opnames, en artsen duidelijkere richtlijnen kunnen bieden over «hoe te stimuleren» in plaats van uitsluitend op proef en fout te vertrouwen.
Bronvermelding: Brogin, J.A.F., Faber, J., Ryvlin, P. et al. Computational modeling of seizure reconstruction and attenuation via model reference control. Sci Rep 16, 9951 (2026). https://doi.org/10.1038/s41598-026-39645-7
Trefwoorden: epilepsie, aanvalbeheersing, hersenstimulatie, computationele modellering, EEG