Clear Sky Science · de
Computergestützte Modellierung zur Rekonstruktion und Abschwächung von Anfällen mittels Model Reference Control
Warum das Beruhigen von Anfällen mit intelligenten Computern wichtig ist
Epileptische Anfälle können plötzlich auftreten, den Alltag stören und in schweren Fällen die Sicherheit gefährden. Ärztinnen und Ärzte setzen bereits elektrische Stimulation ein, um manchen Patientinnen und Patienten zu helfen, doch die genauen Einstellungen—wie stark, wie oft und in welchem Muster stimuliert werden soll—werden weiterhin weitgehend durch Ausprobieren bestimmt. Diese Arbeit untersucht eine neue Methode, bei der Computer und echte Hirnaufzeichnungen genutzt werden, um zunächst an virtuellen Anfällen zu "üben" und zu lernen, wie man sie auf dem Bildschirm abschwächt, bevor irgendein Strom an einen Patienten geliefert wird.
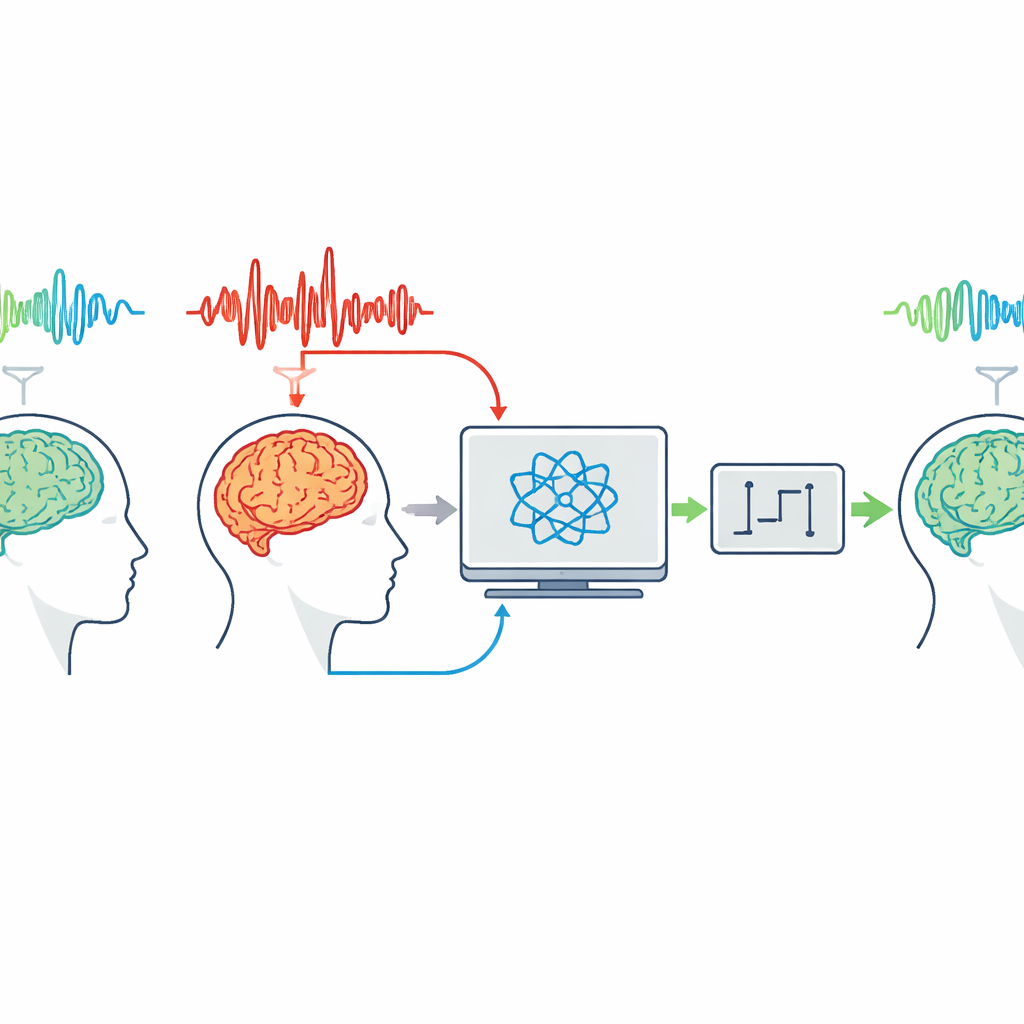
Muster in stürmischen Hirnwellen erkennen
Die Autorinnen und Autoren beginnen mit der Annahme, dass Anfalls- und Nicht-Anfalls-Aktivität jeweils ihre erkennbaren elektrischen Signaturen besitzen. Anhand von EEG an der Kopfoberfläche und intrakraniellen EEGs von Menschen mit generalisierten tonisch‑klonischen Anfällen vergleichen sie Hirnwellen, die in ruhigen Perioden und während kompletter Anfälle aufgezeichnet wurden. Selbst ohne starke Filter weisen Anfälle deutlich größere Ausschläge und regelmäßigere, niederfrequente Impulse auf als die unregelmäßigere, niedrigamplitudige Hintergrundaktivität. Im Frequenzbereich zeigen Anfälle zusätzliche Leistung bei niedrigen Frequenzen und rekrutieren im Zeitverlauf breitere Bänder, was darauf hindeutet, dass wenige dominante Rhythmen die abnorme Aktivität antreiben.
Einfache Stellvertreter für komplexe Gehirne bauen
Statt zu versuchen, jedes Detail des Gehirns nachzubilden, entwickeln die Forschenden sehr einfache „Dummy“-Modelle, die sich wie ein einzelnes schwingendes System verhalten—ähnlich einem Masse‑Feder‑System oder einem einfachen elektrischen Schaltkreis. Sie bestimmen diese Modelle direkt aus aufgezeichneten EEG‑ und iEEG‑Signalen mithilfe mathematischer Werkzeuge auf Basis orthogonaler Funktionen (praktisch Fourier‑ähnliche Bausteine). Ein Modell wird an Nicht‑Anfalls‑Daten angepasst, ein anderes an Anfallsdaten. Für sich genommen sind diese Modelle grob, doch wenn sie in eine Rückkopplungsschleife gesetzt werden, die die Modellausgabe kontinuierlich an die reale Aufzeichnung anpasst, folgt die simulierte Aktivität dem echten Anfalls‑ oder Nicht‑Anfalls‑Signal sehr genau. Ein wichtiger Einstellparameter, die Abklingrate, legt fest, wie schnell das Modell gezwungen wird, den Daten zu folgen—und wie stark die dafür nötige Eingabe sein muss.
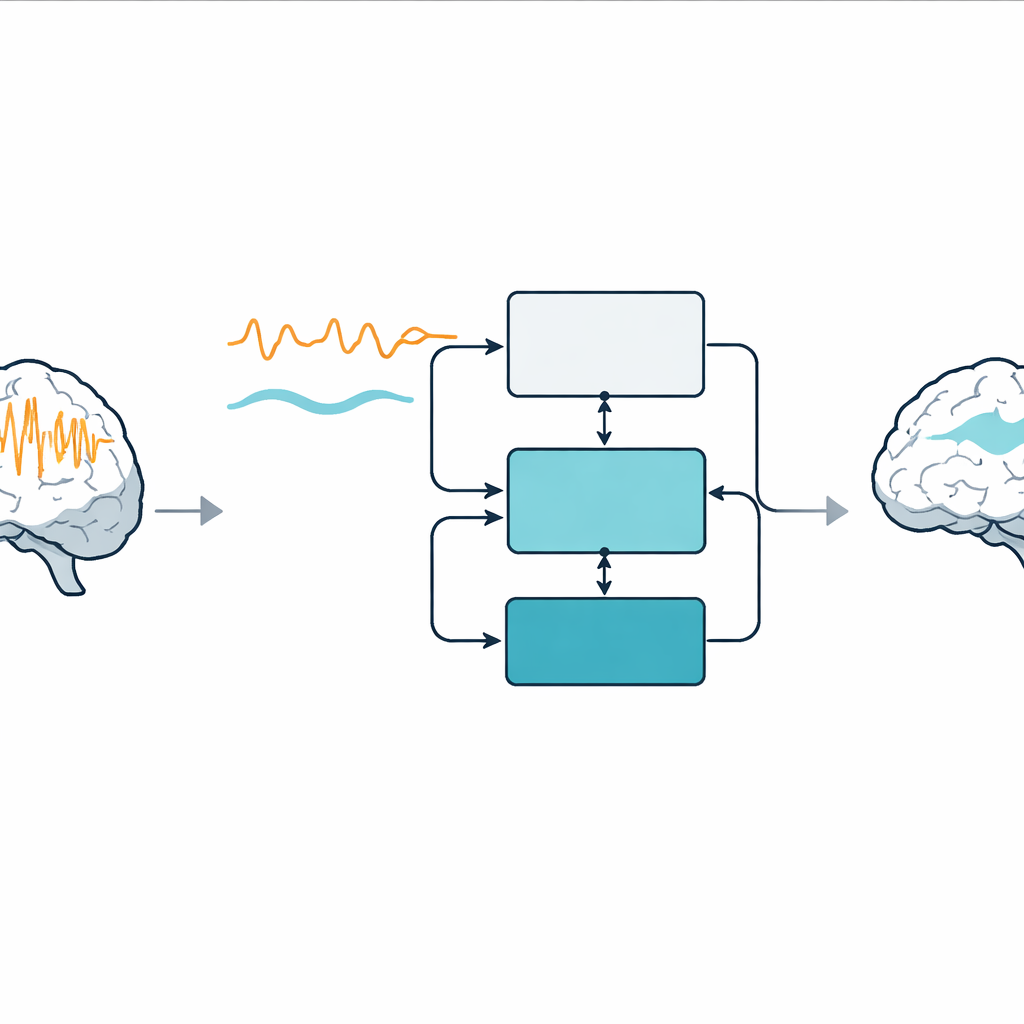
Das Modell darin trainieren, Anfälle zurück in Richtung Normalzustand zu drücken
Sobald ein Anfallsmodell den Anfall eines Patienten treu wiedergeben kann, fügen die Autorinnen und Autoren eine zweite Rückkopplungsschleife hinzu, deren Aufgabe es ist, die anfallsähnliche Aktivität dem Nicht‑Anfalls‑Muster anzugleichen. Dies ist als Model Reference Control bekannt: Das Nicht‑Anfalls‑Modell definiert das gewünschte Verhalten und der Regler berechnet einen elektrischen Stimulus, der das Anfallsmodell in Richtung dieser Referenz treibt. Es werden zwei Versionen getestet. In der adaptiven Version ändern sich die Verstärkungen des Reglers im Zeitverlauf abhängig von seiner Leistung und erzeugen impulshaftes Stimulationsverhalten, das die Anfallsleistung in der gesamten Aufzeichnung um etwa ein Drittel reduziert. In der Festverstärkungs‑Version verwendet der Regler eine ursprünglich zur Rekonstruktion von Nicht‑Anfalls‑Aktivität entworfene Verstärkung; mit geeigneter Abstimmung kann diese einfachere Variante die Anfallsleistung um mehr als 80 % reduzieren, während vergleichsweise moderate Stimulusstärken zum Einsatz kommen.
Realistische Stimulationsrezepte finden
Die Studie untersucht außerdem, wie Designentscheidungen sowohl Wirksamkeit als auch Sicherheit beeinflussen. Höhere Abklingraten lassen die Modelle die Daten besser abbilden, erfordern jedoch stärkere Stimulation und können den prozentualen Anteil der Anfallsunterdrückung tatsächlich verringern. Es besteht ein klarer Zielkonflikt: Eine bessere Beschreibung des Anfalls verlangt intensivere Impulse, um ihn zu zähmen. Durch Anpassung von Parametern und eine bewusste Begrenzung der maximalen Ausgabe halten die Forschenden die simulierten Spannungen größtenteils im Bereich von etwa 5 bis 18 Volt und die Frequenzen grob zwischen 2 und 80 Hertz—Bereiche, die sich mit denen überschneiden, die bereits in der klinischen Gehirnstimulation bei Epilepsie und anderen Störungen verwendet werden. Sie zeigen, dass Methoden wie Sättigung der Ausgabe oder das zeitweilige Ein‑ und Ausschalten des Reglers die Intensität weiter begrenzen können, während dennoch eine sinnvolle Abschwächung erreicht wird.
Von virtuellen Regelkreisen zu bettennahen Werkzeugen
Auch wenn diese Experimente vollständig rechnerisch sind, skizzieren sie eine praktikable Roadmap. Im Alltagsmonitoring könnten lange Abschnitte von Nicht‑Anfalls‑EEG dazu dienen, ein einfaches Referenzmodell und seinen Regler fortlaufend zu aktualisieren. Wenn ein Anfall erkannt wird, könnte derselbe Regler—ohne dass dieser spezielle Anfall im Voraus gesehen werden muss—einen offenen Stimulator steuern, der Impulse mit Formen, Frequenzen und Amplituden abgibt, die von den virtuellen Experimenten informiert sind. Ein separates Überwachungssystem würde beurteilen, ob der reale Anfall nachlässt, und die Eingabe entsprechend anpassen oder begrenzen. Einfach gesagt legt diese Arbeit nahe, dass Computer mithilfe vergangener Aufzeichnungen proben können, wie man Anfälle am besten beruhigt, und Ärztinnen und Ärzten damit klarere Hinweise zum "Wie stimulieren" geben, statt sich allein auf Trial‑and‑Error zu verlassen.
Zitation: Brogin, J.A.F., Faber, J., Ryvlin, P. et al. Computational modeling of seizure reconstruction and attenuation via model reference control. Sci Rep 16, 9951 (2026). https://doi.org/10.1038/s41598-026-39645-7
Schlüsselwörter: Epilepsie, Anfallskontrolle, Gehirnstimulation, computationales Modellieren, EEG