Clear Sky Science · es
Modelado computacional de la reconstrucción y atenuación de convulsiones mediante control por referencia de modelo
Por qué importa calmar las convulsiones con ordenadores inteligentes
Las convulsiones epilépticas pueden aparecer de forma súbita, interrumpiendo la vida cotidiana y, en casos graves, poniendo en riesgo la seguridad. Los médicos ya utilizan la estimulación eléctrica para ayudar a algunos pacientes, pero los ajustes exactos —qué intensidad, con qué frecuencia y en qué patrón estimular— siguen escogiendo en gran medida por prueba y error. Este artículo explora una nueva manera de usar ordenadores y registros reales del cerebro para “practicar” primero con convulsiones virtuales, aprendiendo cómo debilitarlas en pantalla antes de aplicar corriente a un paciente.
Ver patrones en ondas cerebrales tormentosas
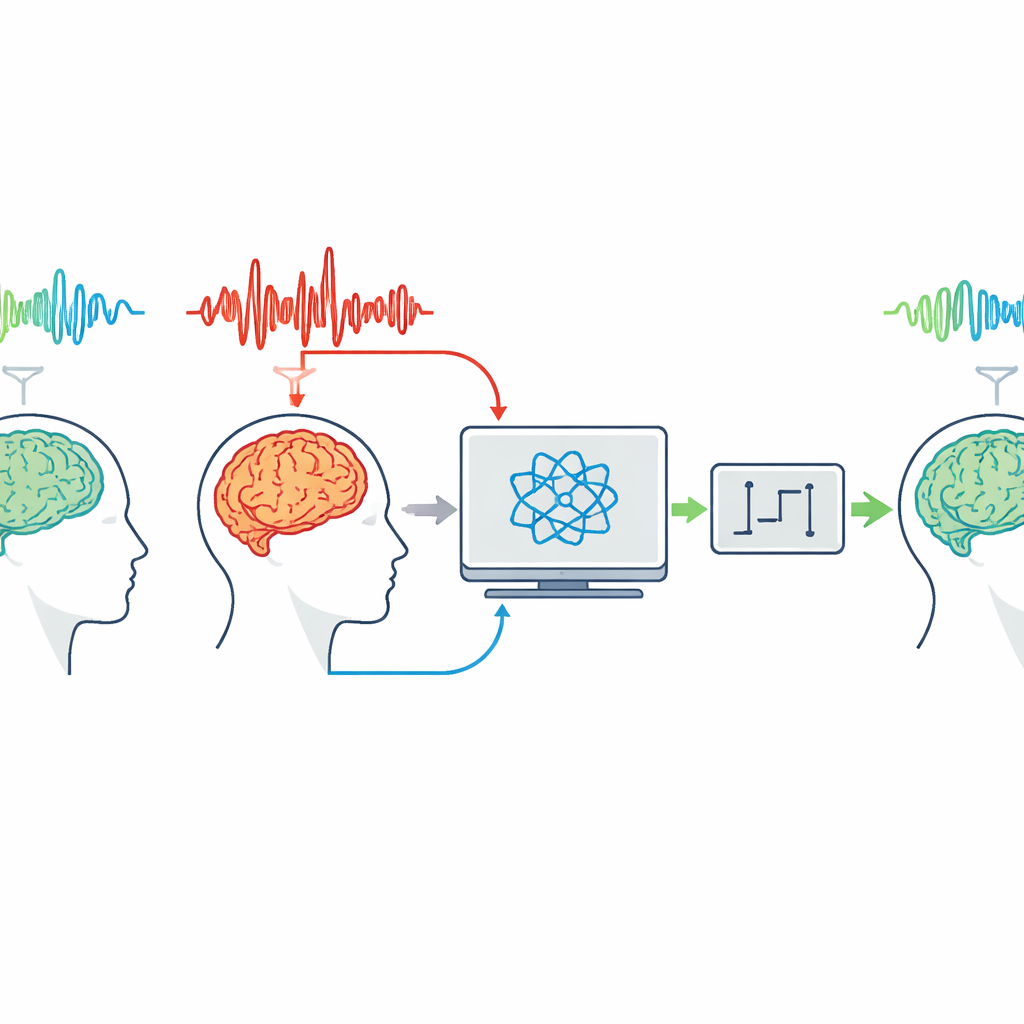
Los autores parten de la idea de que la actividad cerebral con y sin convulsiones tiene cada una su firma eléctrica reconocible. Usando EEG de superficie e intracraneal de personas con convulsiones tónico-clónicas generalizadas, comparan las ondas cerebrales registradas durante periodos tranquilos y durante convulsiones activas. Incluso sin filtros intensos, las convulsiones muestran oscilaciones mucho más grandes y ráfagas regulares de baja frecuencia en contraste con la actividad de fondo, más irregular y de menor amplitud. En el dominio de la frecuencia, las convulsiones presentan potencia adicional en las bajas frecuencias y reclutan bandas más amplias con el tiempo, lo que sugiere que unos pocos ritmos dominantes contribuyen a impulsar la actividad anómala.
Construir sustitutos simples para cerebros complejos
En lugar de intentar reproducir cada detalle del cerebro, el equipo construye modelos muy sencillos que se comportan como un único sistema vibrante—similar en espíritu a una masa en un resorte o a un circuito eléctrico básico. Identifican estos modelos directamente a partir de señales EEG e iEEG grabadas usando herramientas matemáticas basadas en funciones ortogonales (en la práctica, bloques de construcción tipo Fourier). Un modelo se ajusta a los datos sin convulsión y otro a los datos con convulsión. Por sí solos, estos modelos son toscos, pero cuando se colocan en un lazo de retroalimentación que empuja continuamente la salida del modelo hacia el registro real, la actividad simulada sigue de cerca la señal verdadera de convulsión o de no convulsión. Un ajuste clave, denominado tasa de decaimiento, determina qué tan rápido el modelo se fuerza a seguir los datos—y cuánta entrada es necesaria.
Enseñar al modelo a devolver las convulsiones a la normalidad
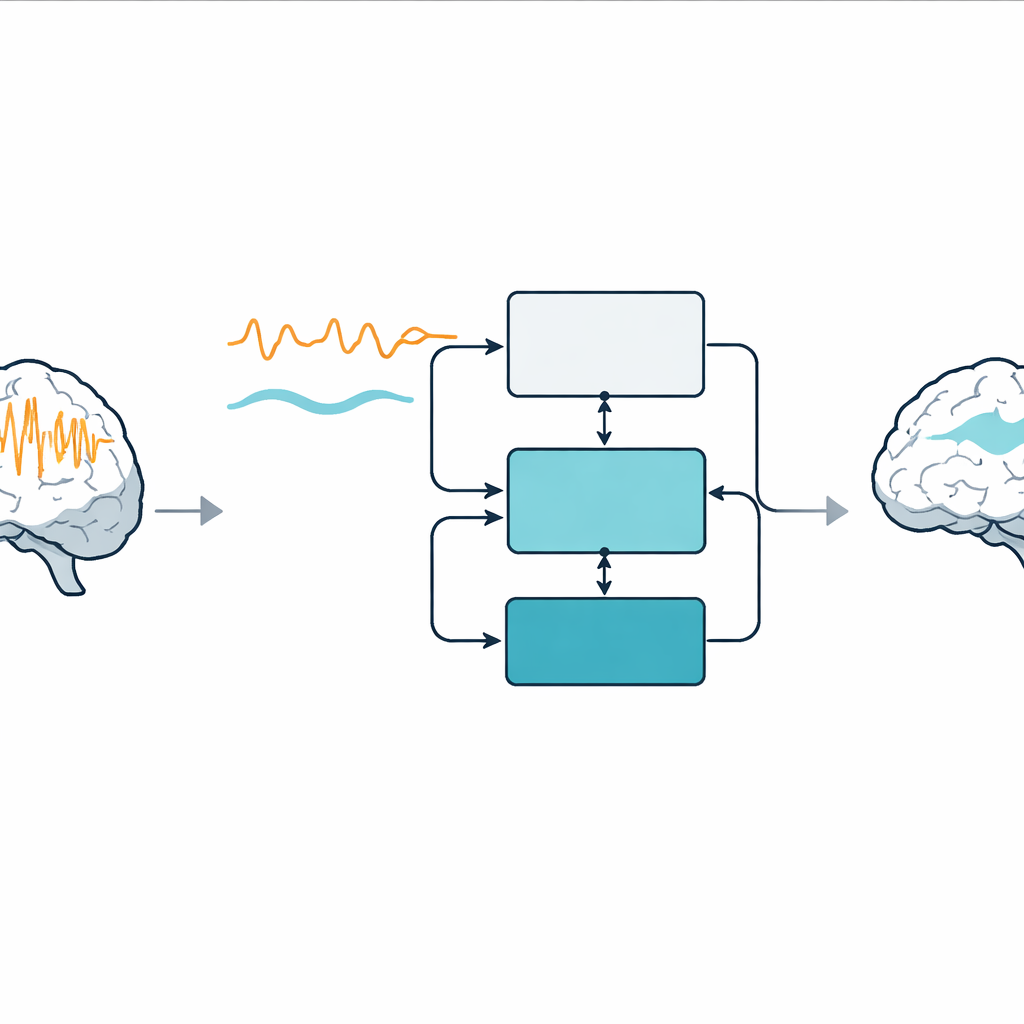
Una vez que un modelo de convulsión puede reproducir fielmente la convulsión de un paciente, los autores añaden un segundo lazo de retroalimentación cuya tarea es hacer que la actividad parecida a una convulsión se asemeje al patrón de no convulsión. Esto se conoce como control por referencia de modelo: el modelo de no convulsión define el comportamiento deseado, y el controlador calcula un estímulo eléctrico que conduce al modelo de convulsión hacia esa referencia. Se prueban dos versiones. En la versión adaptativa, las ganancias del controlador cambian con el tiempo según su rendimiento, produciendo pulsos tipo ráfaga que debilitan la convulsión a lo largo de la grabación en aproximadamente un tercio de su potencia. En la versión de ganancia fija, el controlador reutiliza una ganancia diseñada originalmente para reconstruir la actividad sin convulsión; con un ajuste adecuado, esta opción más simple puede reducir la potencia de la convulsión en más del 80% mientras emplea intensidades de estímulo relativamente moderadas.
Encontrar recetas de estimulación realistas
El estudio también examina cómo las decisiones de diseño afectan tanto la eficacia como la seguridad. Tasas de decaimiento más altas hacen que los modelos coincidan mejor con los datos pero exigen una estimulación más intensa y pueden, de hecho, reducir el porcentaje de supresión de la convulsión. Hay una compensación clara: una mejor descripción de la convulsión requiere pulsos más intensos para dominarla. Ajustando parámetros y limitando deliberadamente la salida máxima, los autores mantienen los voltajes simulados mayormente entre unos 5 y 18 voltios y frecuencias entre aproximadamente 2 y 80 hertz—rangos que se solapan con los ya utilizados en la estimulación cerebral clínica para la epilepsia y otros trastornos. Demuestran que métodos como saturar la salida o encender y apagar el controlador pueden acotar aún más la intensidad mientras se logra una atenuación significativa.
De bucles de control virtuales a herramientas junto a la cama
Aunque estos experimentos son enteramente computacionales, trazan una hoja de ruta práctica. En el monitoreo cotidiano, largos periodos de EEG sin convulsiones podrían usarse para actualizar continuamente un modelo de referencia simple y su controlador. Cuando se detecte una convulsión, el mismo controlador—diseñado sin necesidad de ver esa convulsión de antemano—podría activar un estimulador en lazo abierto que entregue pulsos con formas, frecuencias y amplitudes informadas por los experimentos virtuales. Un sistema de supervisión separado evaluaría si la convulsión real está disminuyendo y ajustaría o limitaría la entrada en consecuencia. En términos sencillos, este trabajo sugiere que los ordenadores pueden ensayar cómo calmar mejor las convulsiones usando grabaciones pasadas, ofreciendo a los médicos una guía más clara sobre “cómo estimular” en lugar de depender únicamente del ensayo y error.
Cita: Brogin, J.A.F., Faber, J., Ryvlin, P. et al. Computational modeling of seizure reconstruction and attenuation via model reference control. Sci Rep 16, 9951 (2026). https://doi.org/10.1038/s41598-026-39645-7
Palabras clave: epilepsia, control de convulsiones, estimulación cerebral, modelado computacional, EEG