Clear Sky Science · nl
Verschillende patronen van samenhang tussen corticale grootschalige netwerken en activiteit in de nucleus subthalamicus bij de ziekte van Parkinson
Waarom deze hersenstudie ertoe doet
De ziekte van Parkinson staat vooral bekend om tremor en traagheid van beweging, maar onder die symptomen ligt een probleem van verstoorde communicatie in de hersenen. Artsen kunnen tijdens operaties al activiteit diep in de hersenen afluisteren, maar ze willen bij voorkeur die signalen niet-invasief van buitenaf kunnen lezen, met behulp van hersenscans. Deze studie stelt een eenvoudige maar krachtige vraag: kunnen patronen van activiteit die vanaf de hersenoppervlakte worden gemeten onthullen wat er diep in een klein gebied gebeurt dat de nucleus subthalamicus heet en een sleutelrol speelt bij Parkinson?
Diepe en oppervlakkige hersensignalen samen bekijken
De onderzoekers registreerden hersenactiviteit van 27 mensen met de ziekte van Parkinson die recentelijk elektroden voor diepe hersenstimulatie hadden gekregen. Terwijl de patiënten rustig zaten met open ogen, mat het team twee soorten signalen tegelijk: magneto-encefalografie (MEG), die snelle activiteit van over het buitenste hersenoppervlak detecteert, en lokale veldpotentialen uit de nucleus subthalamicus diep in de hersenen. Elke persoon werd getest zowel na het stoppen met hun Parkinsonmedicatie als opnieuw na inname van hun gebruikelijke dosis van een snelwerkend middel. Dit ontwerp stelde het team in staat te zien hoe communicatiepatronen in de hersenen veranderden met en zonder medicatie.
Verborgen netwerken die aan- en uitflikkeren
In plaats van de buitenste hersenen als één uniform gebied te beschouwen, gebruikten de wetenschappers een wiskundige methode genaamd een hidden Markov-model om netwerken van regio’s te onthullen die de neiging hebben kortdurend samen actief te worden. Deze netwerken, eerder in gezonde mensen in kaart gebracht, omvatten een “sensorimotorisch” netwerk dat betrokken is bij beweging en een “default mode”-netwerk dat samenhangt met naar binnen gerichte gedachten. Door milliseconde voor milliseconde door de opnamen te schuiven, identificeerde het model wanneer elk netwerk het meest actief was en hoeveel tijd ieders hersenen in deze verschillende patronen doorbrachten.
Diepe hersenritmes gekoppeld aan specifieke netwerken
Toen het team deze netwerkactivaties vergeleek met activiteit in de nucleus subthalamicus, kwamen duidelijke verbanden naar voren. Tijdens activaties van het sensorimotorische netwerk toonde de nucleus subthalamicus sterkere ritmische activiteit in het beta-bereik, een frequentieband die bij Parkinson al bekend staat als overmatig aanwezig en geassocieerd met korte “beta-bursts”. Deze periodes lieten ook een strakkere synchronisatie zien tussen de nucleus subthalamicus en een bewegingsgerelateerd gebied, de supplementary motor area. Het default mode-netwerk vertelde een ander verhaal: diens activaties waren gekoppeld aan lagere-frequentie ritmes in de nucleus subthalamicus en verhoogde synchronie op tragere snelheden, wat wijst op een onderscheiden functionele toestand die mogelijk meer te maken heeft met niet-motorische aspecten van de ziekte.
Medicatie-effecten hangen af van de hersentoestand
De onderzoekers onderzochten vervolgens hoe Parkinsonmedicatie deze diepe ritmes veranderde. Gemiddeld verminderde medicatie de beta-activiteit in de nucleus subthalamicus, in lijn met eerdere studies. Maar bekeken door de lens van de grootschalige netwerken verscheen een genuanceerder beeld. De sterkste medicatiegerelateerde verminderingen in beta-vermogen deden zich voor tijdens netwerktoestanden die geen bijzonder sterke koppeling lieten zien tussen de nucleus subthalamicus en motorische gebieden. Daarentegen waren het sensorimotorische en het default mode-netwerk — waar diepe en oppervlakkige gebieden het meest nauw communiceerden — minder duidelijk beïnvloed. Een onafhankelijke dataset van een andere onderzoeksgroep bevestigde grotendeels de kernbevinding dat bepaalde netwerken gekoppeld zijn aan onderscheidende diepe hersenritmepatronen, hoewel de medicatie-effecten daar zwakker waren.
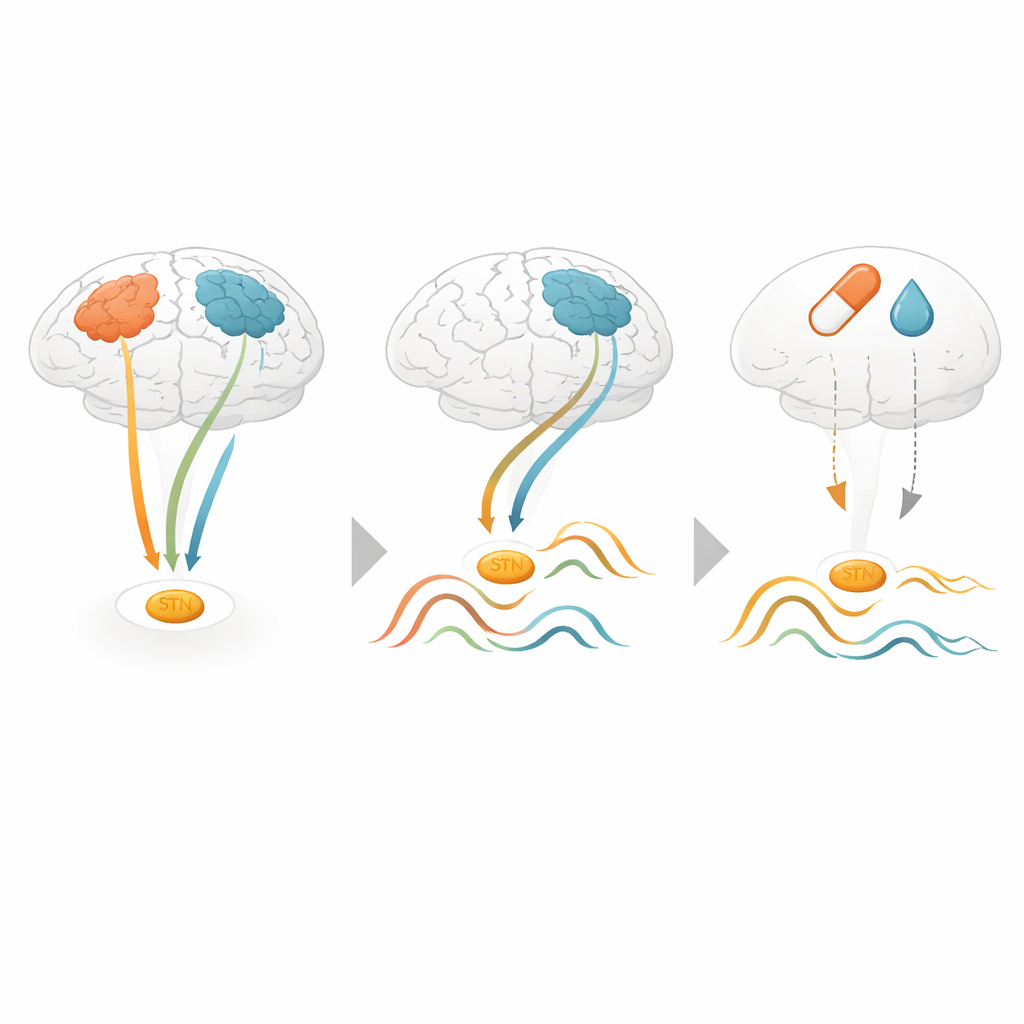
Wat dit betekent voor toekomstige behandeling
Voor een niet-specialistische lezer is de kernboodschap dat de hersenen zich niet in één constante Parkinson-toestand bevinden. In plaats daarvan schakelen ze tussen verschillende grootschalige patronen en elk patroon komt overeen met een specifieke “stemming” van de diepe structuur die door chirurgie en medicijnen wordt gericht. Omdat deze patronen niet-invasief vanaf de hersenoppervlakte kunnen worden gedetecteerd, zouden ze uiteindelijk kunnen dienen als externe markers om diagnose te sturen, ziekteprogressie te monitoren of adaptieve diepe hersenstimulatie te activeren alleen wanneer schadelijke ritmes verschijnen. Op die manier kan het lezen van de taal van hersen-netwerken nieuwe vensters openen op de verborgen werking van de ziekte van Parkinson en clinici helpen behandelingen af te stemmen op de moment-tot-moment behoeften van de hersenen.
Bronvermelding: Kohl, O., Gohil, C., Sure, M. et al. Varying patterns of association between cortical large-scale networks and subthalamic nucleus activity in Parkinson’s disease. npj Parkinsons Dis. 12, 106 (2026). https://doi.org/10.1038/s41531-026-01372-1
Trefwoorden: Ziekte van Parkinson, hersen-netwerken, diepe hersenstimulatie, beta-ritmes, magneto-encefalografie