Clear Sky Science · de
Variierende Muster der Assoziation zwischen großräumigen kortikalen Netzwerken und Aktivität des Nucleus subthalamicus bei Parkinson
Warum diese Gehirn‑Studie wichtig ist
Morbus Parkinson ist vor allem für Zittern und Bewegungsverlangsamung bekannt, doch diesen Symptomen liegt ein Problem gestörter Informationsübertragung im Gehirn zugrunde. Ärzte können während Operationen bereits die Aktivität tiefer Hirnregionen messen, würden solche Signale aber lieber von außen und nicht invasiv erfassen, etwa mit bildgebenden Verfahren. Diese Studie stellt eine einfache, aber wichtige Frage: Lassen sich Muster der an der Hirnoberfläche messbaren Aktivität so lesen, dass sie Rückschlüsse auf das Geschehen in einer kleinen, tief liegenden Region — dem Nucleus subthalamicus, der eine zentrale Rolle bei Parkinson spielt — zulassen?
Tiefe und oberflächliche Signale gemeinsam betrachten
Die Forschenden zeichneten die Gehirnaktivität von 27 Menschen mit Parkinson auf, die kürzlich Elektroden für die tiefe Hirnstimulation erhalten hatten. Während die Patienten ruhig mit offenen Augen saßen, maßen sie gleichzeitig zwei Signalarten: Magnetoenzephalographie (MEG), die schnelle Aktivität über die äußere Hirnoberfläche erfasst, und lokale Feldpotenziale aus dem tief im Gehirn liegenden Nucleus subthalamicus. Jede Person wurde einmal nach Absetzen der Parkinson‑Medikation und einmal nach Einnahme der üblichen Dosis eines schnell wirkenden Medikaments untersucht. Dieses Design erlaubte es, Veränderungen der Kommunikationsmuster im Gehirn mit und ohne Medikamenteneinfluss zu beobachten.
Verborgene Netzwerke, die aufblitzen
Statt die Hirnoberfläche als einheitlichen Bereich zu behandeln, setzten die Wissenschaftlerinnen und Wissenschaftler ein mathematisches Verfahren — ein Hidden‑Markov‑Modell — ein, um Netzwerke von Regionen zu identifizieren, die für kurze Zeiträume gemeinsam aktiv werden. Diese Netzwerke, die zuvor bei gesunden Menschen kartiert wurden, umfassen ein „sensorimotorisches“ Netzwerk, das an Bewegung beteiligt ist, und ein „default‑mode“‑Netzwerk, das mit nach innen gerichteten Gedanken verknüpft ist. Indem das Modell die Aufzeichnungen Millisekunde für Millisekunde durchging, bestimmte es, wann jedes Netzwerk am aktivsten war und wie viel Zeit das Gehirn jeder Person in diesen unterschiedlichen Mustern verbrachte.
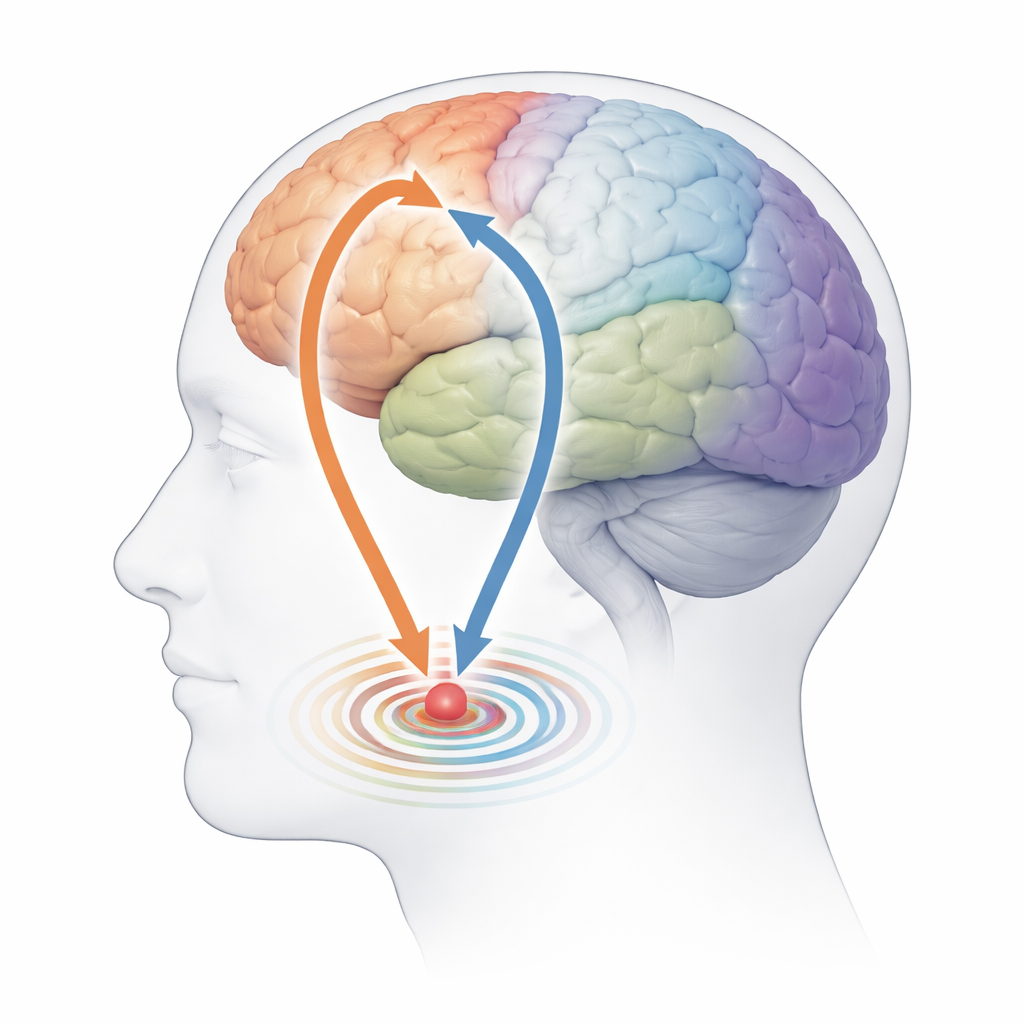
Tiefe Hirnrhythmen mit bestimmten Netzwerken verknüpft
Beim Vergleich dieser Netzwerk‑Episoden mit der Aktivität im Nucleus subthalamicus traten klare Verbindungen zutage. Während Aktivierungen des sensorimotorischen Netzwerks zeigte der Nucleus subthalamicus stärkere rhythmische Aktivität im Beta‑Bereich — ein Frequenzband, das bei Parkinson bereits als übermäßig ausgeprägt und mit kurzen „Beta‑Burst“‑Episoden assoziiert ist. Diese Phasen gingen außerdem mit stärkerer Synchronie zwischen dem Nucleus subthalamicus und einer bewegungsbezogenen Region, dem supplementären motorischen Areal, einher. Das default‑mode‑Netzwerk erzählte eine andere Geschichte: Seine Aktivierungen waren mit niedrigeren Frequenzen im Nucleus subthalamicus und mit verstärkter Synchronie bei langsameren Frequenzbändern verbunden, was auf einen funktional unterscheidbaren Zustand hindeutet, der eher mit nicht‑motorischen Aspekten der Erkrankung zu tun haben könnte.
Medikationseffekte hängen vom Gehirnzustand ab
Die Forschenden untersuchten anschließend, wie Parkinson‑Medikamente diese tiefen Rhythmen veränderten. Im Mittel reduzierte die Medikation die Beta‑Aktivität im Nucleus subthalamicus, was frühere Studien bestätigt. Betrachtet man die Ergebnisse jedoch im Kontext der großräumigen Netzwerke, zeichnet sich ein nuancierteres Bild ab. Die stärksten medikationsbedingten Reduktionen der Beta‑Leistung traten während Netzwerkzuständen auf, die keine besonders starke Kopplung zwischen Nucleus subthalamicus und motorischen Arealen zeigten. Im Gegensatz dazu waren die sensorimotorischen und default‑mode‑Netzwerke — in denen tiefe und oberflächliche Areale am engsten kommunizierten — weniger deutlich beeinflusst. Ein unabhängiger Datensatz einer anderen Forschungsgruppe bestätigte weitgehend den Kernbefund, dass bestimmte Netzwerke mit jeweils charakteristischen Mustern tiefer Hirnrhythmen verknüpft sind, auch wenn dort die Medikamenteneffekte schwächer ausfielen.
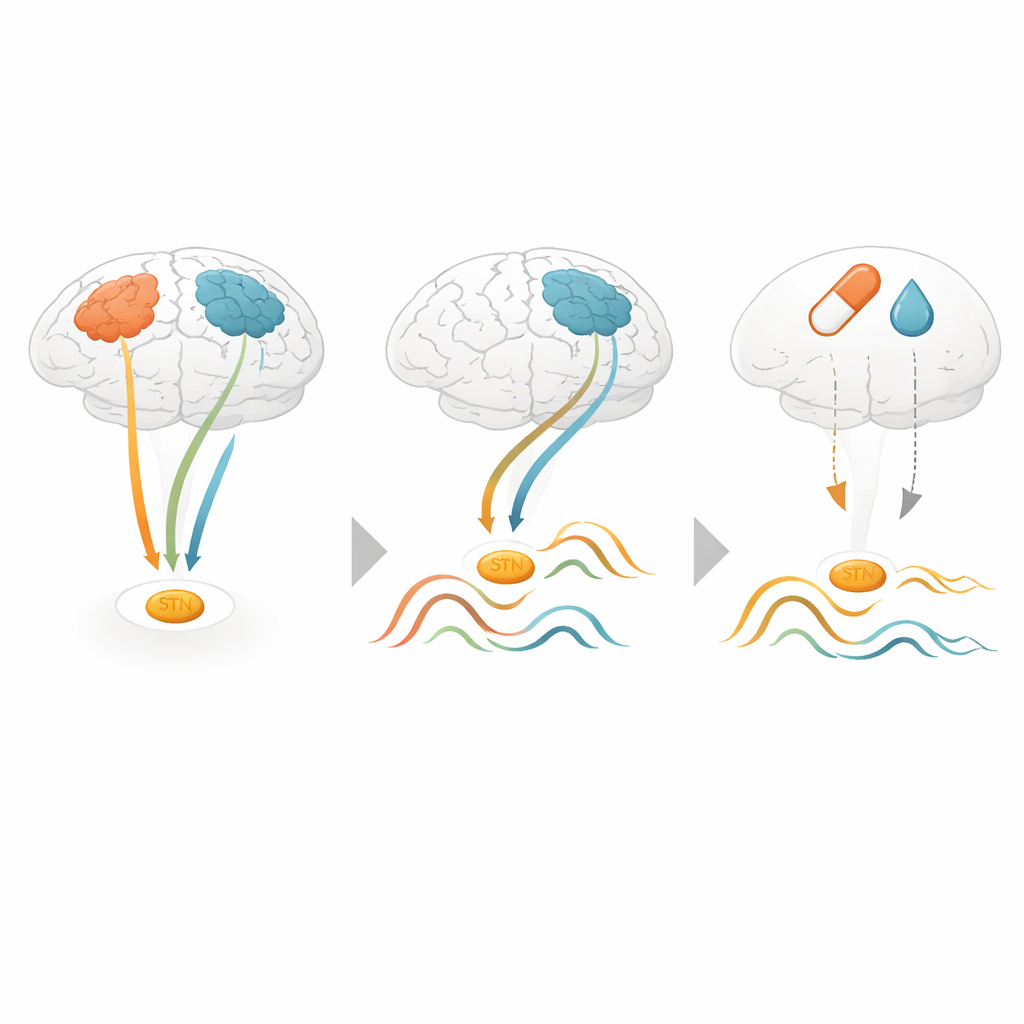
Was das für künftige Behandlungen bedeutet
Für eine nichtfachliche Leserschaft lautet die wichtigste Botschaft: Das Gehirn verharrt nicht in einem einzigen, konstanten Parkinson‑Zustand. Stattdessen wechselt es zwischen verschiedenen großräumigen Mustern, und jedes Muster korrespondiert mit einer bestimmten „Stimmung“ der tiefen Struktur, die Ziel von Operationen und Medikamenten ist. Da sich diese Muster nichtinvasiv von der Hirnoberfläche aus erkennen lassen, könnten sie künftig als externe Marker dienen, um Diagnosen zu unterstützen, den Krankheitsverlauf zu überwachen oder adaptive tiefe Hirnstimulation nur dann auszulösen, wenn schädliche Rhythmen auftreten. So könnte das Lesen der Sprache der Gehirnnetzwerke neue Einblicke in die verborgenen Abläufe von Parkinson eröffnen und Klinikern helfen, Behandlungen besser auf die momentanen Bedürfnisse des Gehirns abzustimmen.
Zitation: Kohl, O., Gohil, C., Sure, M. et al. Varying patterns of association between cortical large-scale networks and subthalamic nucleus activity in Parkinson’s disease. npj Parkinsons Dis. 12, 106 (2026). https://doi.org/10.1038/s41531-026-01372-1
Schlüsselwörter: Morbus Parkinson, Gehirnnetzwerke, tiefe Hirnstimulation, Beta‑Rhythmen, Magnetoenzephalographie