Clear Sky Science · fr
Variations des schémas d’association entre les réseaux corticaux à grande échelle et l’activité du noyau sous-thalamique dans la maladie de Parkinson
Pourquoi cette étude cérébrale importe
La maladie de Parkinson est surtout connue pour ses tremblements et la lenteur des mouvements, mais derrière ces symptômes se cache un problème de communication défaillante dans le cerveau. Les médecins peuvent déjà « écouter » l’activité cérébrale profonde pendant une chirurgie, mais ils préféreraient lire ces signaux de l’extérieur, en utilisant des méthodes non invasives comme les examens cérébraux. Cette étude pose une question simple mais puissante : les motifs d’activité mesurés à la surface du cerveau peuvent-ils révéler ce qui se passe profondément à l’intérieur d’une petite zone appelée noyau sous-thalamique, qui joue un rôle central dans la maladie de Parkinson ?
Observer ensemble signaux profonds et de surface
Les chercheurs ont enregistré l’activité cérébrale de 27 personnes atteintes de la maladie de Parkinson qui venaient de recevoir des électrodes de stimulation cérébrale profonde. Pendant que les patients étaient assis tranquillement, les yeux ouverts, l’équipe a mesuré simultanément deux types de signaux : la magnétoencéphalographie (MEG), qui détecte l’activité rapide de la surface corticale, et les potentiels de champ local enregistrés dans le noyau sous-thalamique profond. Chaque personne a été testée après l’arrêt de son traitement antiparkinsonien et de nouveau après avoir pris sa dose habituelle d’un médicament à action rapide. Ce protocole a permis à l’équipe d’observer comment les schémas de communication cérébrale changeaient avec et sans médicament.
Réseaux cachés qui vacillent
Plutôt que de considérer la surface cérébrale comme une zone uniforme, les scientifiques ont utilisé une méthode mathématique appelée modèle de Markov caché pour mettre au jour des réseaux de régions qui ont tendance à s’activer ensemble pendant de courts instants. Ces réseaux, cartographiés auparavant chez des sujets sains, incluent un réseau « sensori-moteur » impliqué dans le mouvement et un réseau de « mode par défaut » lié à l’activité mentale tournée vers l’intérieur. En parcourant les enregistrements milliseconde par milliseconde, le modèle a identifié quand chaque réseau était le plus actif et combien de temps le cerveau de chaque personne passait dans ces différents motifs.
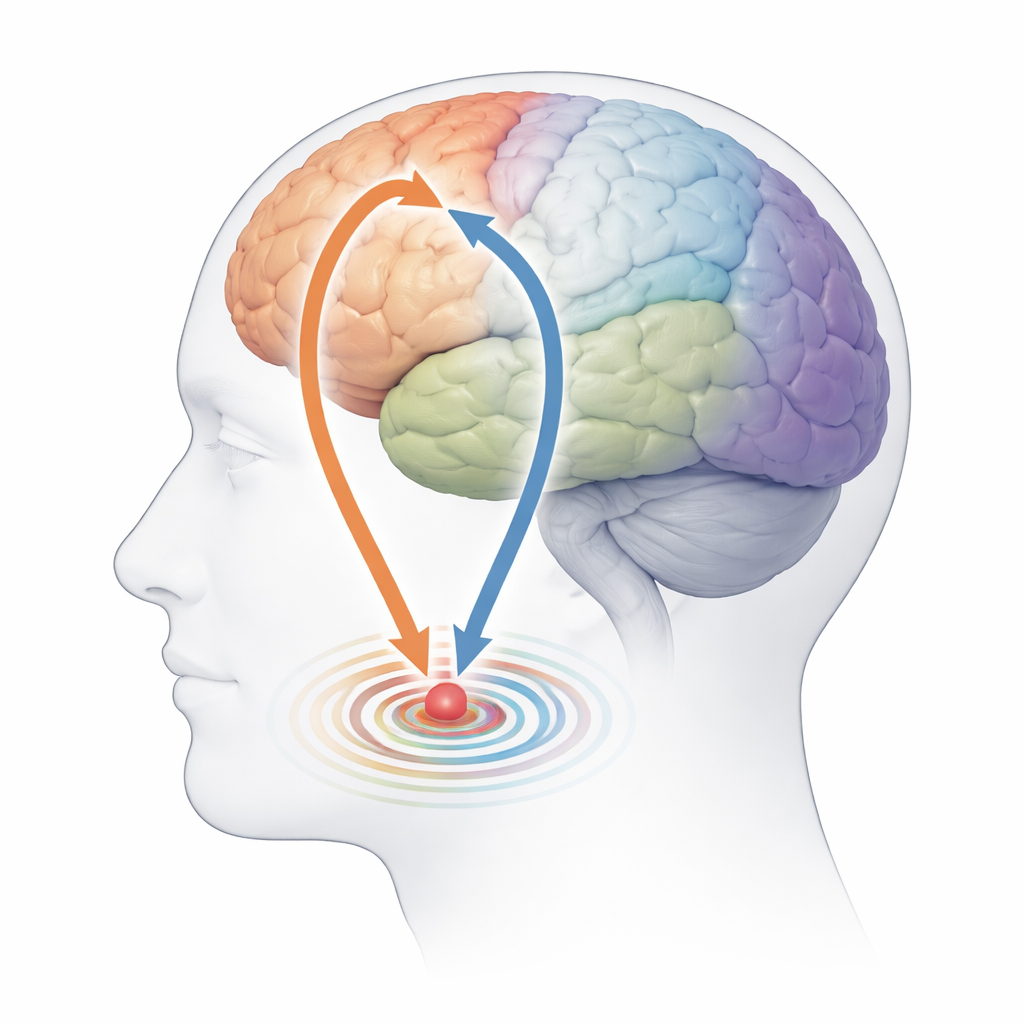
Rythmes profonds associés à des réseaux spécifiques
Quand l’équipe a comparé ces éclats de réseau à l’activité du noyau sous-thalamique, des liens clairs sont apparus. Lors des activations du réseau sensori-moteur, le noyau sous-thalamique présentait une activité rythmique plus forte dans la bande bêta, une fréquence déjà connue pour être exagérée dans la maladie de Parkinson et associée à de brefs « éclats bêta ». Ces périodes montraient également une synchronie plus serrée entre le noyau sous-thalamique et une région liée au mouvement appelée aire motrice supplémentaire. Le réseau de mode par défaut racontait une histoire différente : ses activations coïncidaient avec des rythmes de plus basse fréquence dans le noyau sous-thalamique et une synchronie accrue à des vitesses plus lentes, suggérant un état fonctionnel distinct qui pourrait être davantage lié aux aspects non moteurs de la maladie.
Les effets du médicament dépendent de l’état cérébral
Les chercheurs ont ensuite examiné comment le traitement antiparkinsonien modifiait ces rythmes profonds. En moyenne, le médicament réduisait l’activité bêta dans le noyau sous-thalamique, en accord avec des études antérieures. Mais en observant à travers le prisme des réseaux à grande échelle, un tableau plus nuancé est apparu. Les réductions de puissance bêta liées au médicament étaient les plus marquées durant des états de réseau qui ne montraient pas un couplage particulièrement fort entre le noyau sous-thalamique et les zones motrices. En revanche, les réseaux sensori-moteur et de mode par défaut, où les zones profondes et de surface communiquaient le plus étroitement, étaient moins clairement affectés. Un jeu de données indépendant d’un autre groupe de recherche a largement confirmé la conclusion principale selon laquelle des réseaux particuliers sont liés à des motifs rythmiques profonds distincts, même si les effets du médicament y étaient plus faibles.
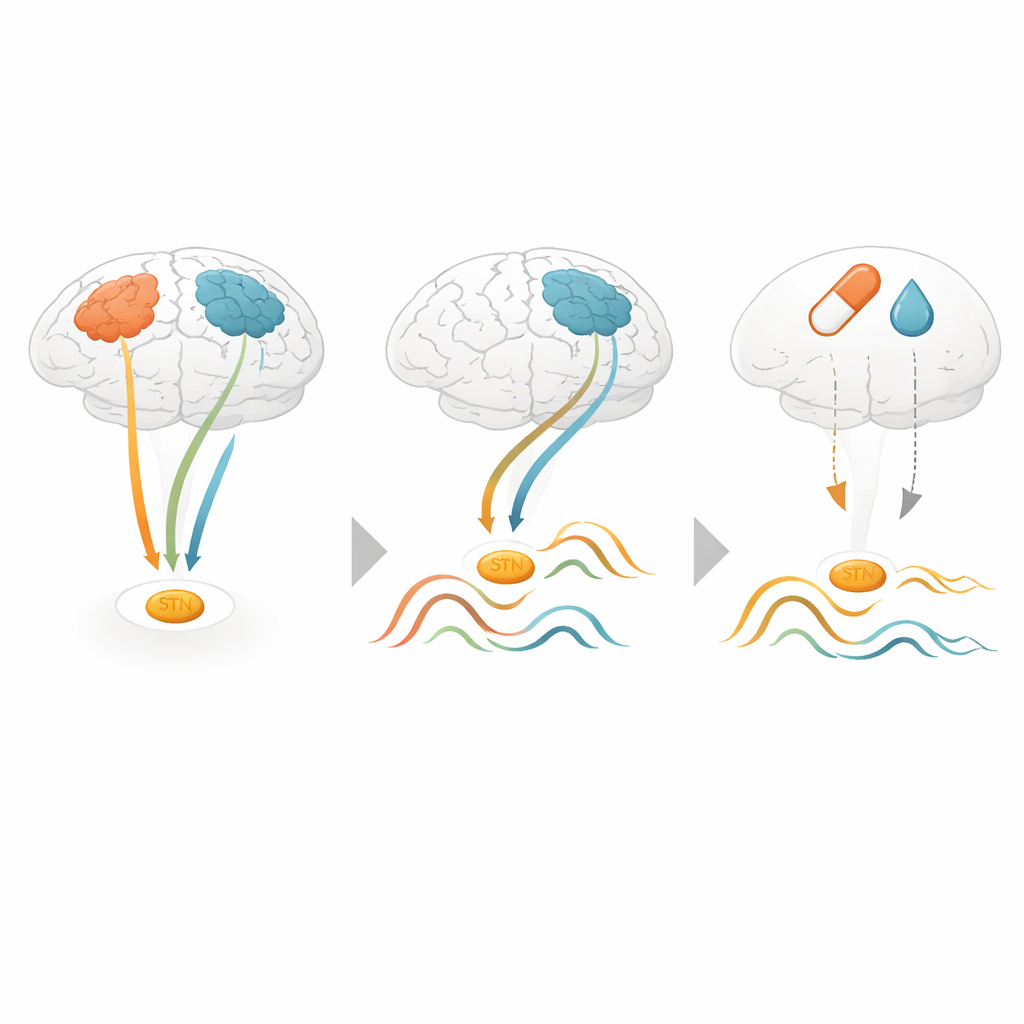
Ce que cela signifie pour les traitements futurs
Pour le lecteur non spécialiste, le message clé est que le cerveau n’est pas dans un état parkinsonien constant. Il bascule entre différents schémas à grande échelle, et chaque schéma correspond à un « état » particulier de la structure profonde ciblée par la chirurgie et les médicaments. Parce que ces schémas peuvent être détectés de manière non invasive à partir de la surface cérébrale, ils pourraient à terme servir de marqueurs externes pour guider le diagnostic, surveiller la progression de la maladie ou déclencher une stimulation cérébrale profonde adaptative uniquement lorsque des rythmes nocifs apparaissent. Ainsi, lire le langage des réseaux cérébraux pourrait ouvrir de nouvelles fenêtres sur les mécanismes cachés de la maladie de Parkinson et aider les cliniciens à adapter les traitements aux besoins du cerveau au fil du moment.
Citation: Kohl, O., Gohil, C., Sure, M. et al. Varying patterns of association between cortical large-scale networks and subthalamic nucleus activity in Parkinson’s disease. npj Parkinsons Dis. 12, 106 (2026). https://doi.org/10.1038/s41531-026-01372-1
Mots-clés: Maladie de Parkinson, réseaux cérébraux, stimulation cérébrale profonde, rythmes bêta, magnetoencéphalographie