Clear Sky Science · nl
Bondige synthese van bufogargarizin B via een conformatie-gecontroleerde skelet-herschikkingsaanpak
Waarom chemici geven om paddergif
Paddergiffen worden al lang in de traditionele geneeskunde gebruikt voor hart- en kanker-gerelateerde aandoeningen, maar veel van de actieve moleculen zijn zeldzaam en structureel complex. Dit artikel beschrijft een gestroomlijnde manier om een van die moleculen, bufogargarizin B, in het laboratorium op te bouwen uit een goedkoop uitgangsmateriaal, wat de deur opent naar beter onderzoek naar de biologische effecten en naar nieuwe chemie voor het vormen van steroid-frames.
Een zeldzaam steroid met een gedraaid rugbeen
Bufogargarizin B behoort tot een familie van steroid-achtige verbindingen genaamd bufadienoliden, aangetroffen in planten en dieren en bijzonder rijk aanwezig in sommige padden die in de Chinese geneeskunde worden gebruikt. In tegenstelling tot typische steroïden, die een regelmatig vier-ring "6/6/6/5"-skelet hebben, dragen bufogargarizinen een herschikt "5/7/6/5"-ringpatroon en een sterk gedecoreerde eindring. Van deze ongewone vormen wordt gedacht dat ze beïnvloeden hoe de moleculen met biologische doelen interageren, maar hun schaarste in de natuur en structurele complexiteit hebben het moeilijk gemaakt ze te bestuderen.
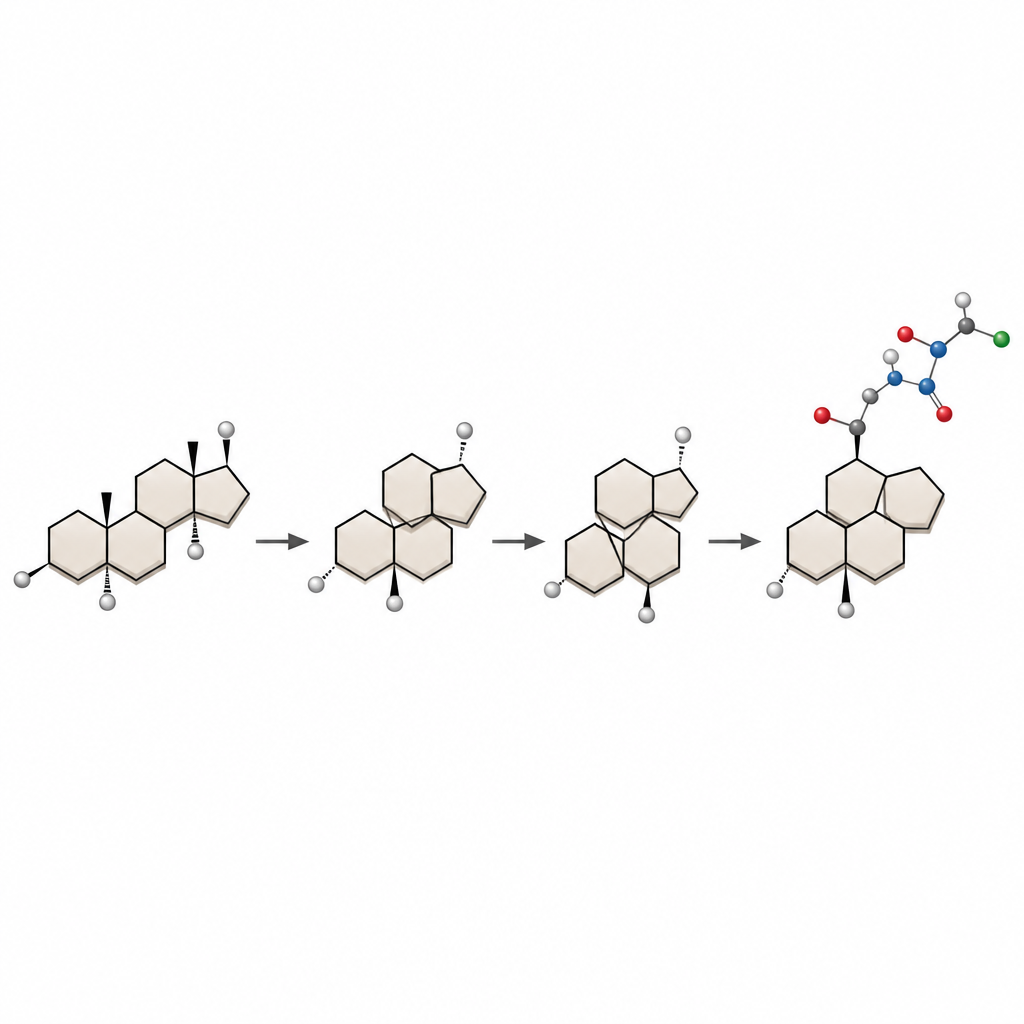
Het steroidframework van binnenuit herbouwen
De auteurs beginnen met dehydroepiandrosteron, een goedkoop en gemakkelijk verkrijgbaar steroid, en herontwerpen het kernskelet. Ze zetten eerst een deel van het starre steroid om in een flexibele tienring. Vervolgens brengen ze met een samarium-gebaseerd reagens een transannulaire reactie op gang, waarbij twee verre punten over de ring verbinden om een nieuw gefuseerd systeem te vormen. Door zorgvuldig te sturen hoe deze ring in drie dimensies vouwt en de plaatsing van een sleutel koolstof–koolstof dubbelsubstitutie, leiden ze de reactie naar het gewenste 5/7/6/5-kernskelet van bufogargarizin B met de correcte driedimensionale oriëntering van atomen.
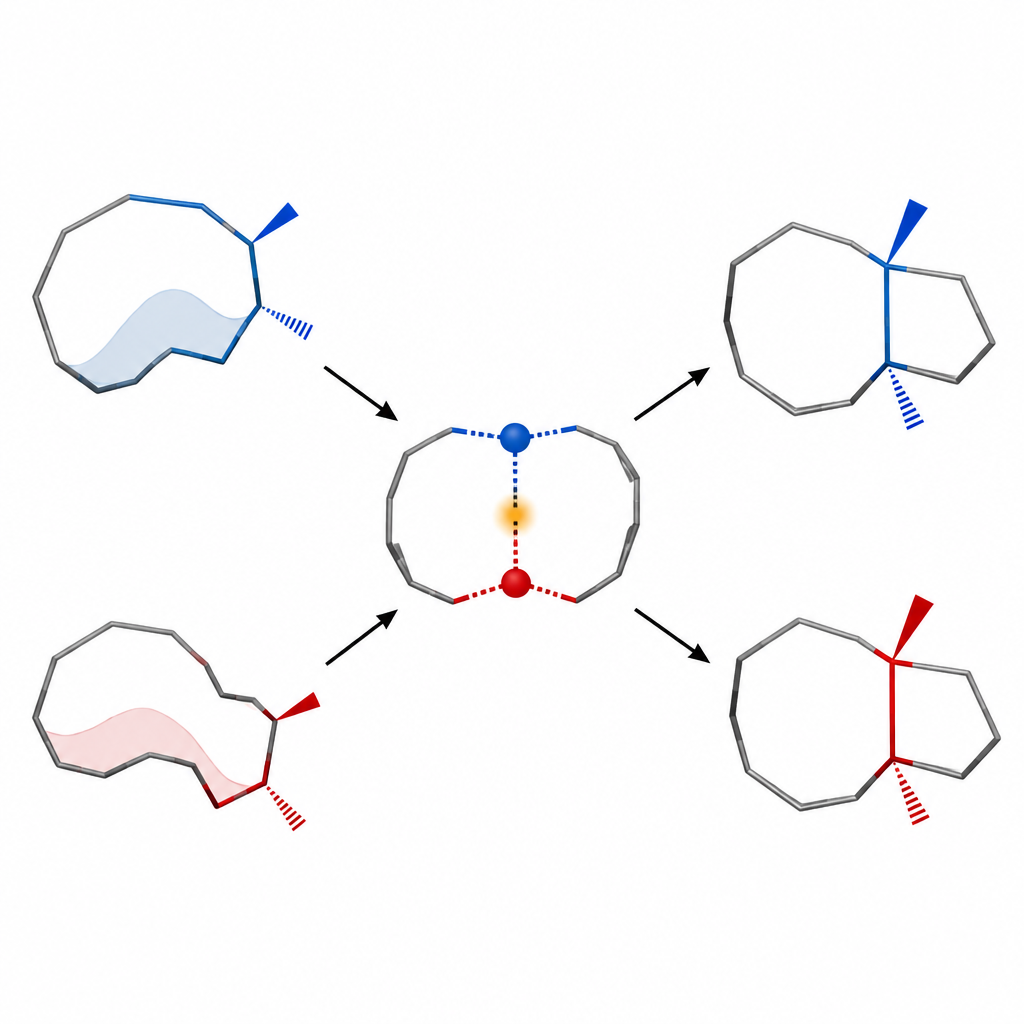
Moleculaire houding beheersen om de uitkomst te kiezen
Een centraal thema van het werk is conformationele controle: het idee dat de manier waarop een molecuul buigt en draait kan bepalen welk product een reactie oplevert. Het team toont aan dat hun tienring verschillende vormen kan aannemen, en dat elke vorm de neiging heeft naar een ander gefuseerd-ringproduct te leiden. Door condities zoals temperatuur en substituenten te tunen, verrijken ze de conformatie die de juiste combinatie van naburige stereocentra in het uiteindelijke skelet levert. Deze aanpak contrasteert met meer traditionele reacties die bij dergelijke mediumgrote ringen vaak rommelige mengsels van stereoisomeren geven.
De sterk gedecoreerde zijring opbouwen
Als het kernskelet op zijn plaats ligt, moeten de onderzoekers nog de dicht functionalisierte eindring aanbrengen die een α-pyroon zijsegment draagt dat kenmerkend is voor bufadienoliden. Ze ontwikkelen een praktische synthese op gram-schaal van een klein bouwblok, 2-pyroon-5-boranaat, uit het eenvoudige chemische furfurylalcohol. Met dit fragment in een cross-coupling reactie, gevolgd door een reeks zorgvuldig gekozen oxidatie- en reductiestappen, construeren ze de volledig cis-georiënteerde "D"-ring van bufogargarizin B, inclusief de meerdere zuurstofhoudende groepen, zonder de rest van het molecuul te verstoren.
De auteurs onderzoeken ook een biomimetische reactie die verschillende gefuseerde ringlay-outs onderling omzet, vergelijkbaar met wat in de natuur kan gebeuren. Ze ontwerpen intermediairen die een retro-aldolstap kunnen ondergaan waarbij een koolstof–koolstofbinding breekt, gevolgd door een transannulaire aldolreactie die een andere verbinding over de ring herstelt. Deze cascade maakt toegang mogelijk tot zowel 5/7/6/5- als 7/5/6/5-kernskeletten en ondersteunt de voorgestelde relatie tussen bufogargarizin B en zijn naaste verwant bufogargarizin A. Onderweg brengen ze in kaart welke stereochemische arrangementen de voorkeur krijgen, wat opnieuw benadrukt hoe moleculaire conformatie bepaalt welke structuren thermodynamisch het meest gunstig zijn.
Wat dit betekent voor toekomstige moleculen
Uiteindelijk realiseert het team een 18-stappen synthese van bufogargarizin B uit een veelvoorkomend steroid en schetsen ze een route naar het kernskelet van bufogargarizin A. Voor niet-specialisten is de kernboodschap dat ze hebben geleerd een flexibele ring zodanig te "poseren" dat één goed gedefinieerd product ontstaat in plaats van een verwarrend mengsel. Deze strategie van conformationeel-gecontroleerde skelet-herschikking, gecombineerd met een praktische route naar het 2-pyroon bouwblok, zal nuttig zijn voor het maken van andere zeldzame uit padden en planten afgeleide bufadienoliden, en zo meer rigoureuze studies naar hun biologische rollen en potentiële therapeutische waarde mogelijk maken.
Bronvermelding: Yang, P., Shen, Y. & Gui, J. Concise synthesis of bufogargarizin B by a conformation-controlled skeletal reorganization approach. Nat Commun 17, 4156 (2026). https://doi.org/10.1038/s41467-026-70735-2
Trefwoorden: bufogargarizin B, steroïdensynthese, conformationele controle, bufadienoliden, transannulaire cyclisatie