Clear Sky Science · de
Kurzgefasste Synthese von Bufogargarizin B durch einen konformationskontrollierten Skelett‑Reorganisationsansatz
Warum Chemiker sich für Kröten‑Gifte interessieren
Krötengifte werden in der traditionellen Medizin seit langem bei Herz‑ und Krebserkrankungen eingesetzt, doch viele der wirksamen Moleküle sind selten und strukturell komplex. Dieser Artikel beschreibt einen gestrafften Weg, ein solches Molekül, Bufogargarizin B, im Labor aus einem preiswerten Ausgangsstoff herzustellen, was bessere Untersuchungen seiner biologischen Effekte und neue Methoden zur Formung von Steroidgerüsten ermöglicht.
Ein seltenes Steroid mit verdrehtem Rückgrat
Bufogargarizin B gehört zu einer Familie steroidähnlicher Verbindungen, den Bufadienoliden, die in Pflanzen und Tieren vorkommen und besonders in einigen für die chinesische Medizin genutzten Kröten reichlich vertreten sind. Anders als typische Steroide mit dem regelmäßigen vierringigen „6/6/6/5“‑Gerüst weisen Bufogargarizine ein umgebautes „5/7/6/5“‑Ringmuster und einen stark substituierten Endring auf. Diese ungewöhnlichen Formen dürften beeinflussen, wie die Moleküle mit biologischen Zielstrukturen interagieren, doch ihre Seltenheit in der Natur und die strukturelle Komplexität erschweren Untersuchungen.
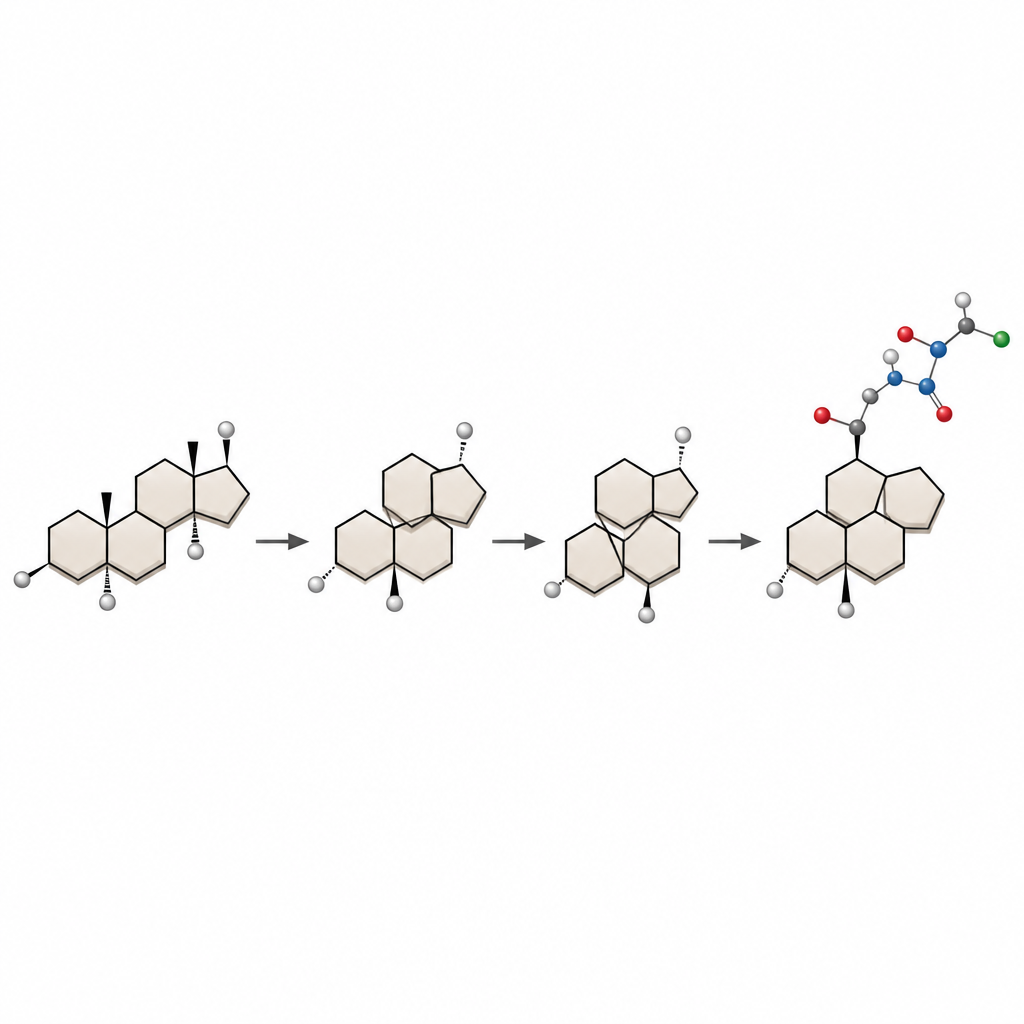
Das Steroidgerüst von innen neu aufbauen
Die Autoren starten von Dehydroepiandrosteron, einem günstigen und leicht verfügbaren Steroid, und entwerfen seinen Kern um. Zunächst wandeln sie einen Teil des starren Steroids in einen flexiblen zehngliedrigen Ring um. Anschließend lösen sie mit einem samariumbasierten Reagens eine transannuläre Reaktion aus, bei der zwei weit auseinanderliegende Stellen des Rings miteinander verbinden und ein neues verschmolzenes System bilden. Durch sorgfältige Kontrolle der dreidimensionalen Ringfaltung und der Lage einer schlüsselnden Kohlenstoff‑Kohlenstoff‑Doppelbindung lenken sie die Reaktion so, dass das gewünschte 5/7/6/5‑Gerüst von Bufogargarizin B mit der korrekten räumlichen Orientierung der Atome entsteht.
Die Molekülhaltung steuern, um das Ergebnis zu wählen
Ein zentrales Thema der Arbeit ist die Konformationskontrolle: die Idee, dass Biegen und Verdrehen eines Moleküls bestimmen kann, welches Produkt eine Reaktion liefert. Das Team zeigt, dass ihr zehngliedriger Ring verschiedene Formen einnehmen kann und dass jede Form dazu neigt, zu einem anderen verschmolzenen Ringresultat zu führen. Durch Variieren von Bedingungen wie Temperatur und Substituenten erhöhen sie die Anteile der Konformation, die das korrekte Paar benachbarter Stereozentren im Endgerüst liefert. Dieser Ansatz steht im Gegensatz zu traditionelleren Reaktionen, die bei der Anwendung auf mittelgroße Ringe oft unübersichtliche Gemische von Stereoisomeren erzeugen.
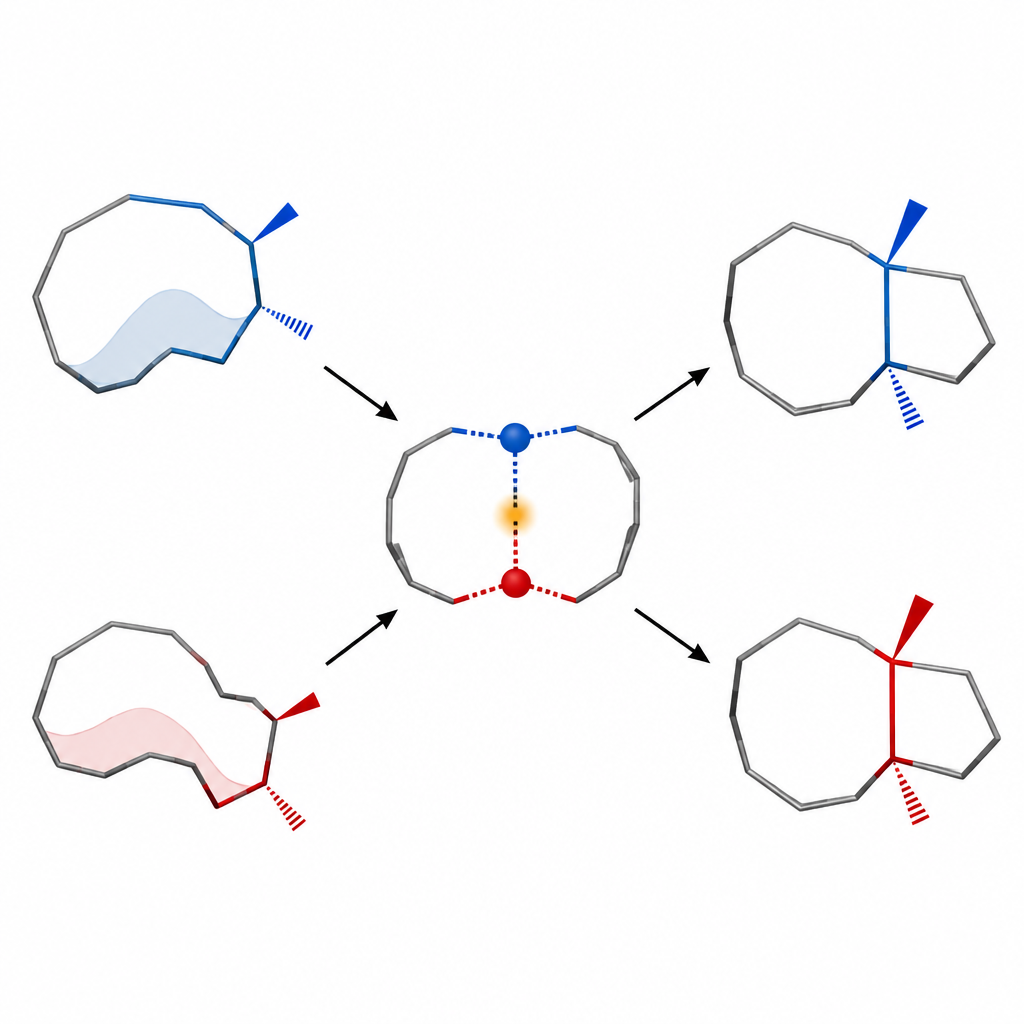
Den stark substituierten Seitenring aufbauen
Sobald das Kerngerüst steht, müssen die Forscher noch den dicht funktionalisierten Endring einführen, der ein α‑Pyrone‑Fragment trägt, das für Bufadienolide charakteristisch ist. Sie entwickeln eine praxisnahe, gramstufige Synthese eines kleinen Bausteins, des 2‑Pyrone‑5‑Boronats, aus dem einfachen Ausgangsstoff Furfurylalkohol. Mit diesem Fragment in einer Kupplungsreaktion, gefolgt von einer Abfolge sorgfältig gewählter Oxidations‑ und Reduktionsschritte, konstruieren sie den vollständig cis‑konfigurierten „D“‑Ring von Bufogargarizin B inklusive seiner mehreren Sauerstoff‑Funktionalitäten, ohne den Rest des Moleküls zu stören.
Zwischen verwandten Ringsystemen umschalten
Die Autoren untersuchen zudem eine biomimetische Reaktion, die unterschiedliche verschmolzene Ringanordnungen ineinander überführt, ähnlich dem, was in der Natur geschehen könnte. Sie entwerfen Zwischenprodukte, die eine retro‑Aldol‑Stufe durchlaufen können, bei der eine C–C‑Bindung gespalten wird, gefolgt von einer transannulären Aldol‑Reaktion, die eine andere Verbindung quer über den Ring wieder ausbildet. Diese Kaskade ermöglicht den Zugang sowohl zu 5/7/6/5‑ als auch zu 7/5/6/5‑Kerngerüsten und stützt die vorgeschlagene Beziehung zwischen Bufogargarizin B und seinem nahen Verwandten Bufogargarizin A. Dabei kartieren sie, welche stereochemischen Anordnungen bevorzugt werden, und unterstreichen erneut, wie die Molekülkonformation bestimmt, welche Strukturen thermodynamisch günstiger sind.
Was das für künftige Moleküle bedeutet
Am Ende erreichen die Forscher eine 18‑stufige Synthese von Bufogargarizin B aus einem gängigen Steroid und skizzieren einen Weg zum Kern von Bufogargarizin A. Für den Nicht‑Spezialisten lautet die Kernbotschaft, dass sie gelernt haben, einen flexiblen Ring gezielt „zu posieren“, sodass ein einzelnes, gut definiertes Produkt entsteht statt eines verwirrenden Gemischs. Diese Strategie der konformationskontrollierten Skelett‑Reorganisation, kombiniert mit einem praktischen Zugang zum 2‑Pyrone‑Baustein, sollte nützlich sein, um andere seltene, aus Kröten oder Pflanzen stammende Bufadienolide herzustellen und so genauere Studien ihrer biologischen Rollen und ihres therapeutischen Potenzials zu ermöglichen.
Zitation: Yang, P., Shen, Y. & Gui, J. Concise synthesis of bufogargarizin B by a conformation-controlled skeletal reorganization approach. Nat Commun 17, 4156 (2026). https://doi.org/10.1038/s41467-026-70735-2
Schlüsselwörter: bufogargarizin B, Steroidsynthese, Konformationskontrolle, Bufadienolide, transannuläre Cyclisierung