Clear Sky Science · fr
Synthèse concise du bufogargarizin B par une réorganisation squelettique contrôlée par conformation
Pourquoi les chimistes s’intéressent au venin de crapaud
Les venins de crapaud sont depuis longtemps employés en médecine traditionnelle pour des affections cardiaques et liées au cancer, mais nombre de molécules actives y sont rares et structurellement complexes. Cet article décrit une manière épurée de construire en laboratoire l’une de ces molécules, le bufogargarizin B, à partir d’un matériau de départ peu coûteux, ouvrant la voie à de meilleures études de ses effets biologiques et à de nouvelles méthodes pour façonner les squelettes stéroïdiens.
Un stéroïde rare au squelette tordu
Le bufogargarizin B appartient à une famille de composés de type stéroïde appelés bufadiénolides, présents dans des plantes et des animaux et particulièrement abondants chez certains crapauds utilisés en médecine chinoise. Contrairement aux stéroïdes typiques, qui possèdent un squelette régulier à quatre cycles « 6/6/6/5 », les bufogargarizins présentent un motif de cycles réarrangés « 5/7/6/5 » et un dernier cycle fortement substitué. Ces formes inhabituelles influencent probablement la façon dont les molécules interagissent avec des cibles biologiques, mais leur rareté dans la nature et leur complexité structurelle ont rendu leur étude difficile.
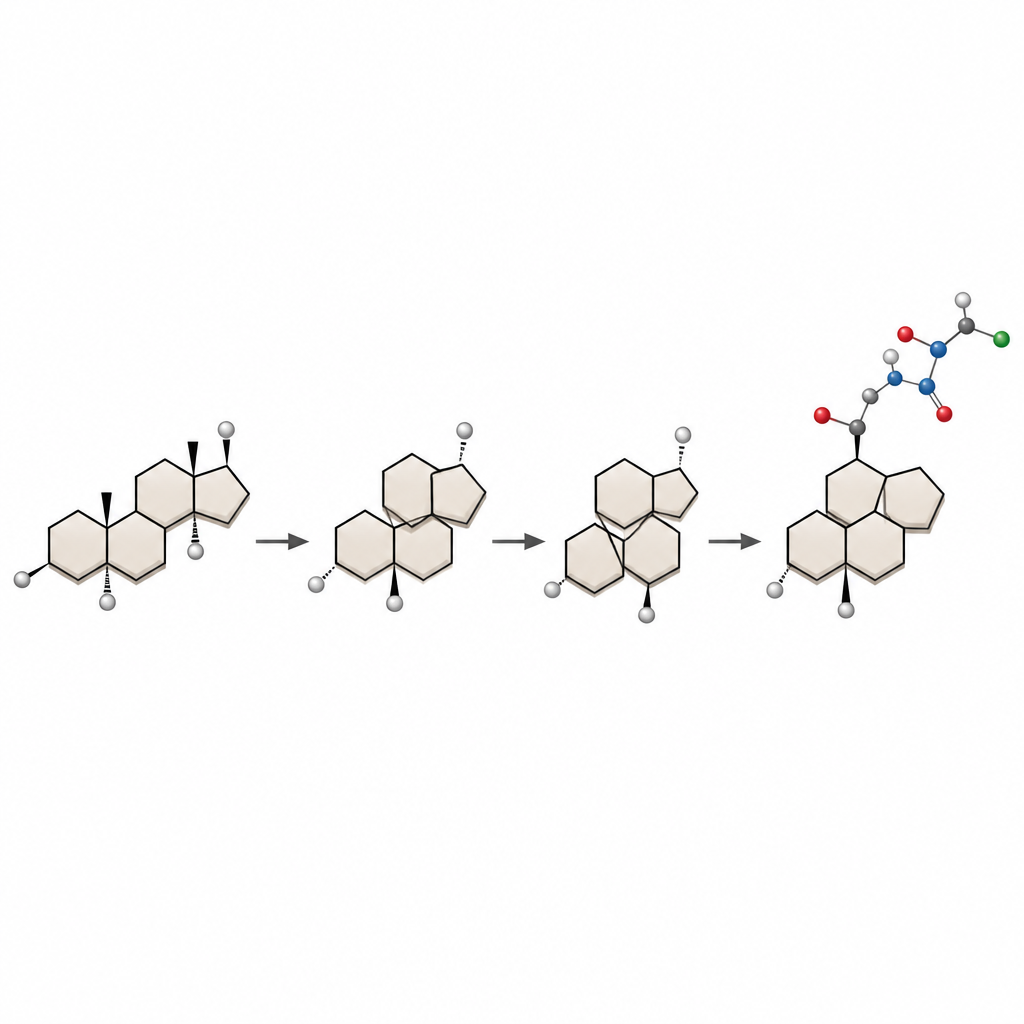
Reconstruire le cadre stéroïdien de l’intérieur
Les auteurs partent de la déhydroépiandrostérone, un stéroïde bon marché et facilement disponible, et repensent son cœur. Ils convertissent d’abord une partie du stéroïde rigide en un cycle flexible à dix atomes. Ensuite, en utilisant un réactif à base de samarium, ils déclenchent une réaction transannulaire, où deux points éloignés à travers le cycle se connectent pour former un nouveau système fusionné. En contrôlant soigneusement la façon dont ce cycle se replie en trois dimensions et la disposition d’une double liaison carbone–carbone clé, ils orientent la réaction pour obtenir le noyau 5/7/6/5 souhaité du bufogargarizin B avec l’orientation tridimensionnelle correcte des atomes.
Contrôler la « posture » moléculaire pour choisir le résultat
Un thème central du travail est le contrôle conformationnel : l’idée que la façon dont une molécule se plie et se tord peut dicter le produit d’une réaction. L’équipe montre que leur cycle à dix atomes peut adopter différentes formes, et que chaque forme tend à conduire à un résultat de cycles fusionnés distinct. En ajustant des conditions telles que la température et les substituants, ils favorisent la conformation qui fournit la paire correcte de stéréocentres voisins dans le cadre final. Cette approche contraste avec des réactions plus traditionnelles qui donnent souvent des mélanges confus de stéréoisomères sur de tels cycles de taille moyenne.
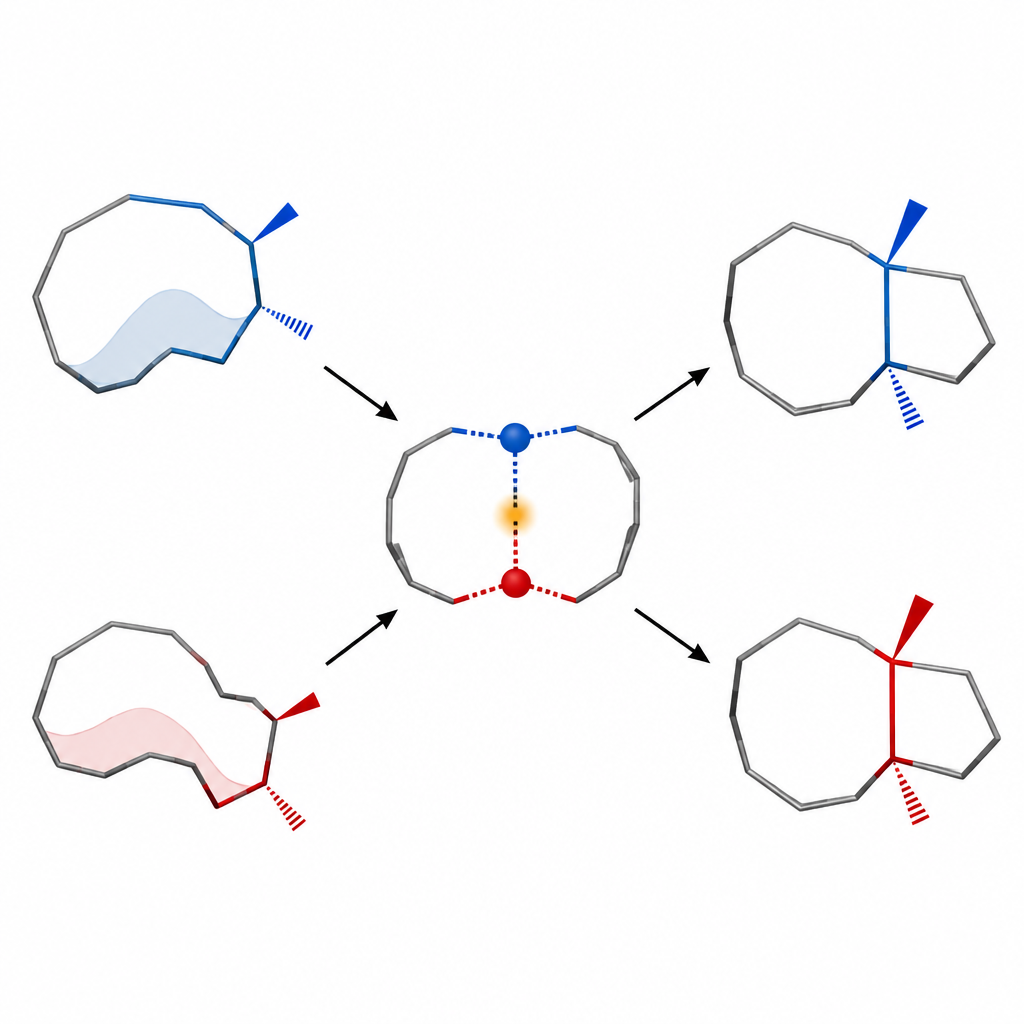
Construire le cycle latéral fortement substitué
Une fois le cadre principal en place, les chercheurs doivent encore installer le cycle final densément fonctionnalisé qui porte un segment α-pyrone caractéristique des bufadiénolides. Ils développent une synthèse pratique à l’échelle gramme d’un petit bloc de construction appelé 2-pyrone-5-boronate à partir de l’alcool furfuryle simple. En utilisant ce fragment dans une réaction de couplage croisé, suivie d’une séquence d’oxydations et de réductions judicieusement choisies, ils construisent le cycle « D » entièrement cis du bufogargarizin B, y compris ses multiples groupes oxygénés, sans perturber le reste de la molécule.
Basculer entre systèmes de cycles apparentés
Les auteurs explorent également une réaction biomimétique qui interconvertit différents agencements de cycles fusionnés, similaire à ce qui peut se produire en nature. Ils conçoivent des intermédiaires susceptibles de subir une étape rétro-aldol, rompant une liaison carbone–carbone, suivie d’une aldol transannulaire qui reforme une connexion différente à travers le cycle. Cette cascade permet d’accéder à la fois aux squelettes centraux 5/7/6/5 et 7/5/6/5 et soutient la relation proposée entre le bufogargarizin B et son proche parent bufogargarizin A. En chemin, ils cartographient quelles dispositions stéréochimiques sont favorisées, soulignant à nouveau comment la conformation moléculaire guide les structures thermodynamiquement préférées.
Ce que cela signifie pour les molécules à venir
Au final, l’équipe réalise une synthèse en 18 étapes du bufogargarizin B à partir d’un stéroïde courant et décrit une voie vers le noyau du bufogargarizin A. Pour un non-spécialiste, le message clé est qu’ils ont appris à « poser » un cycle flexible de sorte qu’un produit unique et bien défini se forme, plutôt qu’un mélange confus. Cette stratégie de réorganisation squelettique contrôlée par conformation, combinée à une voie pratique vers le bloc 2-pyrone, devrait être utile pour préparer d’autres bufadiénolides rares d’origine crapaud ou végétale, permettant des études plus rigoureuses de leurs rôles biologiques et de leur valeur thérapeutique potentielle.
Citation: Yang, P., Shen, Y. & Gui, J. Concise synthesis of bufogargarizin B by a conformation-controlled skeletal reorganization approach. Nat Commun 17, 4156 (2026). https://doi.org/10.1038/s41467-026-70735-2
Mots-clés: bufogargarizin B, synthèse de stéroïdes, contrôle conformationnel, bufadiénolides, cyclisation transannulaire