Clear Sky Science · nl
RRx-001 remt G6PD om NADPH uit te putten en disulfidptosis te veroorzaken gekoppeld aan DAMP-gemedieerde immunogene celdood bij hepatocellulair carcinoom
Waarom deze studie belangrijk is voor leverkanker
Primaire leverkanker, met name hepatocellulair carcinoom, blijft een van de dodelijkste vormen van kanker wereldwijd, waarbij de meeste patiënten te laat worden gediagnosticeerd voor curatieve chirurgie. Deze studie onderzoekt of een experimenteel geneesmiddel in klinische fase, RRx-001, levertumoren op een ongebruikelijk slimme manier kan aanvallen: door een belangrijke bron van cellulaire bbatterijkracht�bb af te snijden en tegelijkertijd stervende kankercellen te veranderen in een vaccinachtige prikkel die het immuunsysteem activeert.
Een nieuwe manier waarop kankercellen sterven
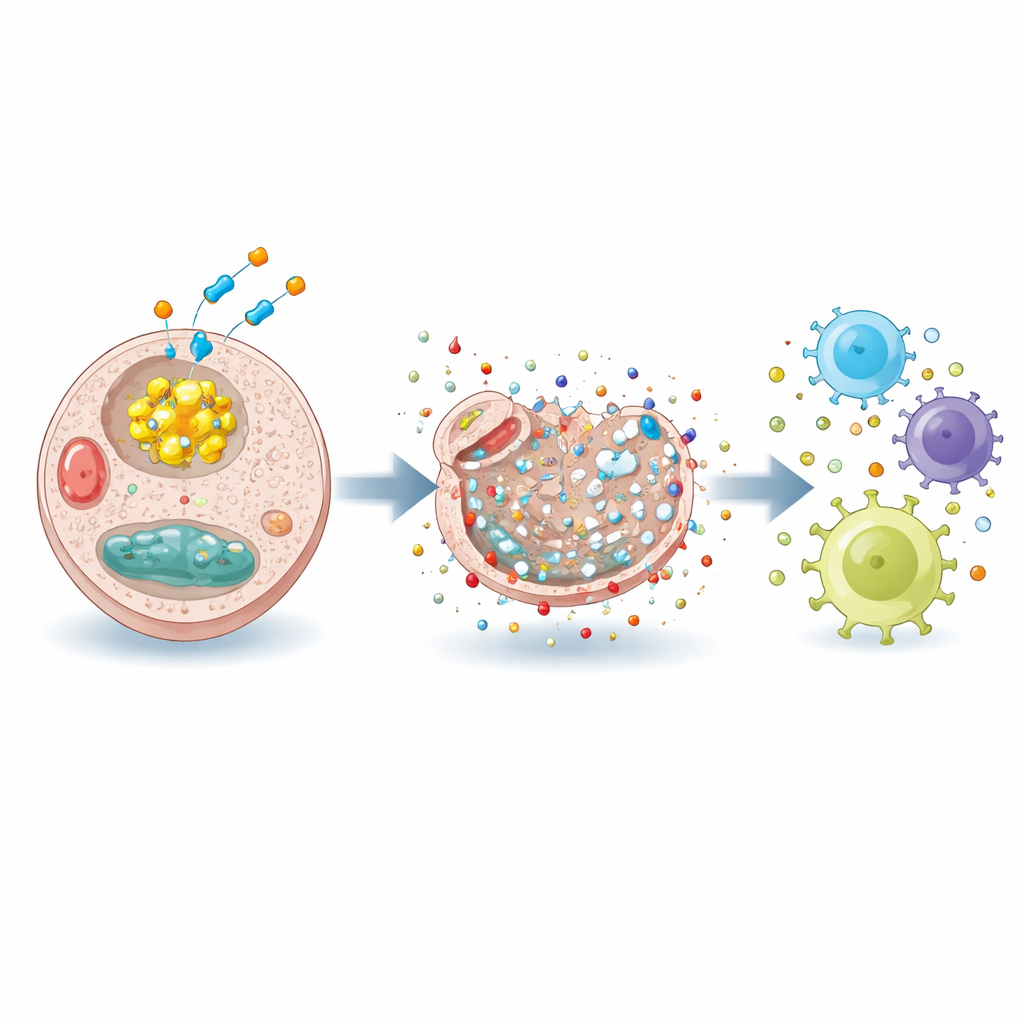
Wetenschappers zien kankerbehandeling steeds meer als het beheersen van hoe tumorcellen leven en sterven. Naast bekende vormen van celdood zoals apoptose, hebben onderzoekers recentelijk bdisulfidptosis�bb beschreven, een type geprogrammeerde celdood dat optreedt wanneer cellen niet langer bepaalde chemische bindingen, disulfiden genaamd, in hun interne skelet kunnen beheren. Wanneer dit evenwicht instort, trekt het geraamte dat cellen hun vorm geeft zich samen en valt uiteen, wat leidt tot snelle celdood. De belofte van disulfidptosis is dat het een kwetsbaarheid benut in het veranderde metabolisme van kankercellen, wat mogelijk een selectieve tumoraanpak mogelijk maakt.
De energievoorziening van de tumor aanvallen
Kankercellen zijn sterk afhankelijk van het molecuul NADPH om hun interne chemie stabiel te houden en schadelijke reactieve deeltjes te neutraliseren. Een belangrijke bron van NADPH is de pentosefosfaatroute, gecontroleerd door een enzym genaamd G6PD. In deze studie vergeleken de onderzoekers verschillende verbindingen die meerdere NADPH-producerende routes blokkeren en vonden dat RRx-001 het krachtigst was in het doden van leverkankercellen in het laboratorium. In tegenstelling tot andere remmers kon de door RRx-001 veroorzaakte celdood gedeeltelijk worden teruggedraaid door een chemische stof die specifiek disulfidebindingen verbreekt, en de cellen vertoonden een karakteristieke instorting van hun interne actinevezels. Deze kenmerken wezen erop dat RRx-001 disulfidptosis veroorzaakte, niet slechts algemene toxiciteit.
Van metabole ineenstorting naar immuunalarm
Door G6PD te blokkeren, onttrok RRx-001 NADPH, verstoorde het de balans tussen beschermend en geoxideerd glutathion, en liet het schadelijke reactieve zuurstof- en stikstofsoorten ophopen. Deze chemische stress duwde leverkankercellen in disulfidptosis, maar deed ook iets extra 0s: het zorgde ervoor dat de cellen zogenaamde gevaarsignalen (DAMPs) blootstelden en vrijgaven, waaronder moleculen zoals calreticuline en warmte-shock-eiwitten. Onder een elektronenmicroscoop toonden behandelde cellen beschadigde organellen en verstoorde membranen, veranderingen die overeenkomen met een vorm van celdood die het immuunsysteem kan mobiliseren in plaats van stil te verdwijnen.
Tumoren van "koud" naar baarm�hot� maken
Het team testte vervolgens RRx-001 in muismodellen met levertumoren. Tumoren die met het geneesmiddel werden behandeld, groeiden trager en wogen minder dan die in onbehandelde dieren. Gedetailleerde analyse van het tumorweefsel toonde een verhoogde infiltratie van helper- (CD4+) en cytotoxische (CD8+) T-cellen, een verschuiving van macrofagen naar een meer inflammatoir, tumorbestrijdend type, en verlaagde niveaus van PD-L1, een oppervlakteeiwit dat tumoren gebruiken om immuunaanvallen uit te schakelen. Genexpressiepatronen in de tumoren lieten activatie zien van T-celreceptor-signalerings- en T-helpercel-differentiatiewegen, allemaal aanwijzingen dat het immuunsysteem was gemobiliseerd in plaats van onderdrukt.
Wat dit kan betekenen voor toekomstige behandelingen
Samengevat suggereren de bevindingen dat RRx-001 leverkanker op twee fronten aanvalt: het benut een metabole achilleshiel door cellen van NADPH te beroven en hen in disulfidptosis te dwingen, en het verandert tegelijkertijd hun dood in een immuunstimulerende gebeurtenis die bekendstaat als immunogene celdood. Voor patiënten opent dit de mogelijkheid van behandelingen die niet alleen tumoren rechtstreeks verkleinen, maar ook het lichaam helpen kanker beter te herkennen en te bestrijden. De auteurs stellen dat RRx-001 bijzonder krachtig zou kunnen zijn in combinatie met moderne remmers van immuuncheckpoints, en zo moeilijk te behandelen �abkoude� levertumoren mogelijk kan omzetten in �abhete� tumoren die beter op immunotherapie reageren.
Bronvermelding: Huang, H., He, Y., Chen, J. et al. RRx-001 inhibits G6PD to deplete NADPH and trigger disulfidptosis coupled with DAMP-mediated immunogenic cell death in hepatocellular carcinoma. Cell Death Discov. 12, 194 (2026). https://doi.org/10.1038/s41420-026-03032-y
Trefwoorden: hepatocellulair carcinoom, kankermetabolisme, immunogene celdood, tumorimmunotherapie, RRx-001