Clear Sky Science · it
RRx-001 inibisce G6PD per esaurire NADPH e innescare la disulfidptosi associata a morte cellulare immunogenica mediata da DAMP nel carcinoma epatocellulare
Perché questo studio è importante per il cancro al fegato
Il tumore primario del fegato, in particolare il carcinoma epatocellulare, rimane uno dei tumori più letali a livello mondiale, con la maggior parte dei pazienti diagnosticati troppo tardi per un intervento chirurgico risolutivo. Questo studio esplora se un farmaco sperimentale in fase clinica, RRx-001, possa attaccare i tumori del fegato in modo insolitamente intelligente: tagliando una fonte chiave della «batteria» cellulare e, contemporaneamente, trasformando le cellule tumorali morenti in un segnale simile a un vaccino che risveglia il sistema immunitario.
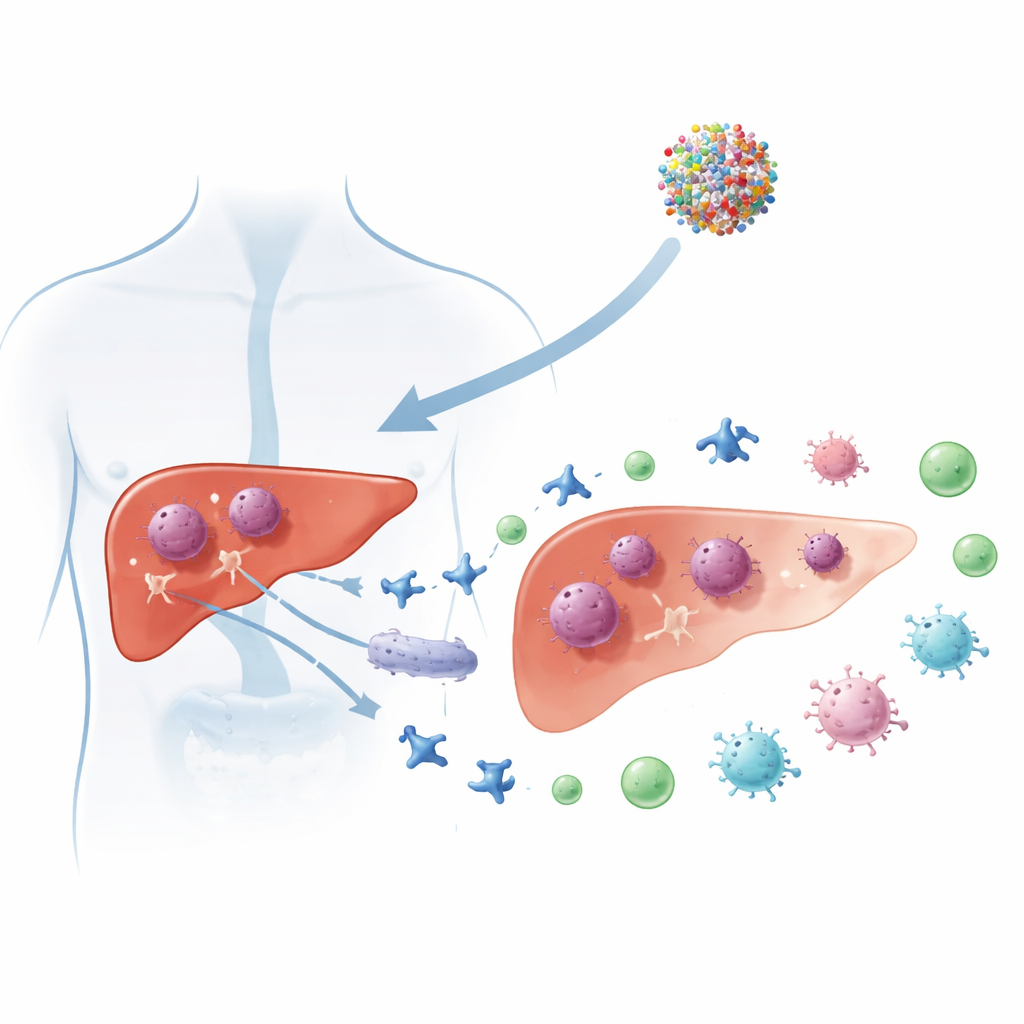
Una nuova modalità di morte delle cellule tumorali
Gli scienziati considerano sempre più il trattamento del cancro come una questione di controllo di come le cellule tumorali vivono e muoiono. Oltre alle forme di morte cellulare ben note come l’apoptosi, i ricercatori hanno recentemente identificato la «disulfidptosi», un tipo di morte programmata che si verifica quando le cellule non sono più in grado di gestire certi legami chimici chiamati disolfuri nel loro scheletro interno. Quando questo equilibrio collassa, l’impalcatura che mantiene la forma cellulare si contrae e si disintegra, portando a una rapida morte cellulare. La promessa della disulfidptosi è che sfrutta una debolezza nel metabolismo alterato delle cellule tumorali, permettendo potenzialmente un targeting più selettivo del tumore.
Colpire l’alimentazione energetica del tumore
Le cellule tumorali dipendono fortemente dalla molecola NADPH per mantenere stabile la loro chimica interna e neutralizzare molecole reattive dannose. Una fonte principale di NADPH è una via metabolica chiamata via dei pentoso-fosfati, controllata da un enzima denominato G6PD. In questo studio, i ricercatori hanno confrontato diversi composti che bloccano varie vie di produzione del NADPH e hanno scoperto che RRx-001 era il più potente nell’uccidere cellule di carcinoma epatocellulare in coltura. Diversamente da altri inibitori, la morte cellulare indotta da RRx-001 poteva essere parzialmente invertita da una sostanza chimica che rompe specificamente i legami disolfuro, e le cellule mostravano il caratteristico collasso delle fibre di actina interne. Questi segni indicavano che RRx-001 stava innescando la disulfidptosi, e non una semplice tossicità generica.
Dal collasso metabolico all’allarme immunitario
Bloccando G6PD, RRx-001 ha prosciugato il NADPH, alterato l’equilibrio tra glutatione protettivo e ossidato e permesso l’accumulo di specie reattive ossigenate e azotate dannose. Questo stress chimico ha spinto le cellule del carcinoma epatocellulare verso la disulfidptosi, ma ha anche fatto qualcosa in più: ha causato l’esposizione e il rilascio di cosiddetti segnali di pericolo, o DAMP, inclusi molecole come la calreticulina e le proteine da shock termico. Al microscopio elettronico, le cellule trattate mostravano organelli danneggiati e membrane alterate, cambiamenti coerenti con una forma di morte cellulare in grado di mobilitare il sistema immunitario anziché passare inosservata.
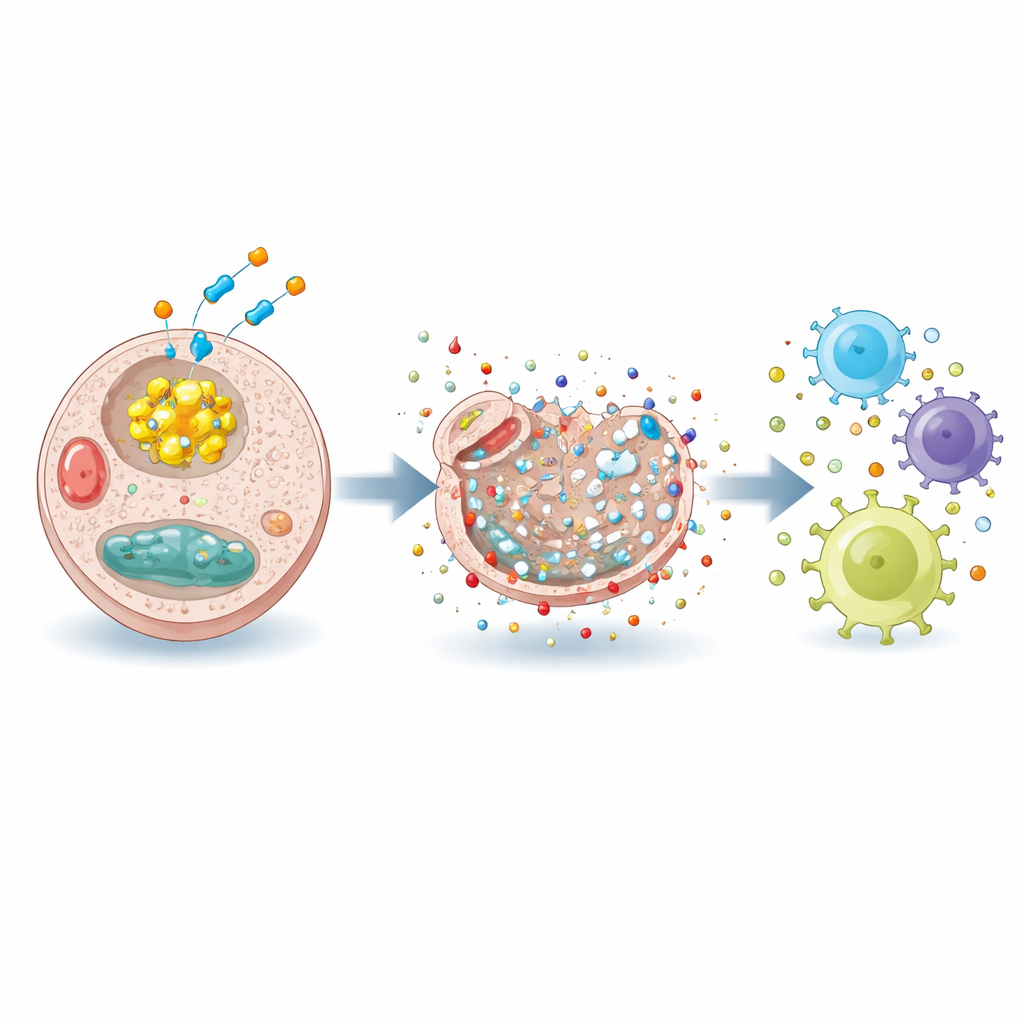
Trasformare i tumori da “freddi” a “caldi”
Il gruppo ha poi testato RRx-001 in topi portatori di tumori epatici. I tumori trattati con il farmaco crescevano più lentamente e pesavano meno rispetto a quelli negli animali non trattati. Un’analisi dettagliata del tessuto tumorale ha rivelato una maggiore infiltrazione di cellule T helper (CD4+) e citotossiche (CD8+), uno spostamento dei macrofagi verso un tipo più infiammatorio e antitumorale, e livelli ridotti di PD-L1, una proteina di superficie che i tumori usano per spegnere gli attacchi immunitari. I modelli di attività genica nei tumori mostravano l’attivazione della segnalazione del recettore delle cellule T e delle vie di differenziazione delle cellule T helper, tutti segnali che il sistema immunitario era stato mobilitato anziché soppresso.
Cosa potrebbe significare per i trattamenti futuri
Nel complesso, i risultati suggeriscono che RRx-001 attacca il carcinoma epatocellulare su due fronti: sfrutta un tallone d’Achille metabolico privando le cellule di NADPH e costringendole alla disulfidptosi, e allo stesso tempo trasforma la loro morte in un evento che stimola il sistema immunitario noto come morte cellulare immunogenica. Per i pazienti, questo apre la possibilità di terapie che non solo riducono direttamente i tumori ma aiutano anche l’organismo a riconoscere e combattere il cancro in modo più efficace. Gli autori propongono che RRx-001 potrebbe essere particolarmente efficace se combinato con gli attuali inibitori del checkpoint immunitario, potenzialmente convertendo tumori epatici “freddi” difficili da trattare in tumori “caldi” più reattivi all’immunoterapia.
Citazione: Huang, H., He, Y., Chen, J. et al. RRx-001 inhibits G6PD to deplete NADPH and trigger disulfidptosis coupled with DAMP-mediated immunogenic cell death in hepatocellular carcinoma. Cell Death Discov. 12, 194 (2026). https://doi.org/10.1038/s41420-026-03032-y
Parole chiave: carcinoma epatocellulare, metabolismo del cancro, morte cellulare immunogenica, immunoterapia del tumore, RRx-001