Clear Sky Science · ja
[64Cu]Cu-DOTA-TYPE7:EphA2陽性腫瘍を標的とするPET放射性トレーサー
隠れた腫瘍を可視化する
がんはしばしば目に見えない場所で進行し、明確な症状が現れる前に体内で成長します。医師は早期発見と治療方針の決定に高度な画像診断に頼りますが、多くの画像法は悪性の腫瘍と無害な組織を区別できません。本研究は、特定のがん関連受容体を持つ腫瘍を選択的に光らせるよう設計された新しい放射性トレーサーを紹介します。これにより、医師が危険な病変をより明確に捉え、患者ごとに治療を調整できる可能性があります。
細胞上のがんの“旗”を標的にする
多くの腫瘍は表面にEphA2というタンパク質を異常に高いレベルで発現しており、これはより浸潤性が高く治療抵抗性を示す病態と関連する分子上の“旗”のようなものです。健康な成人組織では通常この旗は低レベルでしか見られませんが、乳がん、肺がん、膵臓がん、大腸がんなど多くの臓器のがんで高発現が観察されます。そのためEphA2はイメージングと治療の両方で魅力的な標的となり、がん細胞を正常細胞から識別し、放射線を必要な場所に正確に集中させる手段を提供します。
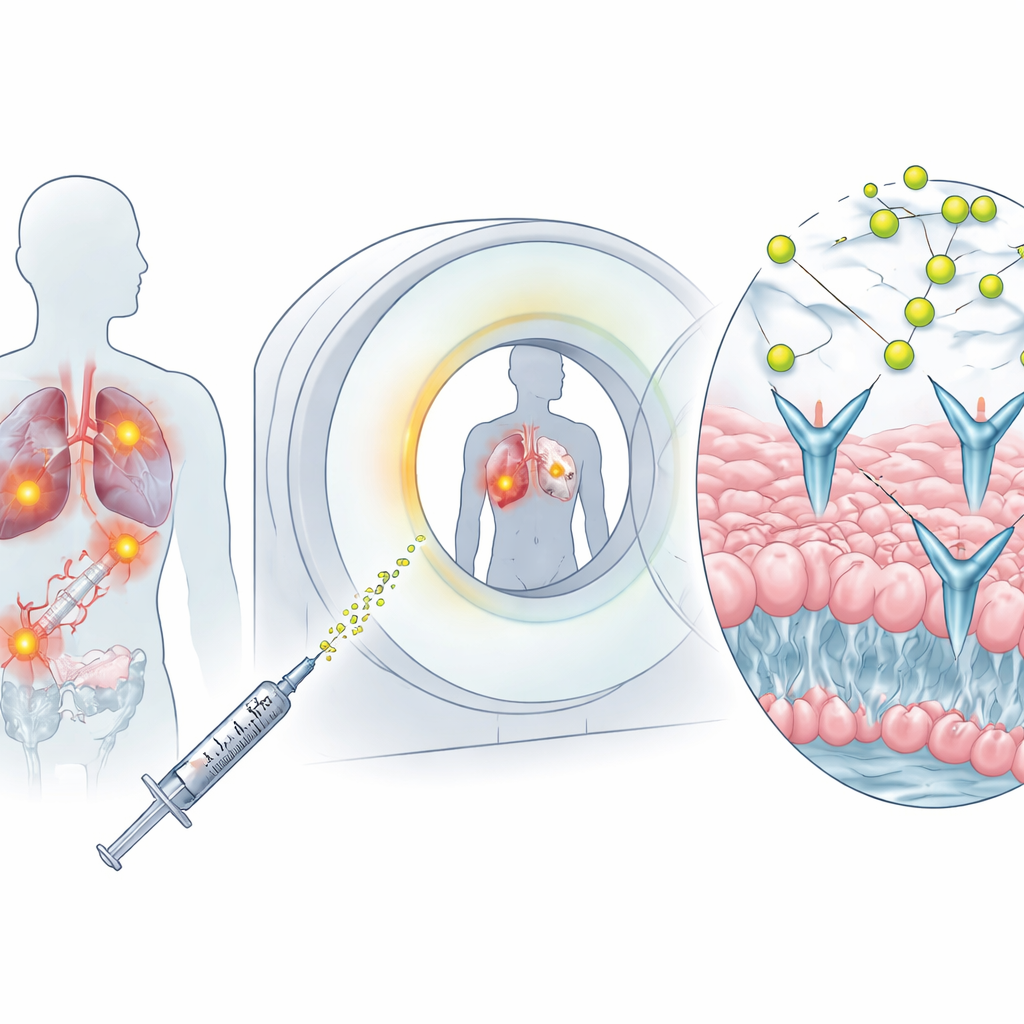
PETスキャン向けに設計された専用トレーサー
研究者らは、細胞の外層に入り込みEphA2に結合できる小さく可溶性のペプチドTYPE7を開発しました。TYPE7は化学的“ホルダー”であるDOTAに結合され、DOTAは放射性金属である銅‑64をしっかり保持します。血流に注入されると、この新しいトレーサー[64Cu]Cu‑DOTA‑TYPE7は体内を循環し、EphA2豊富な細胞を探し出します。実験室試験では、穏やかな条件下で効率よく銅‑64で標識でき、血液様の液や肝酵素存在下でも数時間にわたりほぼ分解されずに残ることが示され、イメージングに十分な持続性があることが確認されました。
正しい細胞に結合することの検証
トレーサーが本当にEphA2陽性細胞を好むかどうかを確認するため、チームは大量のEphA2を産生する細胞とほとんど産生しない細胞という2種類の培養細胞を比較しました。EphA2が豊富な細胞は、すべての測定時点ではるかに多くのトレーサーを取り込み、低発現細胞は弱い取り込みしか示しませんでした。さらに非放射性のTYPE7を過剰に添加すると放射性トレーサーの結合が阻害され、結合がランダムな付着ではなく特異的であることが示されました。重要な点として、トレーサーの大部分は細胞内に取り込まれるのではなく細胞表面に留まっており、これは膜上に存在するEphA2受容体の局在と一致します。
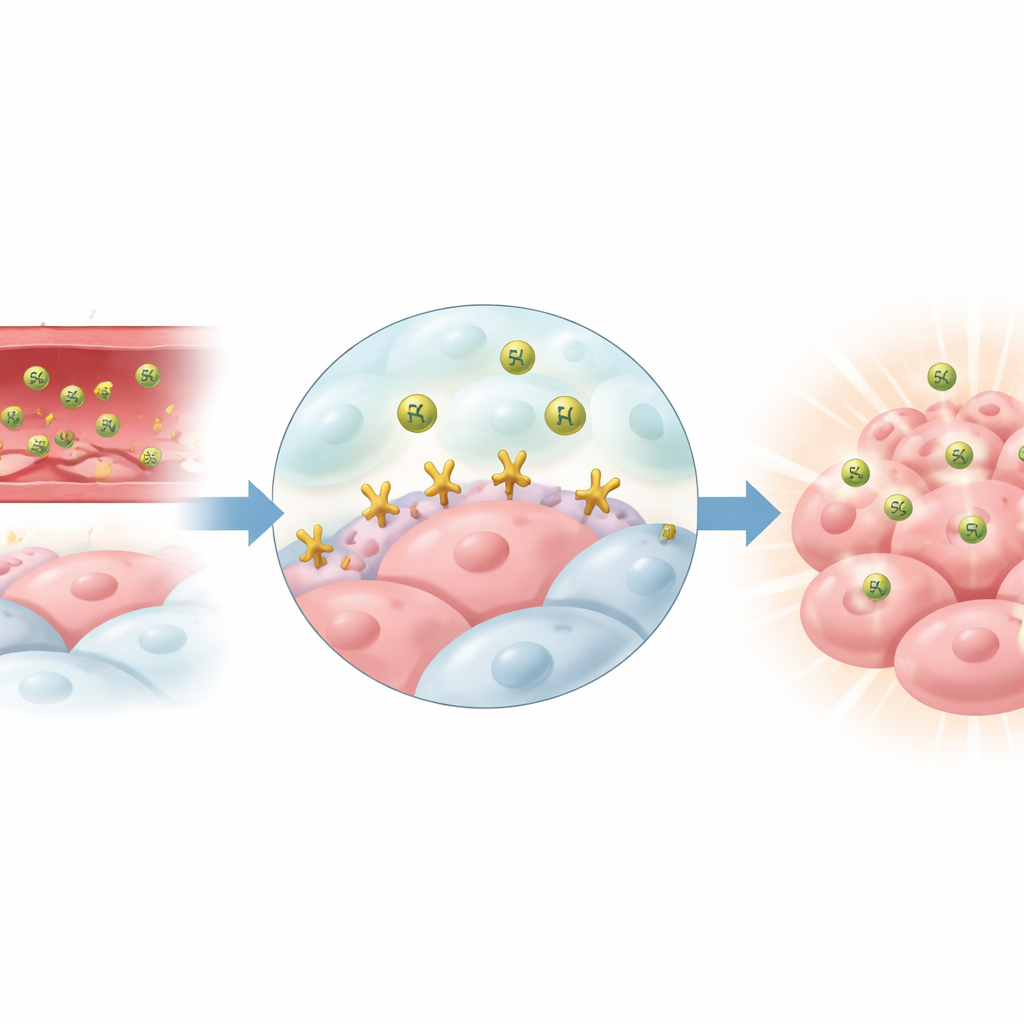
生体マウスで腫瘍を光らせる
次に、このトレーサーが生体内で腫瘍を見つけられるかを検証しました。マウスにはEphA2を発現するかしないかのヒトがん細胞が移植され、注射後の複数の時点でPET/CTで撮像されました。EphA2陽性腫瘍を持つマウスではトレーサーが腫瘍組織に強く蓄積し、注射から約4時間でピークに達して明瞭で高コントラストの画像が得られました。同じトレーサーを大量の非放射性TYPE7と同時投与すると腫瘍シグナルは大幅に低下し、体内での結合もEphA2依存であることが示されました。EphA2を欠く腫瘍ではトレーサー取り込みは低レベルにとどまりました。小さなペプチドに期待される通り、残存する放射能の多くは肝臓や腎臓を通じて排泄されました。
患者にとっての意義
総じて、本研究は[64Cu]Cu‑DOTA‑TYPE7がEphA2豊富な腫瘍に選択的に集積し、適切なタイミングと良好なコントラストでPET画像に可視化できることを示しています。銅‑64には治療用核種である銅‑67という対応物が存在するため、このトレーサーの近縁体は将来的に腫瘍の位置を示すと同時に同じ部位へ細胞破壊をもたらす放射線を届けることも可能になるかもしれません。安定性の向上、ペプチドの改良、さらに多様な腫瘍モデルでの検証といった追加研究は必要ですが、このアプローチは大きさや位置だけでなく分子の特徴に基づいて攻撃的ながんを見つけ治療する汎腫瘍的なツールに近づけるものです。
引用: Sanwick, A.M., Alves, D.S., Haugh, K.N. et al. [64Cu]Cu-DOTA-TYPE7: a targeted PET radiotracer for imaging EphA2+ tumors. npj Imaging 4, 33 (2026). https://doi.org/10.1038/s44303-026-00168-5
キーワード: EphA2, PETイメージング, 銅‑64 トレーサー, がんバイオマーカー, セラノスティクス