Clear Sky Science · fr
[64Cu]Cu-DOTA-TYPE7 : un radiotraceur PET ciblé pour l’imagerie des tumeurs EphA2+
Voir les tumeurs cachées
Les cancers se dissimulent souvent sous nos yeux, se développant à l’intérieur du corps longtemps avant d’induire des symptômes évidents. Les médecins s’appuient sur des examens avancés pour détecter ces tumeurs précocement et orienter le traitement, mais de nombreux outils d’imagerie ne savent pas distinguer les cancers agressifs des tissus bénins. Cette étude présente un nouveau type de traceur radioactif conçu pour éclairer les tumeurs exprimant un récepteur lié au cancer, ce qui pourrait permettre aux praticiens de mieux repérer les lésions dangereuses et d’adapter la thérapie à chaque patient.
Cibler un marqueur tumoral à la surface des cellules
Beaucoup de tumeurs affichent en abondance à leur surface une protéine appelée EphA2, une sorte de drapeau moléculaire associé à des formes de maladie plus invasives et résistantes aux traitements. Les tissus sains de l’adulte en expriment généralement de faibles niveaux, mais les cancers du sein, du poumon, du pancréas, du côlon et de plusieurs autres organes en présentent souvent en grande quantité. Pour cette raison, EphA2 est devenu un marqueur attrayant pour l’imagerie et la thérapie, offrant un moyen de distinguer les cellules cancéreuses des cellules normales et de diriger la radiation précisément là où elle est nécessaire.
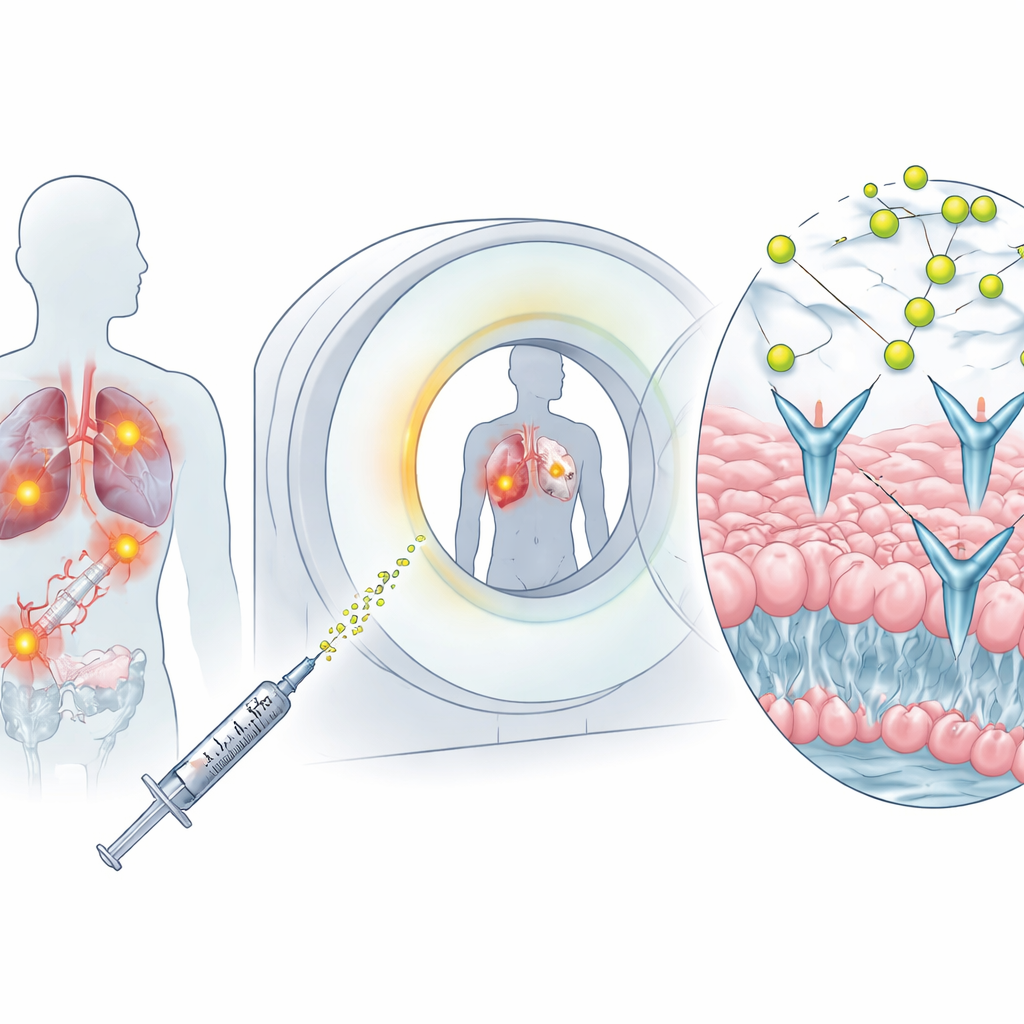
Un traceur conçu sur mesure pour la TEP
Les chercheurs ont mis au point un petit peptide soluble nommé TYPE7, capable de s’insérer dans la couche externe de la cellule et de se lier à EphA2. Ils ont fixé TYPE7 à un « support » chimique appelé DOTA, qui enferme solidement le métal radioactif cuivre‑64. Lorsqu’il est injecté dans la circulation, ce nouveau traceur, [64Cu]Cu‑DOTA‑TYPE7, parcourt l’organisme et cible les cellules riches en EphA2. Des tests en laboratoire ont montré que le traceur pouvait être marqué efficacement avec le cuivre‑64 dans des conditions douces et qu’il restait majoritairement intact dans des milieux simulant le sang et en présence d’enzymes hépatiques pendant plusieurs heures, suffisamment longtemps pour réaliser l’imagerie.
Prouver qu’il se lie aux bonnes cellules
Pour confirmer que le traceur préfère réellement les cellules EphA2‑positives, l’équipe a comparé deux types de cellules en culture : l’une exprimant beaucoup d’EphA2 et l’autre très peu. Les cellules riches en EphA2 ont absorbé nettement plus de traceur à chaque point temporel mesuré, tandis que les cellules à faible expression n’ont montré qu’une faible captation. Lorsque les chercheurs ont saturé le système avec du TYPE7 non radioactif, cela a bloqué la liaison du traceur radioactif, démontrant que l’attachement était spécifique et non dû à un collage aléatoire. Fait important, le traceur restait majoritairement à la surface cellulaire plutôt que d’être internalisé, ce qui correspond à la localisation du récepteur EphA2 dans la membrane.
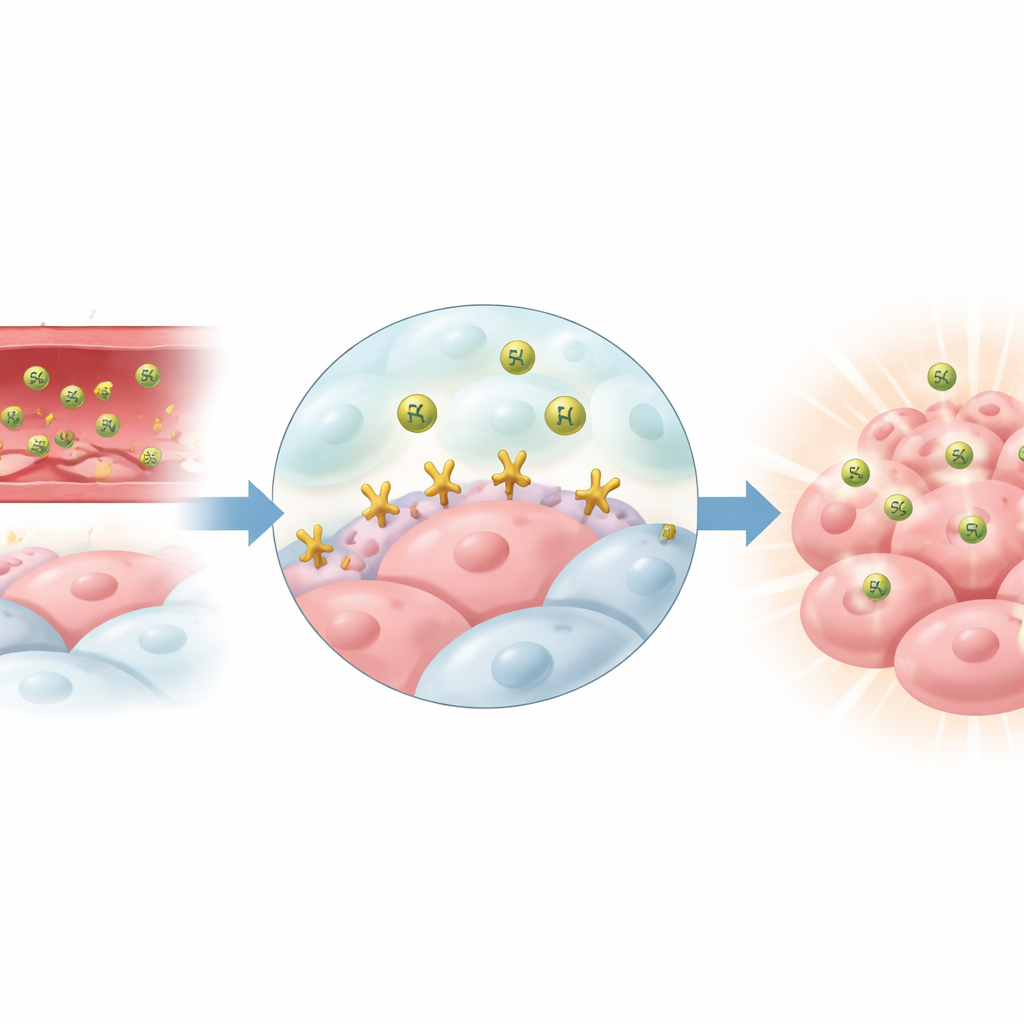
Illuminer les tumeurs chez la souris vivante
L’étape suivante a consisté à vérifier si le traceur pouvait repérer des tumeurs au sein d’un organisme vivant. Des souris ont été implantées avec des cellules cancéreuses humaines exprimant ou non EphA2, puis scannées à plusieurs moments après injection par TEP/CT. Chez les souris portant des tumeurs EphA2‑positives, le traceur s’est fortement accumulé dans le tissu tumoral, avec un pic vers quatre heures après injection et des images nettes à fort contraste. Lorsque le même traceur était administré en même temps qu’une forte dose de TYPE7 non radioactif, les signaux tumoraux chutaient fortement, montrant que la liaison in vivo restait dirigée par EphA2. Les tumeurs dépourvues d’EphA2 présentaient une captation faible. Comme attendu pour un petit peptide, une grande partie de la radioactivité résiduelle était éliminée par le foie et les reins.
Ce que cela pourrait signifier pour les patients
Dans l’ensemble, l’étude montre que [64Cu]Cu‑DOTA‑TYPE7 peut cibler des tumeurs riches en EphA2 et les rendre visibles en TEP avec un bon timing et un bon contraste. Parce que le cuivre‑64 a un homologue thérapeutique, le cuivre‑67, une version apparentée de ce traceur pourrait un jour à la fois localiser le cancer et délivrer une radiation létale aux mêmes sites. Bien que des travaux supplémentaires soient nécessaires pour améliorer la stabilité, affiner le peptide et le tester sur d’autres modèles tumoraux, cette approche rapproche le domaine d’outils pan‑tumoraux permettant aux médecins de voir et de traiter les cancers agressifs en se basant sur leur empreinte moléculaire plutôt que sur leur taille ou leur localisation.
Citation: Sanwick, A.M., Alves, D.S., Haugh, K.N. et al. [64Cu]Cu-DOTA-TYPE7: a targeted PET radiotracer for imaging EphA2+ tumors. npj Imaging 4, 33 (2026). https://doi.org/10.1038/s44303-026-00168-5
Mots-clés: EphA2, Imagerie TEP, traceur au cuivre‑64, biomarqueur du cancer, théranostique