Clear Sky Science · ja
アイリシンは脂肪組織のIL-33と制御性T細胞を介して肥満とインスリン抵抗性を改善する
なぜ「運動の分子」が体重と血糖に重要なのか
肥満と2型糖尿病は現在、世界中で数億人に影響を及ぼしており、多くの治療は主に摂取カロリーの制限に焦点を当てています。本研究は別の視点を探ります:運動する筋肉から分泌される自然なホルモン、アイリシンが脂肪組織と免疫系にどのように働きかけ、食事制限や筋肉量の喪失なしにエネルギー消費を増やし、炎症を抑え、血糖を改善するかを明らかにしようとしています。
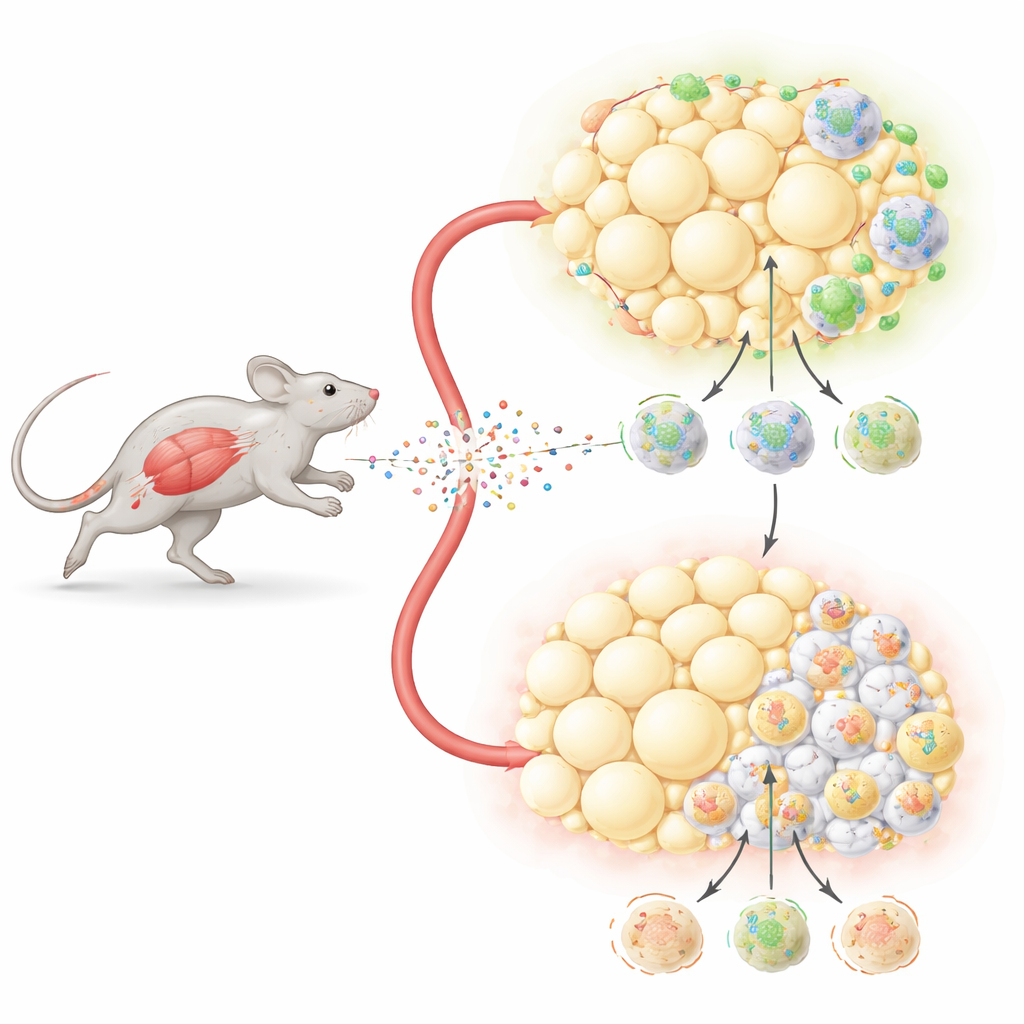
働く筋肉から放たれるメッセンジャー
運動すると筋肉はアイリシンを血流中に放出します。これまでの研究で、アイリシンは皮下にあるエネルギーを蓄える白色脂肪をより活動的で熱を生む状態に変え得ることが示されていました。しかし、この信号が糖尿病や心疾患と強く関連する腹部の深い脂肪(内臓脂肪)にどのように影響するかは不明でした。本研究では、研究者らは無害なウイルスベクターを用いて肝臓から持続的にホルモンを放出させ、雄マウスでアイリシン濃度を上げました。その後、マウスに高脂肪食を数週間与え、肥満とインスリン抵抗性を誘導し、人間の一般的な代謝異常を模倣しました。
脂肪は減り、血糖は改善、食欲は変わらず
長期的にアイリシンが上昇したマウスは、高脂肪食下でも対照群より体重増加が少なかった。摂取した食物量や運動量は同等でした。スキャン解析は、体重差が主に脂肪量の減少によるもので、筋肉などの除脂肪組織の損失によるものではないことを示しました。これらのマウスは糖やインスリンの処理も良好で、グルコースやインスリン注射後の血糖値がより早く、より低いレベルまで下がりました。全身のエネルギー消費の測定は、アイリシン処理マウスが常時より多くのカロリーを燃焼していることを示し、これらの脂肪組織が貯蔵庫よりも炉のように振る舞っていることを示唆しました。
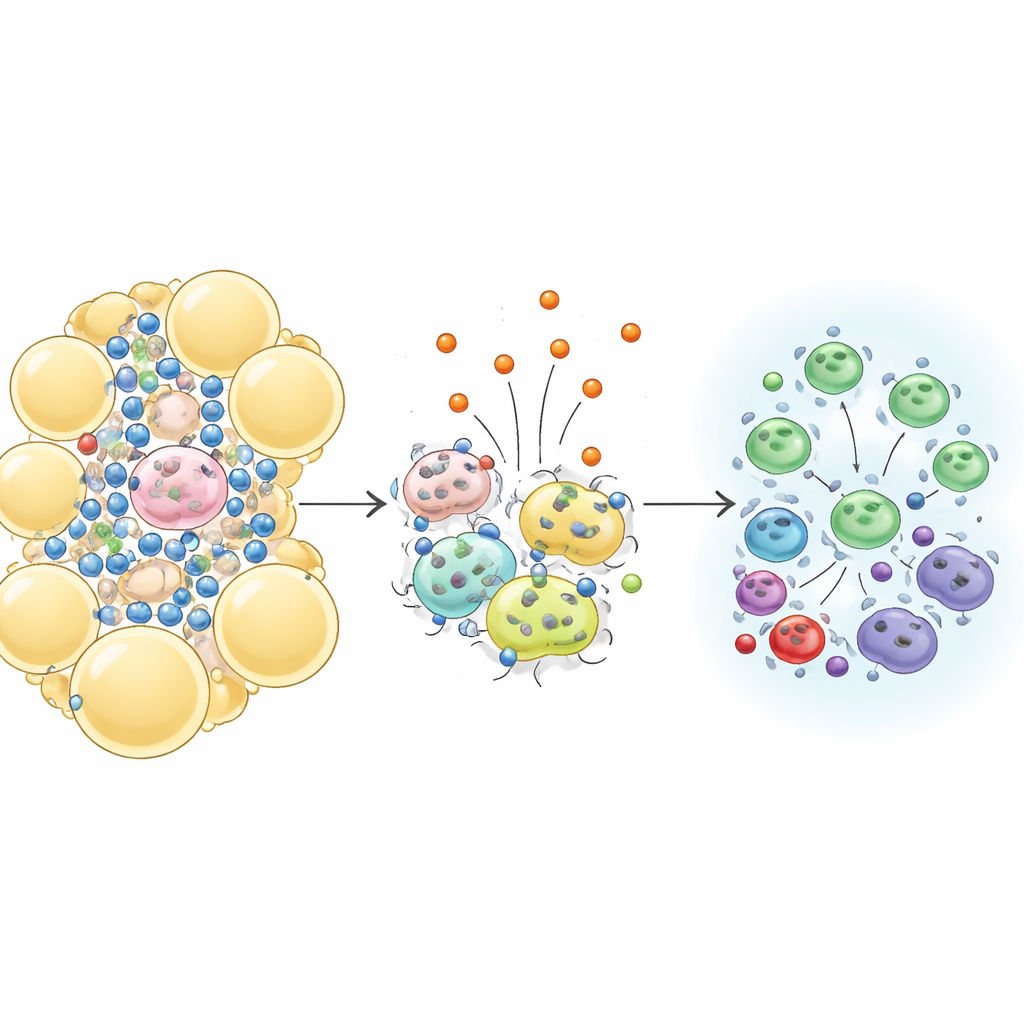
内臓脂肪における有害な炎症の抑制
腹部の内臓脂肪は単なる受動的な貯蔵部位ではなく、慢性的に炎症を起こし得る免疫細胞が豊富に存在し、肥満時には正常な代謝を妨げます。研究チームはマウスの内臓脂肪中のこれらの細胞を精密にマッピングしました。長期の高脂肪食を与えた対照群では予想どおり、攻撃的な免疫細胞が増え、炎症を抑える働きを持つ制御性T細胞が著しく減少していました。対照的に、追加のアイリシンをもつマウスでは、特にST2という受容体を持つサブセットを含むこれらの保護的な細胞群がしっかり維持され、炎症性細胞は少なくなっていました。組織切片でも、死んだ脂肪細胞が免疫細胞に取り囲まれてできる「クラウン様構造(冠状構造)」が減少しており、進行中の損傷が少ないことを示していました。
三者の対話:アイリシン、間質細胞、免疫の守り手
アイリシンがこれらの守護細胞を維持する仕組みを理解するため、研究者らは脂肪組織のもう一つの重要な要因、構造支持を担う間質(メセンキマル)細胞に注目しました。内臓脂肪の一部の間質細胞は通常、ST2を持つ制御性T細胞の生存に不可欠なシグナルタンパク質IL-33を産生します。本研究は、慢性的なアイリシン処理が内臓脂肪におけるIL-33産生間質細胞の数と活性を増加させ、局所および血中のIL-33レベルを高めることを示しました。細胞培養では、アイリシンは間質細胞に直接作用してIL-33の発現を促進し、新しい脂肪細胞への分化に関わる遺伝子を抑えることが示され、免疫を支える役割へのシフトが示唆されました。アイリシンがこれらの細胞で用いる特定のインテグリン受容体を遮断するとIL-33の増加が阻止され、この効果が特定の表面経路に結びつくことが示されました。
IL-33の関与を立証し、信号を他の脂肪へ広げる
次に研究チームは、IL-33が本当にアイリシンの代謝上の利点に必要かを問いただしました。アイリシンの前駆体タンパク質(FNDC5)を欠くマウスでは、内臓脂肪と血中のIL-33レベルが低く、保護的な制御性T細胞が乏しく、肥満に関連する血糖問題が悪化していました;外部からアイリシンを補うとIL-33が回復し、代謝が改善しました。逆に、研究者らが設計タンパク質による“トラップ”でアイリシン処理された肥満マウスでIL-33を捕捉すると、その利点は大部分消失しました:脂肪量は再び増加し、エネルギー消費は低下し、グルコースおよびインスリン応答は悪化しました。別の遺伝学的検証では、制御性T細胞からのみST2受容体を除去すると、炎症を鎮め血糖を改善するアイリシンの能力が鈍りました。同時に、アイリシンは皮下脂肪での熱産生遺伝子の活性も高め、これもIL-33を必要としました。これらを合わせると、アイリシンが間質細胞を駆動してIL-33を産生させ、IL-33が内臓脂肪の制御性T細胞を養い、皮下脂肪の熱産生プログラムを高めるという多組織にまたがる中継経路が描かれ、全体としてより多くのエネルギーを燃やし代謝制御を改善する方向へ体をシフトさせることが示されます。
将来の治療にとっての意味
この研究は、運動中に私たちの体がすでに作っているホルモンが、食欲を抑えることなく脂肪組織と局所免疫細胞を再プログラムし、肥満やインスリン抵抗性に対抗し得ることを示しています。特定のアイリシン–IL-33–制御性T細胞軸を明らかにしたことで、代謝に対する運動の利点を模倣する新たな薬物戦略が示唆されます。これらの実験は雄マウスで行われ、人での検証はまだ多く残されているものの、将来の治療は食欲に焦点を当てた薬とこの脂肪–免疫間のコミュニケーション回路を活性化する薬剤を組み合わせることで、より安全かつ強力に代謝健康を改善できる可能性を示唆しています。
引用: A, M., Wang, G., Zammit, N.W. et al. Irisin ameliorates obesity and insulin resistance via adipose tissue IL-33 and regulatory T cells. Nat Metab 8, 885–901 (2026). https://doi.org/10.1038/s42255-026-01491-2
キーワード: アイリシン, 脂肪組織, 制御性T細胞, IL-33, 熱産生