Clear Sky Science · de
Irisin verbessert Fettleibigkeit und Insulinresistenz über IL-33 im Fettgewebe und regulatorische T‑Zellen
Warum ein Trainingshormon für Gewicht und Blutzucker wichtig ist
Adipositas und Typ‑2‑Diabetes betreffen heute weltweit Hunderte Millionen Menschen, und viele Behandlungen zielen überwiegend darauf ab, weniger zu essen. Diese Studie verfolgt einen anderen Ansatz: Wie ein natürliches Hormon, das beim Sport aus den Muskeln freigesetzt wird – genannt Irisin – mit dem Fettgewebe und dem Immunsystem kommuniziert, um mehr Energie zu verbrennen, Entzündungen zu dämpfen und den Blutzucker zu verbessern, ohne die Nahrungsaufnahme zu reduzieren oder Muskelmasse zu verlieren.
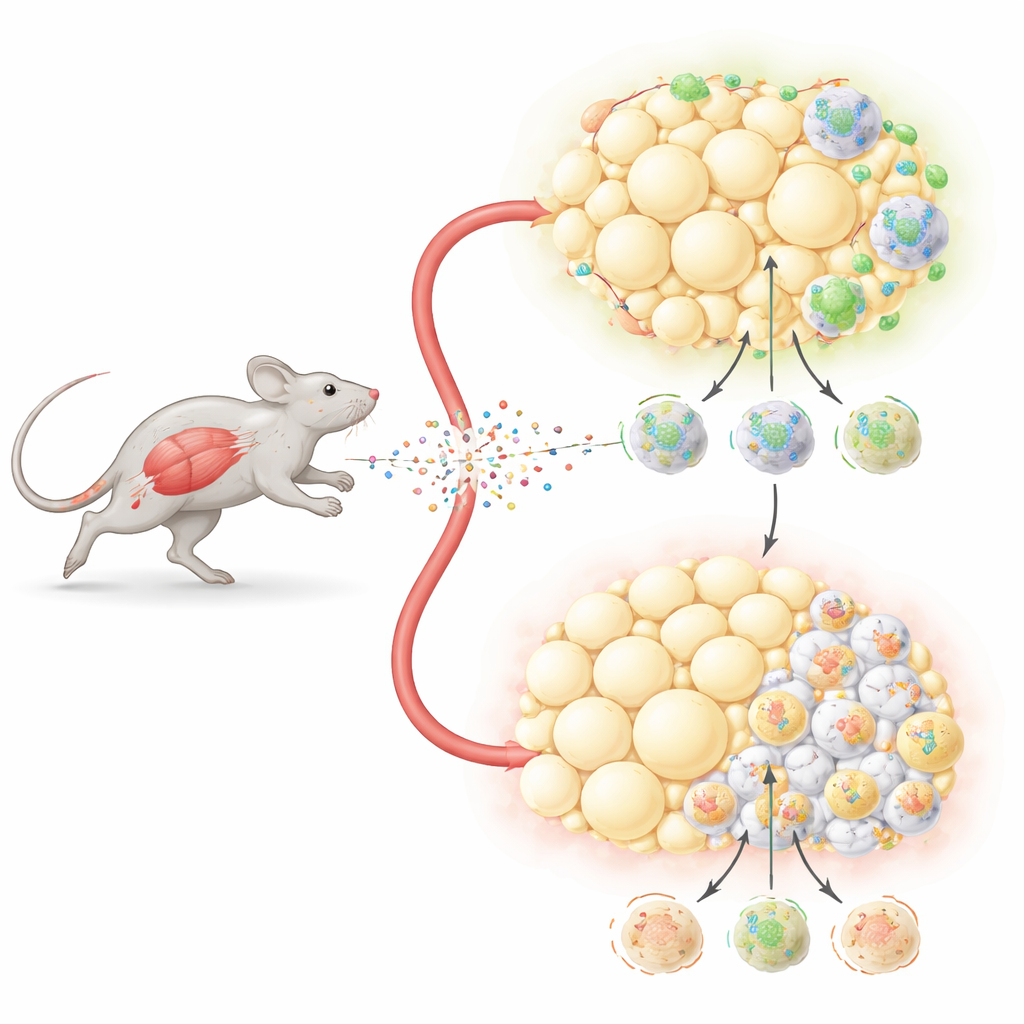
Ein Botenstoff aus arbeitenden Muskeln
Beim Training schütten unsere Muskeln Irisin ins Blut aus. Frühere Arbeiten zeigten, dass Irisin weißes, energiereiches Unterhautfett in eine aktivere, wärmeerzeugende Form umwandeln kann. Unklar war jedoch, wie dieses Signal das tiefere viszerale Bauchfett beeinflusst, das eng mit Diabetes und Herzkrankheiten verbunden ist. In der vorliegenden Studie erhöhten die Forschenden die Irisinspiegel bei männlichen Mäusen mithilfe eines harmlosen Virus, das die Leber dazu brachte, das Hormon dauerhaft freizusetzen. Anschließend wurden die Mäuse über viele Wochen mit einer fettreichen Diät gefüttert, um Fettleibigkeit und Insulinresistenz zu induzieren und so häufige menschliche Stoffwechselstörungen nachzuahmen.
Weniger Fett, besserer Blutzucker, gleiches Appetitverhalten
Mäuse mit langfristig erhöhtem Irisin gewannen auf der fettreichen Diät weniger Gewicht als Kontrolltiere, obwohl sie die gleiche Menge Nahrung zu sich nahmen und sich ähnlich viel bewegten. Scans zeigten, dass der Gewichtsunterschied hauptsächlich auf einen geringeren Fettanteil zurückzuführen war und nicht auf Verlust von magerem Gewebe wie Muskel. Diese Tiere bewältigten außerdem Glukose und Insulin besser: Nach Injektionen von Glukose oder Insulin sanken ihre Blutzuckerwerte schneller und auf niedrigere Werte. Messungen des gesamten Energieverbrauchs zeigten, dass die Irisin‑behandelten Tiere rund um die Uhr mehr Kalorien verbrannten, was darauf hindeutet, dass ihr Fettgewebe eher wie ein Ofen denn als Speicher fungierte.
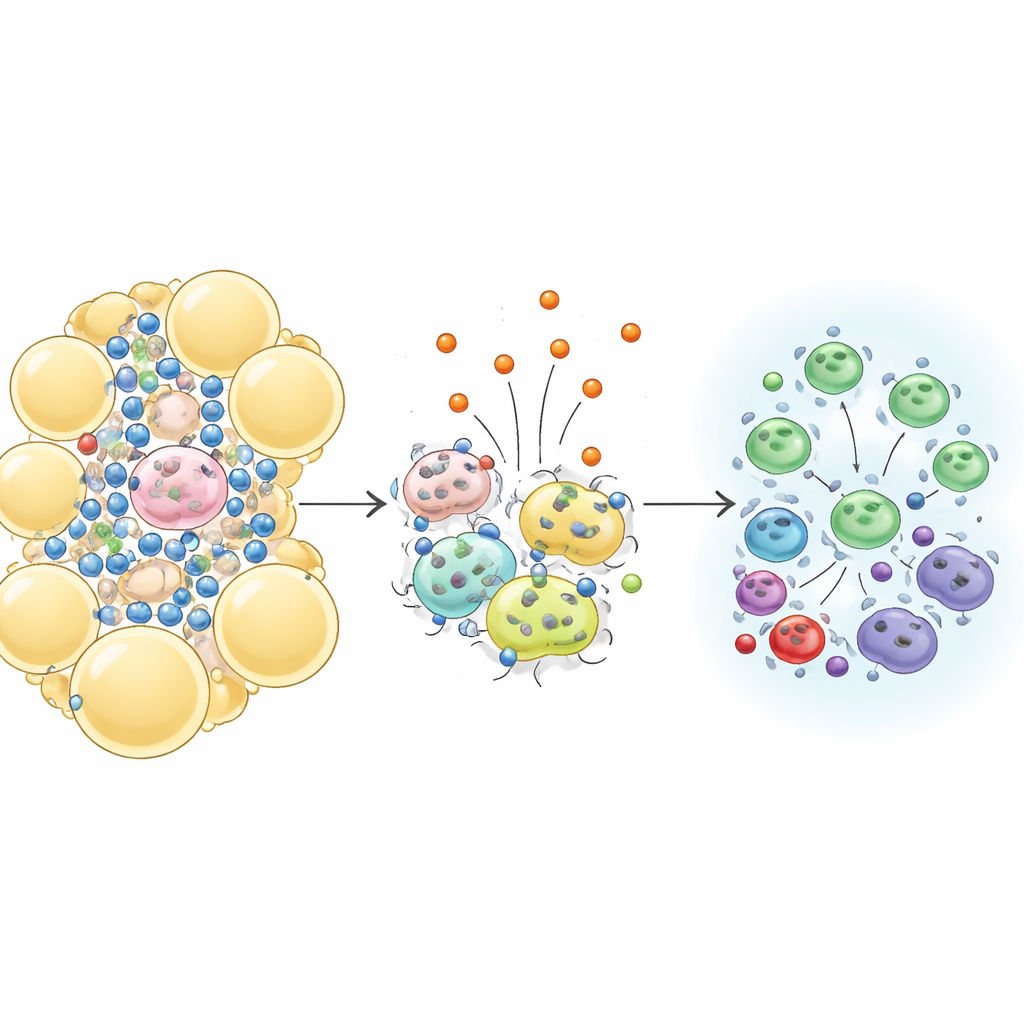
Schädliche Entzündungen im Bauchfett dämpfen
Bauch‑ bzw. viszerales Fett ist nicht nur ein passiver Speicherort; es ist voller Immunzellen, die bei Adipositas chronisch entzündet werden können und die normale Stoffwechselaktivität stören. Das Team kartierte diese Zellen im Viszeralfett der Mäuse sorgfältig. Unter langfristiger fettreicher Ernährung zeigten die Kontrolltiere das erwartete Muster: mehr aggressive Immunzellen und ein deutlicher Rückgang einer schützenden Zellpopulation, der regulatorischen T‑Zellen, die normalerweise Entzündungen in Schach halten. Im Gegensatz dazu behielten Mäuse mit zusätzlichem Irisin eine robuste Population dieser schützenden Zellen, insbesondere einen Teilbestand, der den Rezeptor ST2 trägt, und wiesen gleichzeitig weniger entzündliche Zellen auf. Histologische Schnitte des Fettgewebes zeigten außerdem weniger „crown‑like structures“, Narben, die tote Fettzellen umgeben von Immunzellen markieren, was auf geringere anhaltende Schäden hindeutet.
Ein Dreiecks‑Gespräch: Irisin, Stroma‑Zellen und Immunwächter
Um zu verstehen, wie Irisin diese Wächterzellen bewahrte, richteten die Forschenden den Blick auf einen weiteren Schlüsselakteur im Fettgewebe: strukturelle Stütz‑Zellen, bekannt als mesenchymale Stromazellen. In viszeralem Fett produziert eine Untergruppe dieser Stromazellen normalerweise das Signalmolekül IL‑33, das für das Überleben der ST2‑tragenden regulatorischen T‑Zellen entscheidend ist. Die Studie fand heraus, dass chronische Irisin‑Behandlung sowohl die Zahl als auch die Aktivität der IL‑33‑produzierenden Stromazellen im Viszeralfett erhöhte und die IL‑33‑Spiegel lokal und im Blut ansteigen ließ. In Zellkultur veranlasste Irisin Stromazellen direkt dazu, IL‑33 hochzufahren und Gene zu drosseln, die mit der Umwandlung in neue Fettzellen verbunden sind, was auf eine Verschiebung hin zu einer immununterstützenden Funktion hindeutet. Das Blockieren des spezifischen Integrinrezeptors, den Irisin auf diesen Zellen nutzt, verhinderte diesen IL‑33‑Anstieg und verknüpfte den Effekt mit einem definierten Oberflächenweg.
Den IL‑33‑Zusammenhang beweisen und das Signal auf anderes Fett ausweiten
Die Forschenden prüften anschließend, ob IL‑33 wirklich für Irisins metabolische Vorteile erforderlich ist. Bei Mäusen, denen das Irisin‑Vorläuferprotein (FNDC5) fehlte, waren die IL‑33‑Spiegel im Viszeralfett und im Blut niedriger, schützende regulatorische T‑Zellen seltener und die diabetes‑ähnlichen Stoffwechselstörungen ausgeprägter; die Gabe von zusätzlichem Irisin stellte IL‑33 wieder her und verbesserte den Stoffwechsel. Umgekehrt verschwanden die Vorteile größtenteils, wenn die Forschenden IL‑33 in Irisin‑behandelten adipösen Mäusen mit einem konstruierten „Trap“‑Protein neutralisierten: Die Fettmasse stieg, der Energieverbrauch fiel und Glukose‑ sowie Insulinantworten verschlechterten sich. In einem weiteren genetischen Test schwächte das Entfernen des ST2‑Rezeptors ausschließlich aus regulatorischen T‑Zellen Irisins Fähigkeit, Entzündungen zu dämpfen und den Blutzucker zu verbessern. Zugleich erhöhte Irisin die Aktivität wärmebildender Gene im subkutanen Fett, und auch dies erforderte IL‑33. Zusammengenommen skizzieren diese Befunde eine Mehrgewebe‑Relay: Irisin veranlasst Stromazellen zur IL‑33‑Produktion, IL‑33 fördert regulatorische T‑Zellen im Bauchfett und stärkt thermogene Programme im Unterhautfett, sodass das System den Körper in Richtung höherer Energieverbrennung und besserer metabolischer Kontrolle verschiebt.
Was das für künftige Therapien bedeuten könnte
Diese Arbeit zeigt, dass ein Hormon, das unser Körper beim Sport bereits bildet, Fettgewebe und lokale Immunzellen so umprogrammieren kann, dass Adipositas und Insulinresistenz entgegengewirkt wird – ohne den Appetit zu unterdrücken. Indem sie eine spezifische Irisin–IL‑33–regulatorische T‑Zell‑Achse aufdecken, deutet die Studie auf neue Strategien für Arzneimittel hin, die die Stoffwechselvorteile von Bewegung nachahmen. Obwohl diese Experimente an männlichen Mäusen durchgeführt wurden und beim Menschen noch viel zu prüfen bleibt, legen die Ergebnisse nahe, dass künftige Therapien appetitfokussierte Mittel mit Agenzien kombinieren könnten, die diesen Fett‑Immunsignalweg aktivieren, um die Stoffwechselgesundheit sicherer und wirkungsvoller zu verbessern.
Zitation: A, M., Wang, G., Zammit, N.W. et al. Irisin ameliorates obesity and insulin resistance via adipose tissue IL-33 and regulatory T cells. Nat Metab 8, 885–901 (2026). https://doi.org/10.1038/s42255-026-01491-2
Schlüsselwörter: irisin, Fettgewebe, regulatorische T‑Zellen, IL-33, Thermogenese