Clear Sky Science · ja
糖尿病を伴う骨粗鬆症におけるNETs関連バイオマーカーの同定と検証
なぜ骨と血糖は同じ議題に上るべきか
寿命が延びるにつれ、骨を弱らせる骨粗鬆症と血糖を乱す糖尿病という二つの一般的だが別々に扱われがちな診断に直面する人が増えています。本研究はその二つの世界を結びつけ、単純だが重要な問いを投げかけます:なぜ糖尿病の人に骨が脆くなる人が多いのかを説明する共通の生物学的要因はあるのか。本研究は好中球のあまり知られていない防御機構に注目し、医師がこの危険な組み合わせを早期に見つけ、将来的には標的にできるような血中の警告信号を探します。
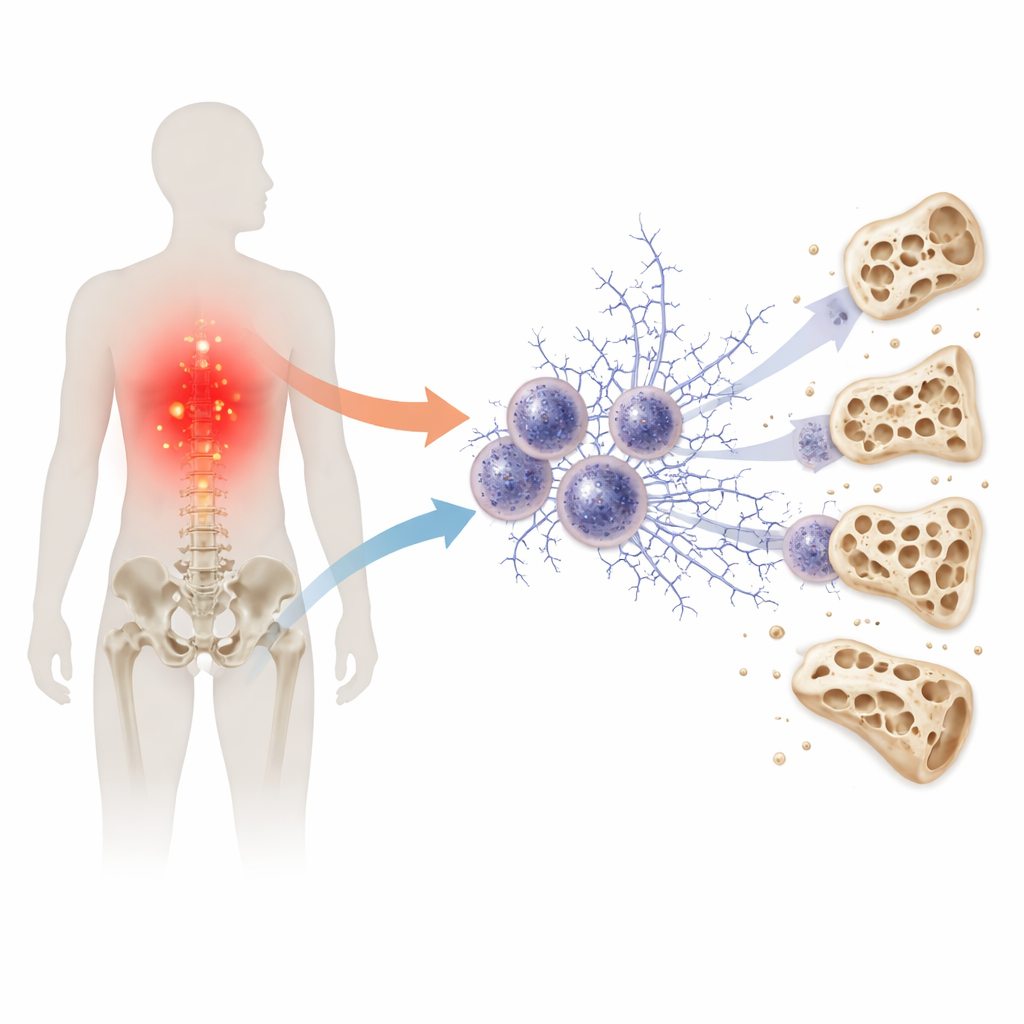
免疫系に潜む見えない網
病原体に対する最初の防衛線には、素早く移動する好中球が含まれます。好中球はDNAとタンパク質でできた粘着性の網を投げ出して侵入者を捕らえます。これらは細胞外トラップと呼ばれ、短期間では有益ですが、頻繁に現れたり長く残ったりすると害を及ぼすことがあります。これまでの研究はこうした免疫の網を腎臓や血管における糖尿病合併症と結びつけてきました。本研究は同じプロセスが糖尿病と骨の薄化を結びつけ、急性の防御反応が慢性的な損傷の原因になり得るかを問います。
血中の分子の手がかりを読む
この考えを検証するために、研究チームは骨粗鬆症と糖尿病の両方を持つ15人と健常ボランティア15人の血液サンプルの遺伝子発現を解析しました。彼らは好中球の網形成に関与すると既に知られている69遺伝子に焦点を当て、患者でどれがオン/オフに異なっているかを調べました。二種類の機械学習を含む高度な計算手法を用いて、2000以上の変動遺伝子から患者と健常者を最もよく区別する二つの有力候補に絞り込みました。
注目の二つの信号:S100A12とSLC25A37
注目された二つの遺伝子、S100A12とSLC25A37は炎症とエネルギー代謝が重要な役割を果たすことを示唆します。S100A12は免疫細胞が放出するタンパク質をコードし、炎症を増幅する作用があり、いくつかの糖尿病合併症で上昇することが既に知られています。SLC25A37は細胞内の小さな発電所であるミトコンドリアへ鉄を運ぶ役割を担い、細胞のエネルギー処理や酸化ストレスに影響を与えます。小規模な追跡群で、研究者らはこれらの遺伝子がコードするタンパク質を血中で測定し、遺伝子発現の変動が大きくても、糖尿病関連の骨量減少のある人では両者が明らかに高値であることを見いだしました。
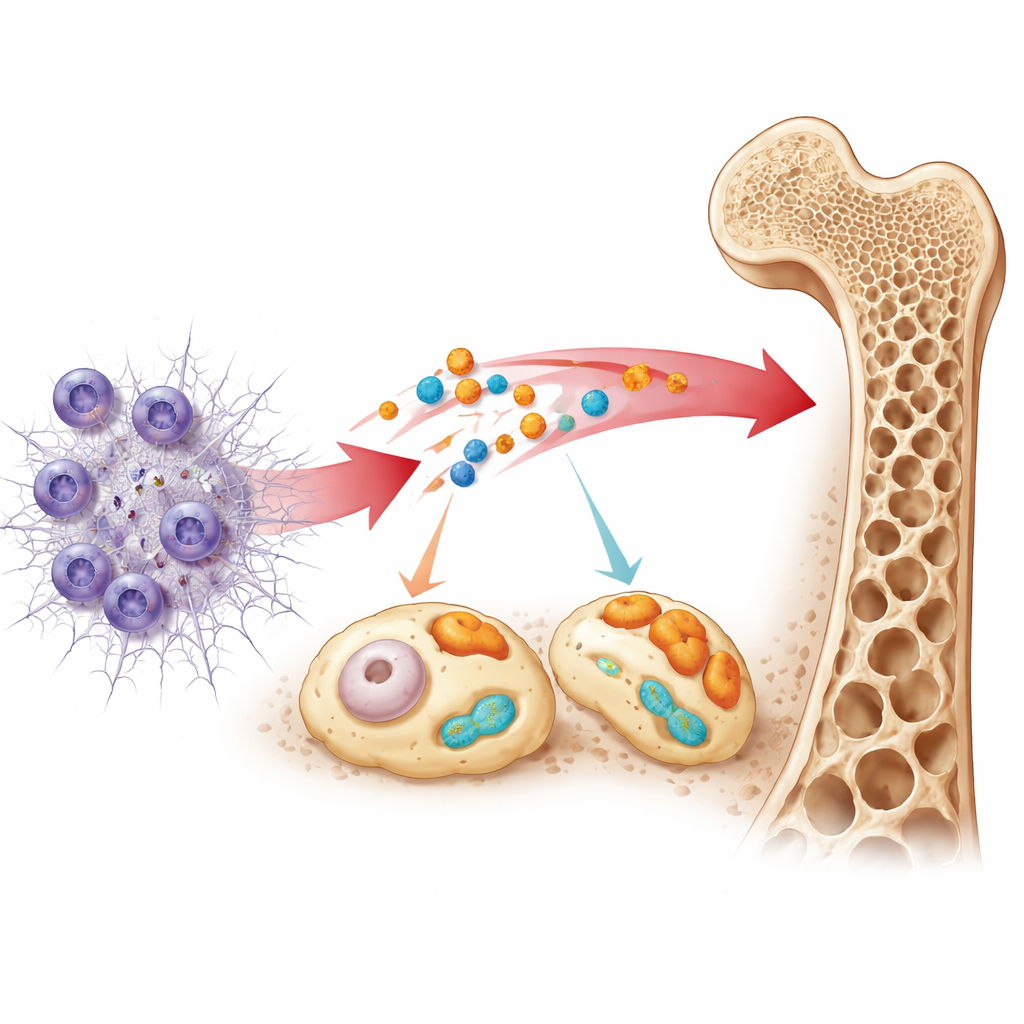
これらの信号が示す体の防御の様子
これら二つのマーカーに関連する生物学的経路をマッピングすることで、本研究はそれらが免疫反応、代謝、骨のリモデリングの交差点に位置することを示唆します。S100A12は糖によって損傷したタンパク質に応答する経路や骨の分解を促す信号系に結びついていました。SLC25A37はタンパク質合成や体内の危険を検知するセンサーに関連する経路と結びついていました。チームはまた、患者と健常ボランティアの間で好中球を中心にいくつかの免疫細胞のシフトを確認しました。最後に、医薬品データベースを掘り下げることで関連するシグナル系に作用する既存薬を特定し、将来の治療方向を示唆しましたが、これらはまだ仮説的な段階にとどまります。
患者にとって何を意味するか
総じて、これらの所見は高血糖、過活動化した免疫の網、細胞エネルギーの乱れが合わさって糖尿病の人の骨を弱くすることを示唆します。S100A12とSLC25A37はこのプロセスを示す有望な血中指標として浮かび上がり、有害な炎症を鎮める薬や神経・血管・骨間の健康なシグナルを回復する治療といった新たな治療の出発点となり得ます。本研究は小規模で初期段階の解析に大きく依存しているため、結果はより大きく多様な集団で確認される必要があり、これらのマーカーの役割は細胞や動物モデルで直接検証されねばなりません。それでも、この研究は免疫と代謝の複雑な絡まりを、糖尿病とともに生きる人々の骨折リスクを予測し最終的に減らすための実用的な手段に変える基盤を築いています。
引用: Zhang, L., Hao, L., Wang, Y. et al. Identification and validation of NETs-associated biomarkers in osteoporosis with diabetes. Sci Rep 16, 14074 (2026). https://doi.org/10.1038/s41598-026-44721-z
キーワード: 糖尿病性骨粗鬆症, 好中球細胞外トラップ, 骨の脆弱性, 炎症と代謝, バイオマーカー