Clear Sky Science · de
Identifikation und Validierung von NETs‑assoziierten Biomarkern bei Osteoporose mit Diabetes
Warum Knochen und Blutzucker zur gleichen Diskussion gehören
Da Menschen länger leben, stehen immer mehr von uns vor zwei häufigen, aber oft getrennt betrachteten Diagnosen: Osteoporose, die die Knochen schwächt, und Diabetes, der den Blutzucker stört. Diese Studie verknüpft diese Bereiche, indem sie eine einfache, aber wichtige Frage stellt: Gibt es einen gemeinsamen biologischen Faden, der erklärt, warum viele Menschen mit Diabetes auch brüchige Knochen haben? Indem die Forscher sich auf einen wenig bekannten Abwehrmechanismus der weißen Blutkörperchen konzentrieren, suchen sie nach Warnsignalen im Blut, die Ärzten eines Tages helfen könnten, diese gefährliche Kombination früher zu erkennen und vielleicht sogar gezielt anzugehen.
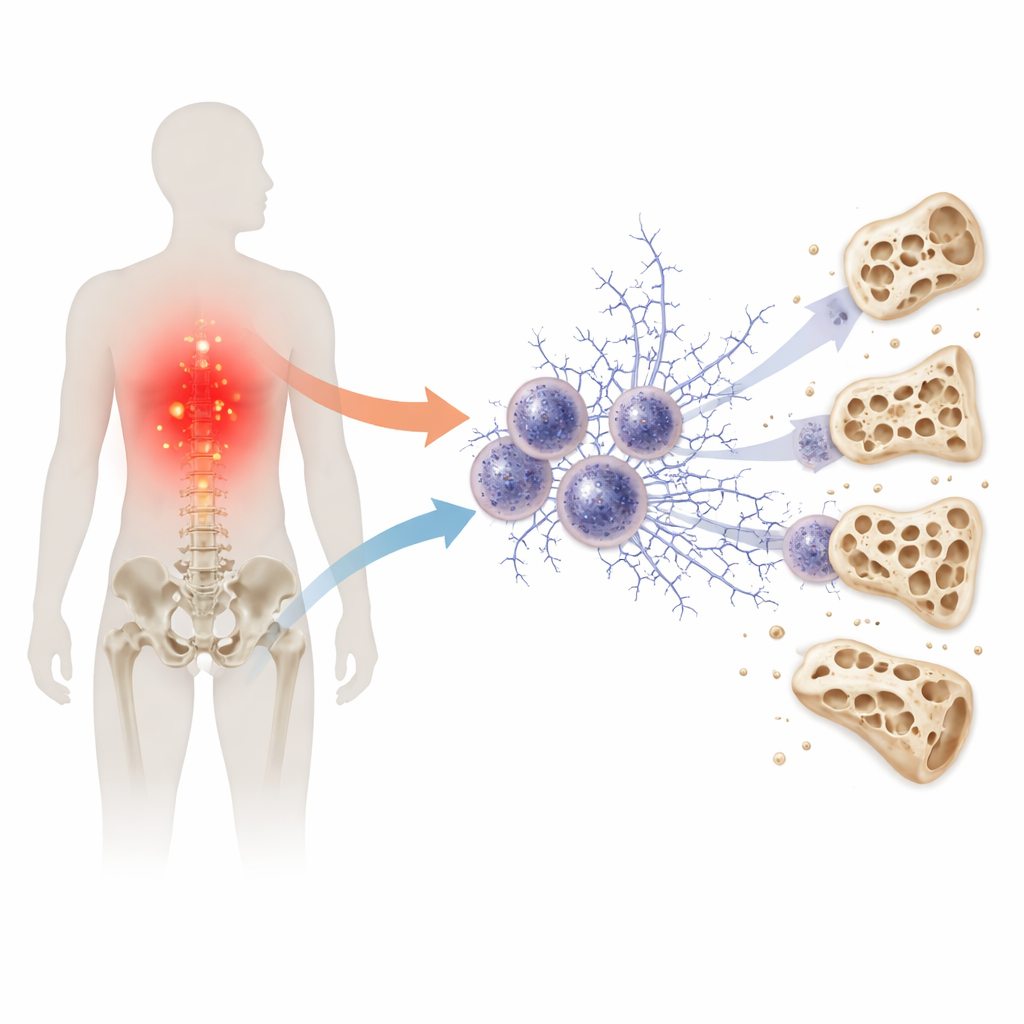
Ein verborgenes Netz im Immunsystem
Unsere erste Verteidigungslinie gegen Keime umfasst die Neutrophilen, schnell reagierende weiße Blutkörperchen, die klebrige Netze aus DNA und Proteinen auswerfen können, um Eindringlinge zu fangen. Diese Strukturen, sogenannte extrazelluläre Netze, sind in kurzen Episoden nützlich, können aber Schaden anrichten, wenn sie zu häufig auftreten oder zu lange bestehen bleiben. Frühere Arbeiten haben diese immunologischen Netze mit diabetischen Komplikationen in Nieren und Blutgefäßen in Verbindung gebracht. Die vorliegende Studie fragt, ob derselbe Prozess auch Diabetes mit dem Ausdünnen von Knochen verbinden könnte, wobei ein akuter Abwehrmechanismus zu einer chronischen Schadensquelle wird.
Molekulare Hinweise im Blut lesen
Um diese Idee zu untersuchen, analysierte das Team die Genaktivität in Blutproben von 15 Personen mit sowohl Osteoporose als auch Diabetes und 15 gesunden Freiwilligen. Sie konzentrierten sich auf 69 Gene, die bereits an der Bildung neutrophiler Netze beteiligt sind, und suchten danach, welche davon bei den Patienten anders ein- oder ausgeschaltet waren. Mit Hilfe fortgeschrittener Rechenmethoden, einschließlich zweier Arten von maschinellem Lernen, reduzierten sie mehr als zweitausend veränderte Gene auf nur zwei herausragende Kandidaten, deren Aktivitätsmuster Patienten am besten von gesunden Kontrollen unterschieden.
Zwei hervorgehobene Signale: S100A12 und SLC25A37
Die beiden hervorgehobenen Gene, S100A12 und SLC25A37, deuten auf Entzündung und Energiestoffwechsel als Schlüsselfaktoren hin. S100A12 codiert für ein von Immunzellen freigesetztes Protein, das Entzündungen verstärken kann und bereits bei mehreren diabetischen Komplikationen erhöht bekannt ist. SLC25A37 ist an der Einfuhr von Eisen in die winzigen Kraftwerke der Zelle, die Mitochondrien, beteiligt und beeinflusst, wie Zellen Energie und oxidativen Stress handhaben. In einer kleinen Folgegruppe maßen die Forscher die durch diese Gene kodierten Proteine im Blut und fanden, dass beide bei Menschen mit diabetesbedingtem Knochenabbau deutlich höher waren als bei gesunden Teilnehmern, selbst wenn die Genaktivitätswerte variabler waren.
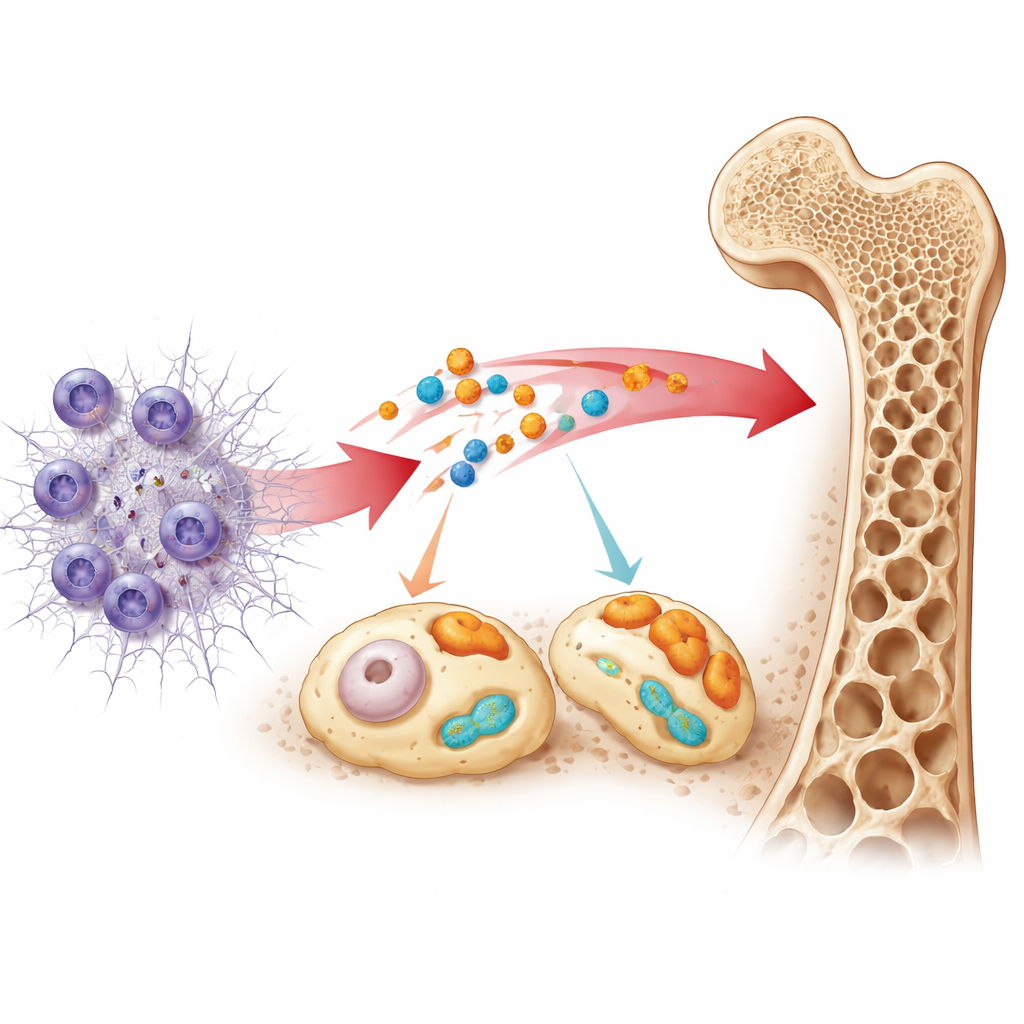
Was diese Signale über die Abwehr des Körpers aussagen
Indem sie kartierten, welche biologischen Signalwege mit diesen beiden Markern verknüpft sind, legt die Studie nahe, dass sie an Schnittstellen zwischen Immunreaktionen, Stoffwechsel und Knochenumbau sitzen. S100A12 war mit Wegen verbunden, die auf zuckerbedingte Proteinveränderungen reagieren, und mit Signalkaskaden, die den Knochenabbau fördern können. SLC25A37 war mit Wegen verknüpft, die die Proteinproduktion und Sensoren betreffen, die Gefahren im Körper detektieren. Das Team fand außerdem Verschiebungen in mehreren Typen von Immunzellen, insbesondere Neutrophilen, bei Patienten im Vergleich zu gesunden Freiwilligen. Schließlich identifizierten sie durch das Durchsuchen von Arzneimitteldatenbanken bereits existierende Medikamente, die auf verwandte Signalwege einwirken, was auf mögliche zukünftige Behandlungsansätze hinweist — diese Hinweise bleiben jedoch spekulativ.
Was das für Patienten bedeuten könnte
In der Summe deuten die Ergebnisse darauf hin, dass hoher Blutzucker, überaktive immunologische Netze und gestörte Zellenergie zusammenlaufen und bei Menschen mit Diabetes die Knochen schwächen. S100A12 und SLC25A37 tauchen als vielversprechende blutbasierte Indikatoren dieses Prozesses auf und als Ansatzpunkte für die Entwicklung neuer Therapien, etwa Medikamente, die schädliche Entzündungen dämpfen oder die gesunde Kommunikation zwischen Nerven, Blutgefäßen und Knochen wiederherstellen. Da es sich um eine kleine, frühe Studie handelt, die stark auf computerbasierte Analysen setzte, müssen die Ergebnisse in größeren und vielfältigeren Kohorten bestätigt und die Rollen dieser Marker direkt in Zell- und Tiermodellen geprüft werden. Dennoch legt die Arbeit eine Grundlage dafür, ein komplexes Geflecht aus immunologischen und metabolischen Veränderungen in praktische Werkzeuge zur Vorhersage und schließlich Verringerung des Frakturrisikos bei Menschen mit Diabetes zu übersetzen.
Zitation: Zhang, L., Hao, L., Wang, Y. et al. Identification and validation of NETs-associated biomarkers in osteoporosis with diabetes. Sci Rep 16, 14074 (2026). https://doi.org/10.1038/s41598-026-44721-z
Schlüsselwörter: diabetische Osteoporose, neutrophile extrazelluläre Netze, Knochenbrüchigkeit, Entzündung und Stoffwechsel, Biomarker