Clear Sky Science · fr
Identification et validation de biomarqueurs associés aux NETs dans l’ostéoporose liée au diabète
Pourquoi os et glycémie méritent la même conversation
À mesure que l’espérance de vie augmente, un nombre croissant de personnes cumulent deux diagnostics fréquents mais souvent traités séparément : l’ostéoporose, qui fragilise les os, et le diabète, qui perturbe la glycémie. Cette étude rassemble ces deux domaines en posant une question simple mais importante : existe‑t‑il un fil biologique commun qui explique pourquoi de nombreux diabétiques ont aussi des os fragiles ? En se concentrant sur un mécanisme de défense peu connu des globules blancs, les chercheurs cherchent des signaux d’alerte dans le sang qui pourraient un jour aider les médecins à repérer — et peut‑être cibler — plus tôt cette association dangereuse.
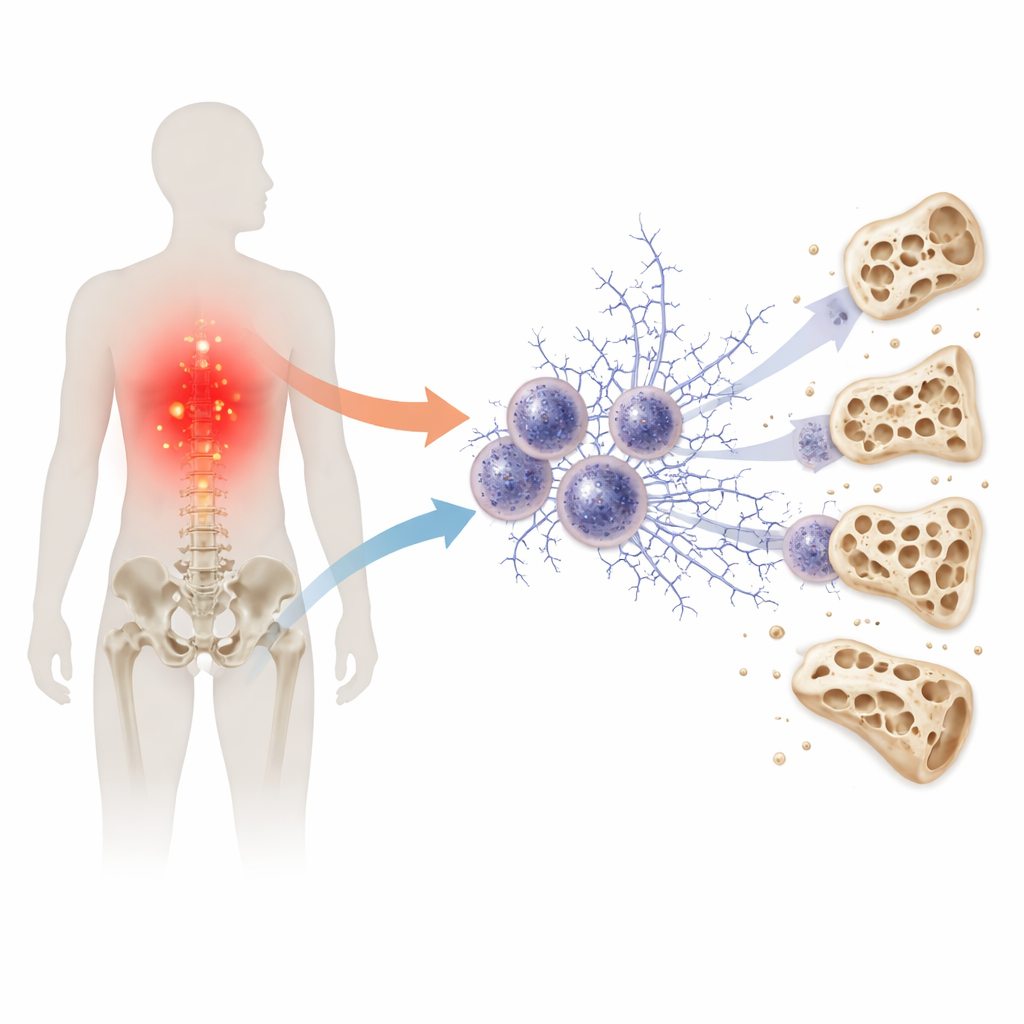
Une toile cachée dans le système immunitaire
Notre première ligne de défense contre les microbes comprend les neutrophiles, des globules blancs rapides qui peuvent déployer des toiles collantes composées d’ADN et de protéines pour piéger les envahisseurs. Ces structures, appelées filets extracellulaires, sont utiles à court terme mais peuvent devenir délétères si elles sont trop fréquentes ou persistent. Des travaux antérieurs ont lié ces toiles immunitaires à des complications diabétiques rénales et vasculaires. L’étude actuelle se demande si le même processus pourrait aussi relier le diabète à l’amincissement des os, transformant potentiellement une défense aiguë en une source chronique de dommages.
Lire des indices moléculaires dans le sang
Pour explorer cette idée, l’équipe a analysé l’activité génique dans des échantillons de sang de 15 personnes atteintes à la fois d’ostéoporose et de diabète et de 15 volontaires sains. Ils se sont concentrés sur 69 gènes déjà connus pour participer à la formation des filets neutrophiles, puis ont cherché lesquels étaient activés ou réprimés différemment chez les patients. En utilisant des méthodes informatiques avancées, y compris deux types d’apprentissage automatique, ils ont réduit plus de deux mille gènes altérés à seulement deux candidats marquants dont les profils d’activité distinguaient le mieux les patients des témoins sains.
Deux signaux marquants : S100A12 et SLC25A37
Les deux gènes mis en avant, S100A12 et SLC25A37, indiquent que l’inflammation et le métabolisme énergétique jouent un rôle central. S100A12 code une protéine libérée par les cellules immunitaires qui peut amplifier l’inflammation et dont les taux augmentent déjà dans plusieurs complications du diabète. SLC25A37 participe au transport du fer vers les petites centrales énergétiques des cellules, les mitochondries, influençant la gestion de l’énergie et le stress oxydatif. Dans un petit groupe de suivi, les chercheurs ont mesuré les protéines codées par ces gènes dans le sang et ont constaté que les deux étaient clairement plus élevées chez les personnes atteintes de perte osseuse liée au diabète que chez les participants sains, même lorsque les niveaux d’expression génique étaient plus variables.
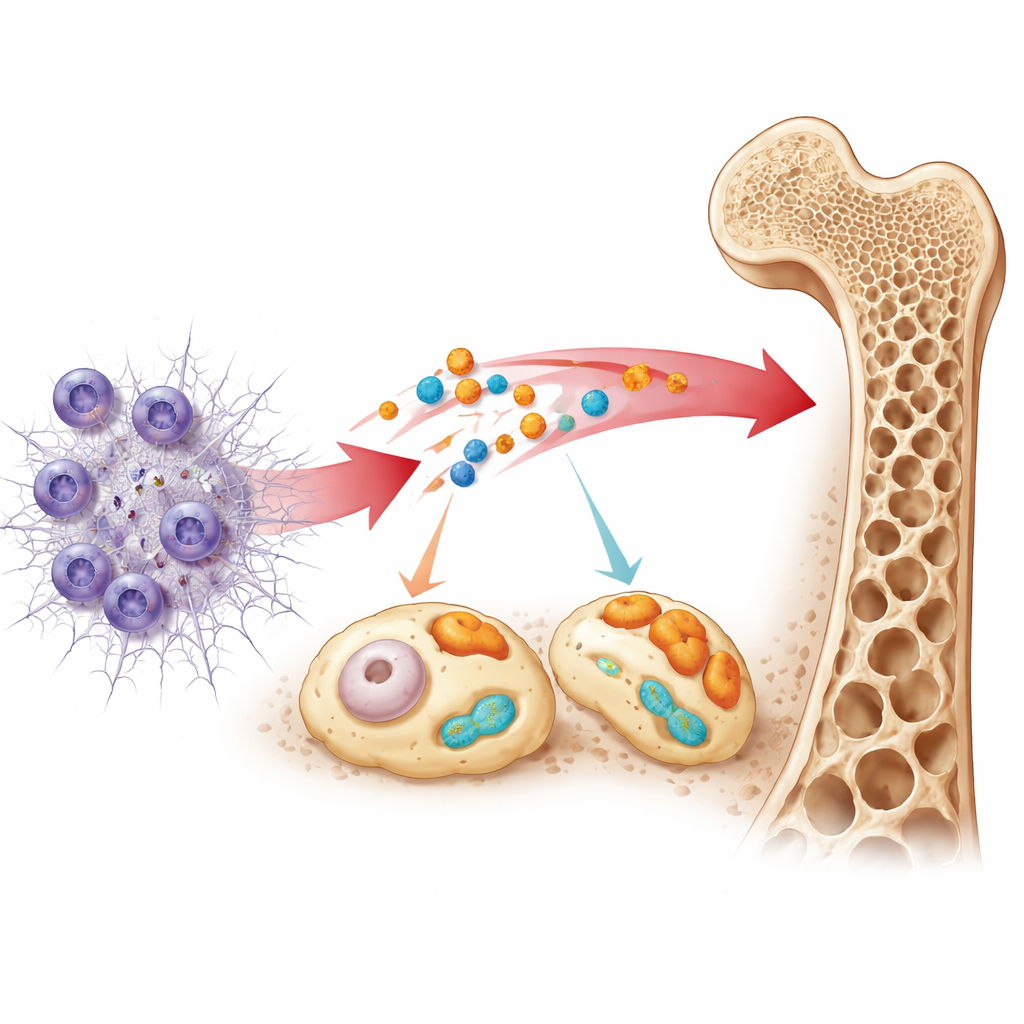
Ce que ces signaux révèlent des défenses de l’organisme
En cartographiant les voies biologiques associées à ces deux marqueurs, l’étude suggère qu’ils se situent à l’intersection des réactions immunitaires, du métabolisme et du remodelage osseux. S100A12 était lié à des voies répondant aux protéines endommagées par le sucre et à des systèmes de signalisation qui peuvent favoriser la résorption osseuse. SLC25A37 était associé à des voies impliquant la production protéique et des senseurs détectant le danger dans l’organisme. L’équipe a également observé des modifications de plusieurs types de cellules immunitaires, en particulier des neutrophiles, chez les patients par rapport aux volontaires sains. Enfin, en explorant des bases de données sur les médicaments, ils ont identifié des traitements existants agissant sur des systèmes de signalisation connexes, ouvrant la voie à des pistes thérapeutiques potentielles, bien que ces pistes restent pour l’instant spéculatives.
Ce que cela pourrait signifier pour les patients
Pris ensemble, les résultats suggèrent que l’hyperglycémie, la suractivité des filets immunitaires et la perturbation de l’énergie cellulaire convergent pour affaiblir l’os chez les personnes diabétiques. S100A12 et SLC25A37 émergent comme des indicateurs prometteurs mesurables dans le sang de ce processus et comme points de départ pour penser à de nouvelles thérapies, par exemple des médicaments qui calment l’inflammation nocive ou rétablissent une communication saine entre nerfs, vaisseaux et os. Comme il s’agit d’une étude pilote de petite taille reposant largement sur l’analyse informatique, ses résultats doivent être confirmés dans des cohortes plus larges et diversifiées, et les rôles de ces marqueurs doivent être testés directement dans des cellules et des modèles animaux. Néanmoins, ce travail jette les bases pour transformer un enchevêtrement complexe de changements immunitaires et métaboliques en outils pratiques pour prédire et, éventuellement, réduire le risque de fracture chez les personnes vivant avec le diabète.
Citation: Zhang, L., Hao, L., Wang, Y. et al. Identification and validation of NETs-associated biomarkers in osteoporosis with diabetes. Sci Rep 16, 14074 (2026). https://doi.org/10.1038/s41598-026-44721-z
Mots-clés: ostéoporose diabétique, filets extracellulaires des neutrophiles, fragilité osseuse, inflammation et métabolisme, biomarqueurs