Clear Sky Science · ja
ZDHHC9はLAMTOR1をパルミトイル化して腎細胞がんの悪性進行を促進する
この腎がん研究が重要な理由
腎細胞がんは一般的で命に関わることもある腎臓がんの一種で、しばしば既存薬に耐性を示し患者の治療選択肢が限られてしまいます。本研究は、がん細胞内に存在する見えにくい分子スイッチが増殖を促進し、一部の腫瘍が現行治療を回避する理由を説明している可能性を明らかにしました。このスイッチの所在を突き止めることで、腎腫瘍を弱め、既存薬の効果を高める新たな手段が示唆されます。
細胞内部にある増殖のスイッチ
がん細胞は分裂と拡散のために強力な内部増殖回路に依存しています。その主要な回路の一つがmTOR経路で、栄養やエネルギーを感知して細胞に成長すべきか静止すべきかを指示します。腎がんの半数以上でこの経路が異常に活性化しています。医師はラパマイシンなどのmTOR阻害薬を既に使用していますが、腫瘍はしばしば適応して増殖優位を取り戻します。著者らは、ZDHHC9と呼ばれるあまり知られていないタンパク質が、腎細胞がんでこの経路をオンに保つ隠れた制御因子の一つであるのではないかと考えました。
腎腫瘍で見つかった過剰に働く助っ人
研究者らはまず、腎がん患者の腫瘍サンプルと隣接する正常腎組織を比較しました。その結果、ZDHHC9の発現はRNAレベルとタンパク質レベルの両方で健康な細胞よりも一貫して高いことが分かりました。腎がん細胞株でZDHHC9を低下させると、細胞分裂が遅くなり、コロニー形成が減り、プログラムされた細胞死が増加しました。マウスでは、ZDHHC9を欠く細胞から作られた腫瘍は制御群よりも成長が遅く、重量も軽かったのです。これらの結果は、ZDHHC9が腎腫瘍の成長を加速する“アクセルペダル”のように働くことを示しています。
ZDHHC9が細胞の成長エンジンを高める仕組み
ZDHHC9は他のタンパク質に脂肪様の小さな分子を付加する酵素群に属しており、その化学修飾は標的タンパク質の細胞内での局在や相互作用を変え得ます。遺伝学的・生化学的検査を用いて、研究チームはZDHHC9がLAMTOR1という別のタンパク質に物理的に結合することを発見しました。LAMTOR1はリソソームの表面にある足場として働き、mTORシグナル伝達の調節に関与します。ZDHHC9はLAMTOR1の二つの特定の位置に脂肪基を付加し、これによってLAMTOR1がリソソームにより強く固定されます。その結果、mTOR複合体がその部位に集まりやすくなり活性化されやすくなるのです。
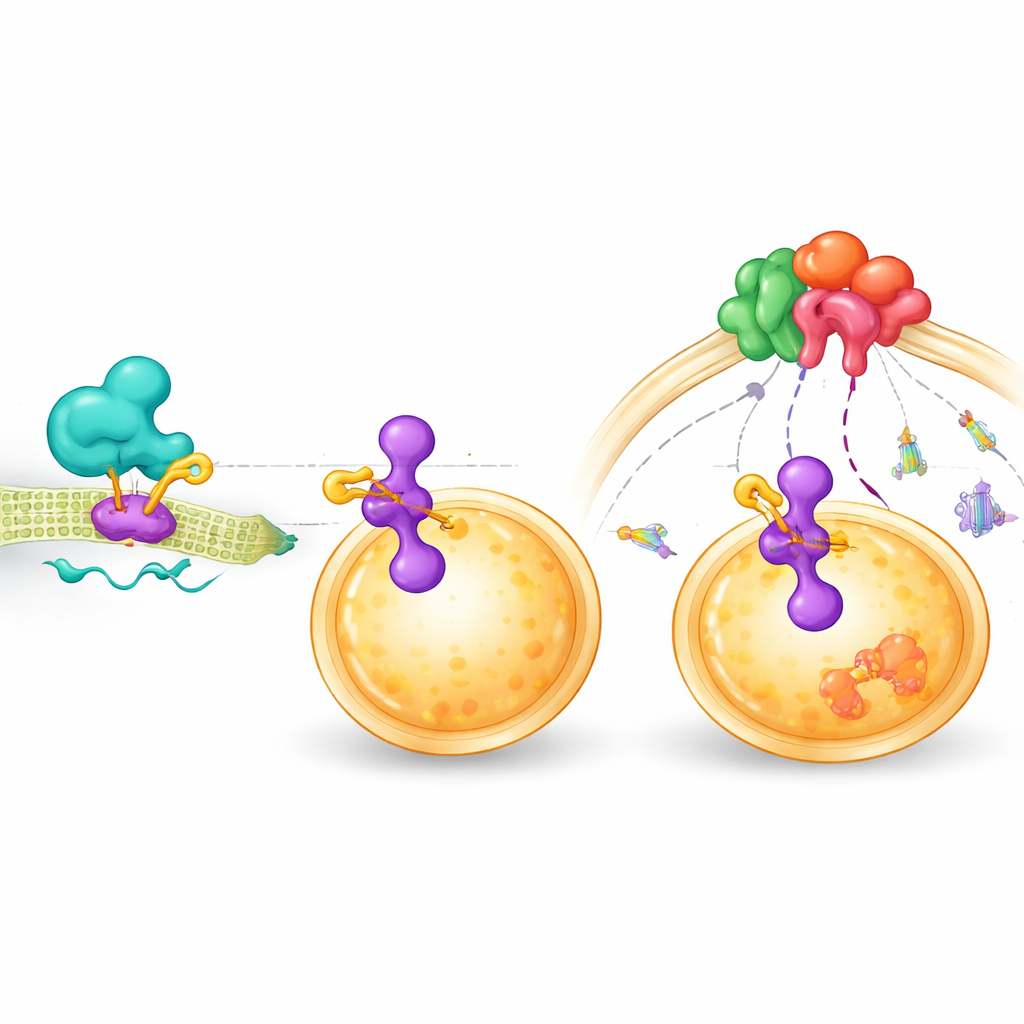
シグナルから腫瘍増殖への連鎖を断つ
研究者らがこの脂肪付加ステップを化学阻害剤で阻害したり、ZDHHC9の働く部位やLAMTOR1の重要部位を変異させたりすると、その連鎖反応は中断されました。リソソームに到達するmTORが減少し、下流の増殖シグナルが低下しました。この処置を受けた細胞は生存率が下がり、自己破壊の兆候が増えました。重要なことに、ZDHHC9を低下させると、ラパマイシンやAZD-8055といった標準的なmTOR阻害薬が細胞培養およびマウス腫瘍の両方でより効果的になりました。併用治療は単独治療よりも腫瘍増殖を強く抑え、がん組織における細胞死マーカーの増加を誘導しました。
将来の腎がん治療への意味
一般向けには、本研究は腎腫瘍が単一の誤作動スイッチによって駆動されるのではなく、成長エンジンを稼働させ続ける複数の助け手の連鎖によって支えられていることを示しています。ZDHHC9は隠れた技術者としてLAMTOR1を改変し、mTORの成長ハブが細胞内部の表面に固定され活性化された状態を維持させます。ZDHHC9を標的にすることで、この固定を緩め、腫瘍を既存のmTOR薬に対してより感受性の高い状態にし、病勢の進行を遅らせる可能性があります。本研究はまだ実験段階にありますが、将来的に腎細胞がん患者の治療を改善し得る有望な新規標的を示しています。
引用: Liu, B., Hou, T., Liu, X. et al. ZDHHC9 palmitoylates LAMTOR1 to promote renal cell carcinoma malignant progression. Cell Death Dis 17, 323 (2026). https://doi.org/10.1038/s41419-026-08558-8
キーワード: 腎細胞がん, mTORシグナル伝達, タンパク質のパルミトイル化, ZDHHC9, LAMTOR1