Clear Sky Science · ar
يزيل ZDHHC9 بالميتويلايت LAMTOR1 لتعزيز التقدّم الخبيث لسرطان الخلايا الكلوية
لماذا تهم هذه الدراسة عن سرطان الكلى
سرطان الخلايا الكلوية، وهو شكل شائع وغالبًا ما يكون قاتلاً من سرطان الكلى، يصبح في كثير من الأحيان مقاومًا للأدوية المتاحة، مما يترك المرضى مع خيارات قليلة. تكشف هذه الدراسة عن مفتاح جزيئي مخفي داخل الخلايا السرطانية يساعد في دفع نموها السريع وقد يفسر سبب تغلب بعض الأورام على العلاجات الحالية. من خلال تحديد هذا المفتاح، يوحي العمل بطريقة جديدة لإضعاف أورام الكلى وجعل الأدوية الحالية تعمل بشكل أفضل.
مفتاح نمو عميق داخل الخلية
تعتمد الخلايا السرطانية على دوائر نمو داخلية قوية للانقسام والانتشار. إحدى الدوائر الرئيسية هي مسار mTOR، الذي يستشعر المغذيات والطاقة ثم يقرر ما إذا كانت الخلايا ستنمو أم تبقى خاملة. في أكثر من نصف سرطانات الكلى، يكون هذا المسار نشطًا بشكل غير طبيعي. يستخدم الأطباء بالفعل أدوية تثبط mTOR مثل الراباميسين، لكن الأورام غالبًا ما تتكيف وتستعيد ميزة النمو الخاصة بها. افترض الباحثون أن بروتينًا أقل شهرة يُدعى ZDHHC9 قد يكون واحدًا من المتحكمين الخفيين الذين يبقون هذا المسار مفعلاً في سرطان الخلايا الكلوية.
اكتشاف مساعد مفرط النشاط في أورام الكلى
قارن الباحثون أولًا عينات الأورام من مرضى سرطان الكلى مع نسيج الكلى السليم المجاور. وجدوا أن مستويات ZDHHC9 كانت أعلى باستمرار في الخلايا السرطانية مقارنة بالخلايا السليمة، على مستوى الرنا والبروتين على حد سواء. عندما خفضوا ZDHHC9 في خطوط خلايا سرطان الكلى، انقسمت الخلايا بشكل أبطأ، تكونت مستعمرات أقل، وخاضت مزيدًا من الموت المبرمج. في الفئران، نمت الأورام المبنية من خلايا تفتقد ZDHHC9 بشكل أبطأ ووزنت أقل من أورام التحكم. مجتمعة، تظهر هذه النتائج أن ZDHHC9 يتصرف مثل "دواسة تسريع" لنمو ورم الكلى.
كيف يعزز ZDHHC9 محرك نمو الخلية
ينتمي ZDHHC9 إلى عائلة من الإنزيمات التي تضيف مجموعات دهنية صغيرة إلى بروتينات أخرى، وهو تعديل كيميائي يمكن أن يغير موضع هذه البروتينات داخل الخلية وكيفية تفاعلها. باستخدام اختبارات وراثية وكيميائية حيوية، اكتشف الفريق أن ZDHHC9 يرتبط فعليًا ببروتين آخر يدعى LAMTOR1، الذي يعمل كمنصة رست على سطح الليسوسومات — مقصورات صغيرة تساعد في تنسيق إشارة mTOR. يضيف ZDHHC9 مجموعات دهنية إلى موضعين محددين على LAMTOR1، مما يرسخ LAMTOR1 بقوة أكبر عند الليسوسوم. وهذا بدوره يجعل من الأسهل لتجمع مركب mTOR أن يتجمع في ذلك الموقع ويُفَعَّل.
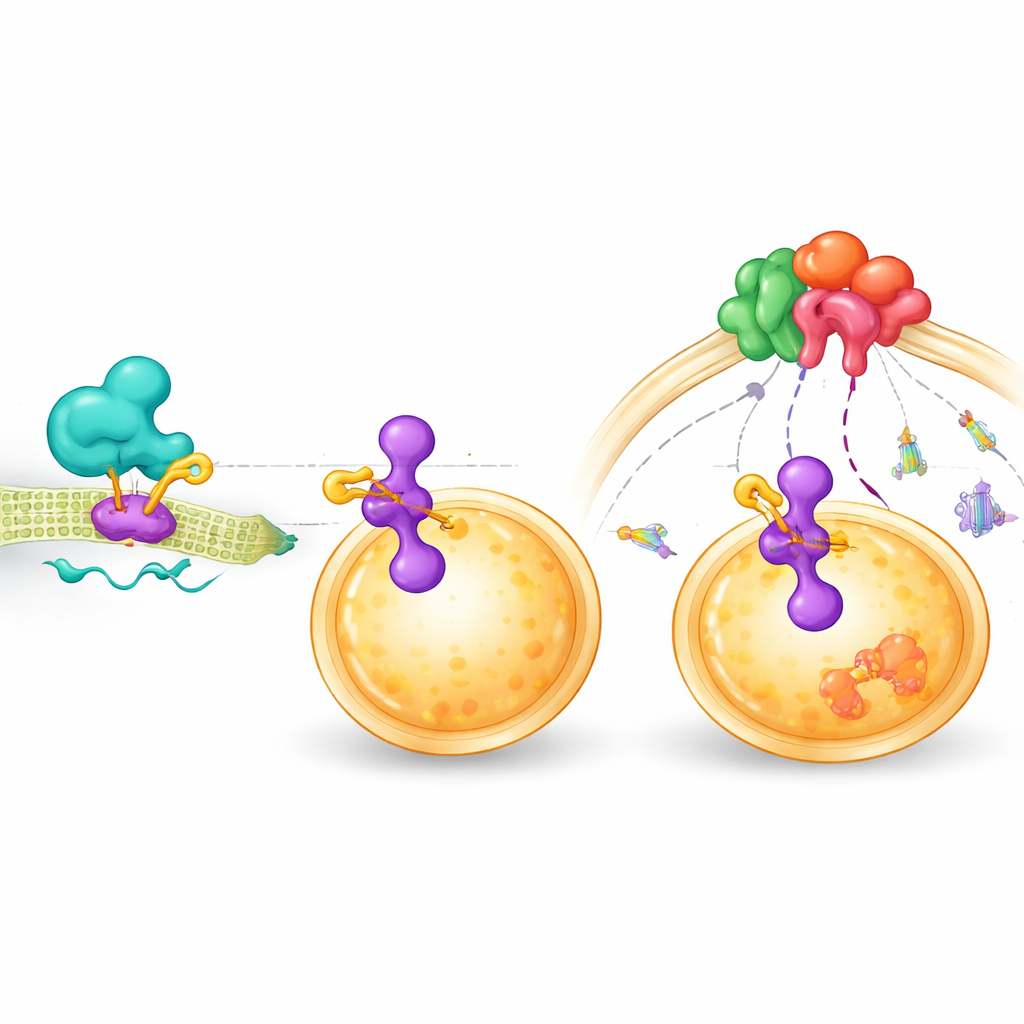
إيقاف السلسلة من الإشارة إلى نمو الورم
عندما أعاق الباحثون هذه الخطوة المضافة للدهن بمثبط كيماوي، أو عندما عدلوا موقع عمل ZDHHC9 أو المواقع الأساسية على LAMTOR1، انقطعت سلسلة التفاعلات. وصل مقدار أقل من mTOR إلى الليسوسوم، وتراجعت إشارات النمو المتتابعة downstream. أظهرت الخلايا المعالجة بهذه الطريقة بقاءً أقل وعلامات أكثر على الانتحار الخلوي. ومن المهم أنه عندما خُفضت مستويات ZDHHC9، أصبحت أدوية تثبيط mTOR القياسية مثل الراباميسين وAZD-8055 أكثر فعالية، سواء في المستنبتات الخلوية أو في أورام الفئران. أبطأت المعالجة المجمعة نمو الورم أكثر من أي نهج منفرد وأدت إلى مستويات أعلى من علامات موت الخلايا في النسيج السرطاني.
ما معنى ذلك لعلاج سرطان الكلى في المستقبل
للشخص العادي، توضح الدراسة أن أورام الكلى لا يُشغّلها مفتاح واحد معطوب، بل سلسلة من المساعدين الذين يبقون محرك النمو يعمل. يعمل ZDHHC9 كتقني مخفي، يعدل LAMTOR1 بحيث يُحكم تثبيت محور نمو mTOR على السطح الداخلي للخلية ويظل نشطًا. من خلال استهداف ZDHHC9، قد يكون بإمكان الأطباء تخفيف هذا التثبيت، مما يجعل الأورام أكثر حساسية لأدوية mTOR الحالية ويبطئ تقدم المرض. وعلى الرغم من أن هذا العمل لا يزال في مرحلة تجريبية، فإنه يسلط الضوء على هدف واعد قد يحسّن يومًا ما علاج المرضى المصابين بسرطان الخلايا الكلوية.
الاستشهاد: Liu, B., Hou, T., Liu, X. et al. ZDHHC9 palmitoylates LAMTOR1 to promote renal cell carcinoma malignant progression. Cell Death Dis 17, 323 (2026). https://doi.org/10.1038/s41419-026-08558-8
الكلمات المفتاحية: سرطان الخلايا الكلوية, إشارة mTOR, البيميويتويلايت البروتيني, ZDHHC9, LAMTOR1