Clear Sky Science · ja
コルチゾール耐性CAR-NK細胞は肺がんにおけるステロイド誘導免疫抑制を克服する
なぜストレスホルモンが肺がんで重要か
肺腫瘍は単に増殖するだけでなく、体の防御をかわすために周囲の環境を再構築します。本研究は、肺がんが体の主要なストレスホルモンであるコルチゾールに富む局所環境を作り出し、がんに対する前線の免疫力であるナチュラルキラー(NK)細胞を弱めていることを示します。研究者らはさらに、コルチゾールの抑制シグナルを無視できる新しいタイプの免疫細胞療法を設計し、患者がステロイド薬を必要とする状況でも肺腫瘍を攻撃する能力を回復させました。
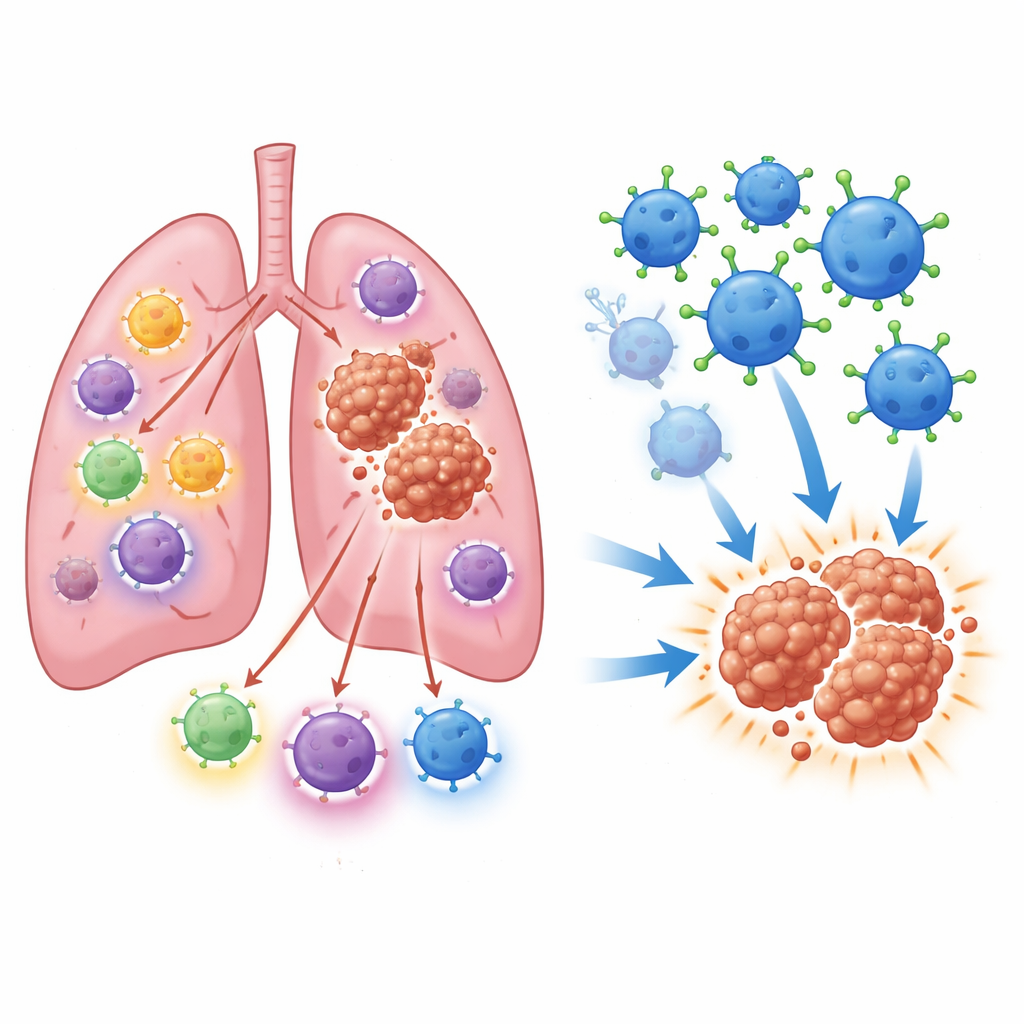
腫瘍の周りに隠れたホルモンの雲
研究チームはまず、人の肺腫瘍組織片で多数のステロイド分子を注意深く測定しました。その結果、コルチゾールがこれらの腫瘍内で最も豊富なステロイドであり、他のホルモンと比べて驚くほど高いレベルで存在していることがわかりました。数千の細胞を対象とした単一細胞遺伝子マッピングを用いて、複数の細胞型がこのホルモンに富むニッチの形成に寄与していることを突き止めました。免疫細胞、がん細胞、支持細胞はコレステロールからステロイド前駆体を作ることができ、特定の線維芽細胞やマクロファージは不活性なコルチゾンを再び活性なコルチゾールに変換する能力に優れていました。こうして、免疫細胞が戦おうとするまさにその場所で、持続的な局所的コルチゾール供給が生み出されているのです。
コルチゾールがナチュラルキラーを沈黙させる仕組み
ナチュラルキラー細胞は、異常な細胞を迅速に認識して破壊するよう設計されており、多くのがん細胞を含みます。しかし肺腫瘍内では、NK細胞はしばしば枯渇し効果を失ったように見えます。ヒトNK細胞をコルチゾールにさらし、遺伝子発現の変化を調べたところ、コルチゾールはこれらの細胞を鈍く攻撃性の低い状態へと押しやることが示されました。細胞殺傷や移動に関連する重要な遺伝子は抑制され、一方で抑制やストレスに関連する遺伝子は活性化されました。肺腫瘍から直接採取したNK細胞を調べると、コルチゾール受容体を多く持つ細胞は攻撃プログラムが弱く、機能障害や低酸素(酸素不足)ストレスの署名が強いことが示されました。肺がんにおける多くの免疫および支持細胞型で、より高いコルチゾール反応は強い低酸素シグナルと一致しており、ストレスホルモンと酸素欠乏が協調して免疫を鈍らせていることを示唆しています。
ホルモンシグナルを遮断すると免疫が再活性化する
コルチゾールのシグナルを断つことで腫瘍への攻撃力が回復するかを確かめるため、研究者らは肺がんのマウスモデルを用い、コルチゾール受容体(グルココルチコイド受容体)を阻害する薬剤で治療しました。この阻害剤を投与されたマウスは未処置の動物よりも小さな腫瘍を示しました。腫瘍に浸潤したNK細胞はより多くの殺傷分子と活性化マーカーを産生し、抑制受容体や低酸素ストレスのマーカーは減少しました。腫瘍内のT細胞もより活性化されましたが、脾臓の免疫細胞は大きな変化を示さず、薬剤が全身的な免疫活性化を引き起こすのではなく主に腫瘍微小環境内の抑制を解除したことを示唆しました。肺転移モデルでも、受容体の遮断は同様に肺内の腫瘍斑の数とサイズを減少させました。
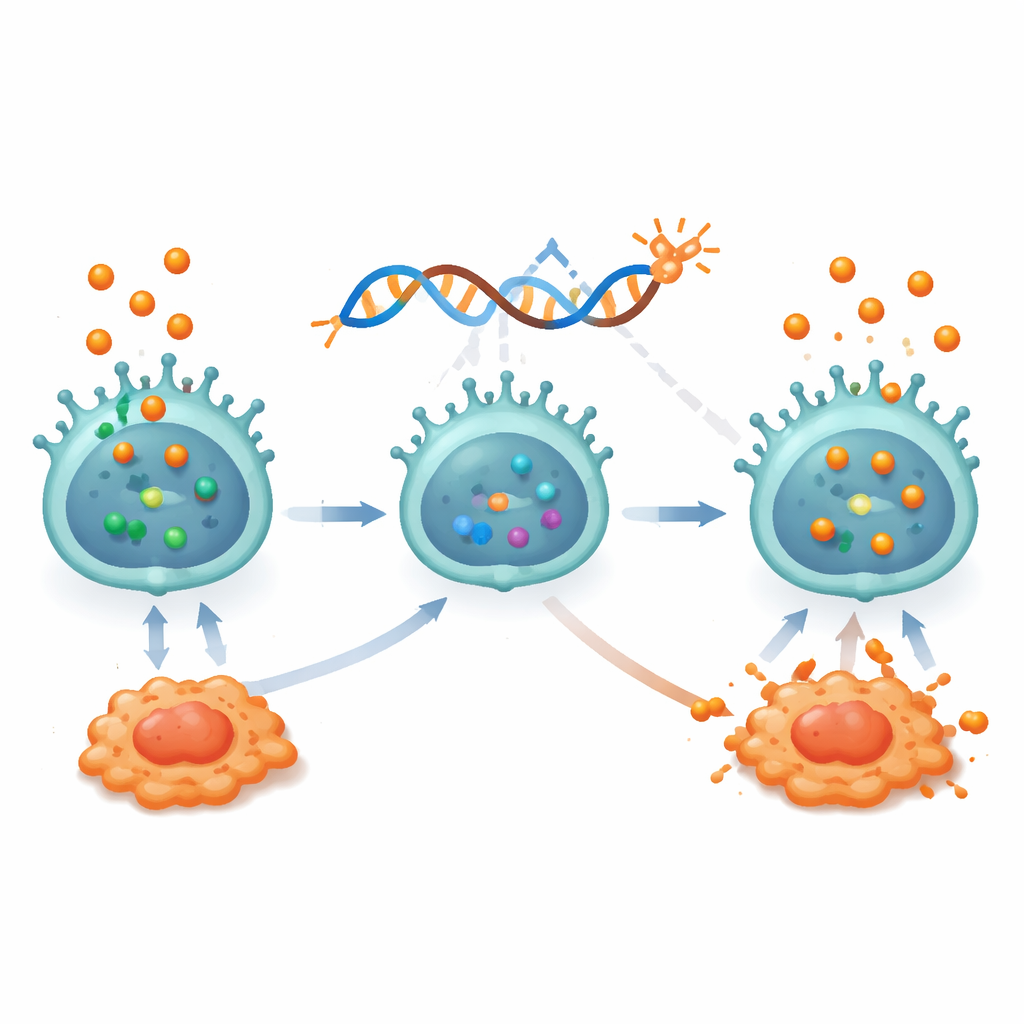
コルチゾール耐性のがん殺傷細胞の設計
これらの知見に基づき、研究者らはステロイドに富む環境で機能できる免疫療法を設計しました。彼らはCEACAM5を認識するキメラ抗原受容体(CAR)を持つNK細胞を作製しました。CEACAM5は肺がん細胞で高発現することが多いタンパク質です。これらのCAR-NK細胞はin vitroでCEACAM5陽性の肺がん細胞株を効果的に殺しましたが、コルチゾールを加えるとその能力は急激に低下しました:腫瘍細胞の殺傷数は減り、有益なサイトカインの産生も減少し、枯渇マーカーが出現しました。これを克服するためにチームは遺伝子編集技術を用いてコルチゾール受容体NR3C1の遺伝子を削除し、コルチゾール耐性のCAR-NK細胞を作製しました。改変されたこれらの細胞は、コルチゾールにさらされたり低酸素様条件に置かれても強い殺傷能を保ち、活性化状態を維持し枯渇を回避しました。経路解析では、標準的なCAR-NK細胞とは異なり、編集細胞はNK細胞の活性化と生存を駆動するPI3K–AKTやNF-κBなどの重要な内部シグナル経路を保持していることが示されました。
ステロイドに富む肺でのより強い腫瘍制御
最後に、研究者らは人肺がんの肺転移を持つマウスに標準型とコルチゾール耐性のCAR-NK細胞を投与して比較しました。臨床の実情を模倣するため、すべてのマウスには合成ステロイド薬も投与し、症状管理のためにグルココルチコイドを必要とする患者の状況を再現しました。この条件下で、堅牢かつ持続的な腫瘍制御を達成したのはコルチゾール耐性CAR-NK細胞のみであり、画像診断および組織学的検査により、通常のCAR-NK細胞を投与した動物より腫瘍は小さく広がりも少ないことが示されました。重要なことに、改変細胞は目立った組織損傷や血中での高い炎症性サイトカインを誘発せず、安全性プロファイルは良好であることが示唆されました。
今後のがん治療への示唆
本研究は、局所的なコルチゾールシグナルが肺がんにおける免疫攻撃の主要な、これまで過小評価されていた障害であることを明らかにします。肺腫瘍はホルモンの産生と再活性化の両方を利用し、コルチゾールに富む低酸素のニッチを維持してNK細胞の殺傷力を奪います。CAR-NK細胞からコルチゾール受容体を取り除くことで、研究者らはステロイドが存在し環境が過酷な状況でも活性を保つ免疫療法を作り出しました。将来的には、このようなコルチゾール耐性の細胞療法により、命を救う免疫療法と必要なステロイド治療を併用できるようになり、肺がんや他のステロイドを産生する固形腫瘍の患者の転帰改善につながる可能性があります。
引用: Chakraborty, S., Pramanik, J., Alviter-Raymundo, G. et al. Cortisol-resistant CAR-NK cells overcome steroid-induced immunosuppression in lung cancer. Sig Transduct Target Ther 11, 128 (2026). https://doi.org/10.1038/s41392-026-02638-z
キーワード: 肺がん免疫療法, ナチュラルキラー細胞, コルチゾールと腫瘍, CAR-NK細胞療法, 腫瘍微小環境