Clear Sky Science · es
Las células CAR-NK resistentes al cortisol superan la inmunosupresión inducida por esteroides en el cáncer de pulmón
Por qué importan las hormonas del estrés en el cáncer de pulmón
Los tumores pulmonares no solo crecen por sí mismos; también remodelan su entorno para mantener a raya las defensas del organismo. Este estudio revela que los cánceres de pulmón crean un nicho rico en cortisol—la principal hormona del estrés—que debilita a las células asesinas naturales (NK), una fuerza inmunitaria de primera línea contra el cáncer. Los investigadores diseñaron luego un nuevo tipo de terapia celular inmunitaria capaz de ignorar las señales de freno del cortisol, restaurando su capacidad de atacar los tumores pulmonares incluso cuando los pacientes necesitan fármacos esteroideos.
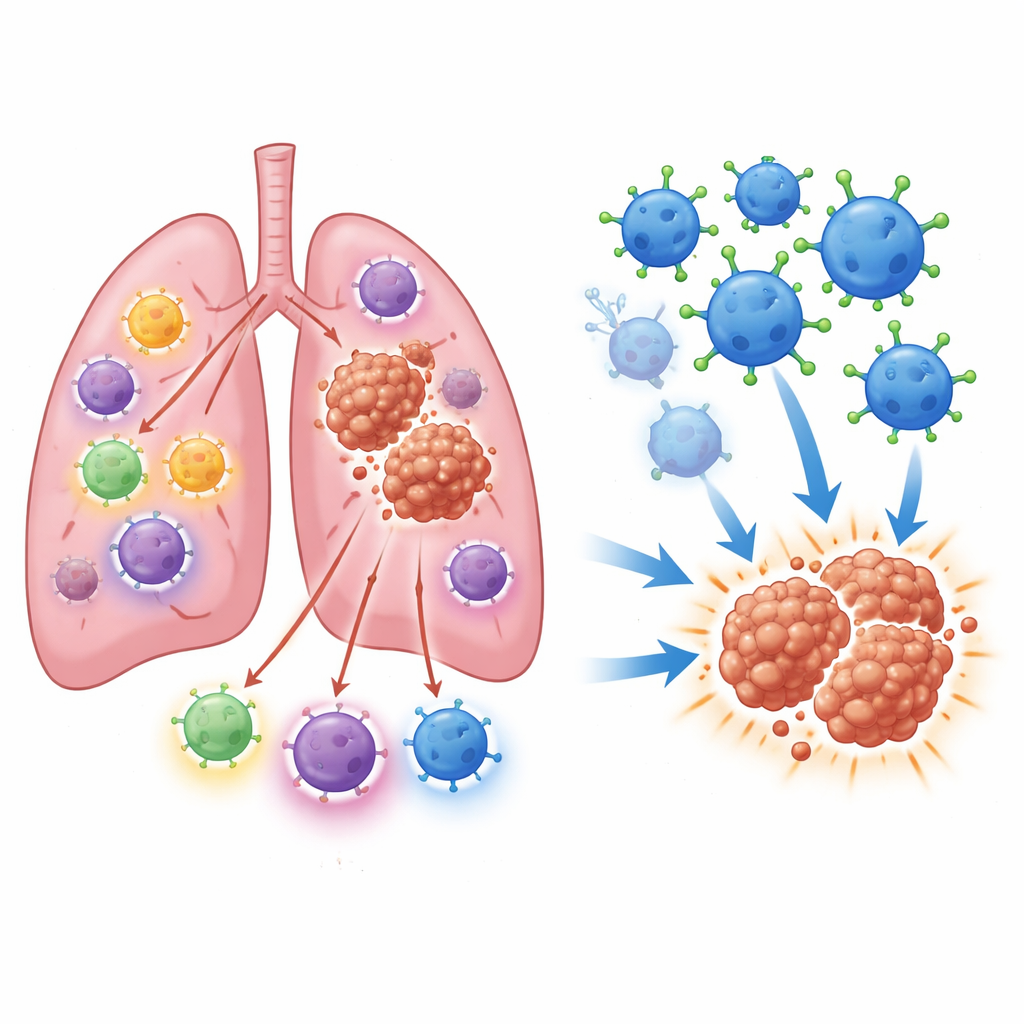
Una nube hormonal oculta alrededor de los tumores
El equipo comenzó midiendo con detalle muchas moléculas esteroideas distintas en fragmentos de tumores pulmonares humanos. Encontraron que el cortisol era el esteroide más abundante dentro de estos tumores, presente en niveles sorprendentemente altos en comparación con otras hormonas. Usando mapas genéticos de una sola célula de miles de células de cáncer de pulmón, descubrieron que varios tipos celulares contribuyen a construir este nicho rico en hormonas. Células inmunitarias, células cancerosas y células de sostén dentro del tumor pueden fabricar precursores esteroideos a partir del colesterol, mientras que ciertos fibroblastos y macrófagos son especialmente eficaces en convertir la cortisona inactiva de nuevo en cortisol activo. En conjunto, crean un suministro local continuo de esta potente hormona del estrés justo donde las células inmunitarias intentan combatir.
Cómo el cortisol silencia a las células asesinas naturales
Las células asesinas naturales están diseñadas para reconocer y destruir rápidamente células anormales, incluidas muchas células cancerosas. Sin embargo, dentro de los tumores pulmonares, las NK suelen parecer agotadas e ineficaces. Al exponer NK humanas al cortisol y estudiar los cambios en la actividad génica, los investigadores mostraron que el cortisol empuja a estas células hacia un estado más lento y menos agresivo. Genes importantes relacionados con la capacidad de matar y la movilidad se redujeron, mientras que aumentaron genes vinculados a la inhibición y al estrés. Cuando examinaron NK obtenidas directamente de tumores pulmonares, las que mostraban mayores niveles del receptor de cortisol presentaban programas de ataque más débiles y firmas más fuertes de “disfunción” e hipoxia (estrés por bajo oxígeno). A lo largo de muchos tipos celulares inmunitarios y de sostén en el cáncer de pulmón, mayores respuestas al cortisol iban de la mano con señales de hipoxia más intensas, lo que sugiere que la hormona del estrés y la privación de oxígeno actúan conjuntamente para debilitar la inmunidad.
Bloquear la señal hormonal reaviva la inmunidad
Para probar si cortar la señalización del cortisol podía restaurar la capacidad de combatir tumores, los científicos usaron modelos de ratón de cáncer de pulmón y los trataron con un fármaco que bloquea el receptor del cortisol, conocido como receptor de glucocorticoides. Los ratones que recibieron este bloqueador desarrollaron tumores más pequeños que los animales no tratados. Sus NK infiltrantes en el tumor produjeron más moléculas de muerte y marcadores de activación, mientras que los receptores inhibidores y los marcadores de estrés por hipoxia disminuyeron. Las células T dentro de los tumores también fueron más activas, pero las células inmunitarias del bazo permanecieron en gran medida sin cambios, lo que indica que el fármaco levantó principalmente la supresión dentro del microambiente tumoral en lugar de desencadenar una activación inmune generalizada. En un modelo de metástasis pulmonar, bloquear el receptor redujo de forma similar el número y tamaño de las lesiones tumorales en los pulmones.
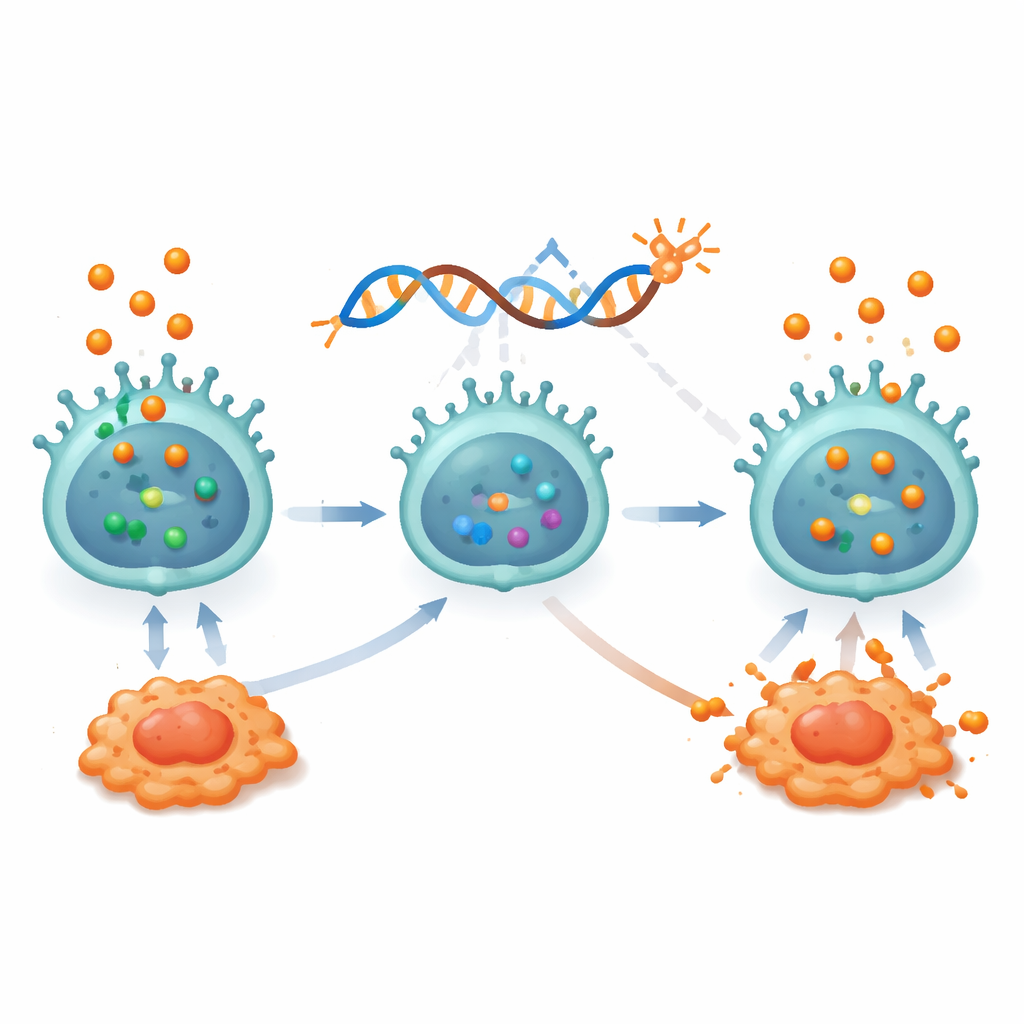
Diseñando células asesinas resistentes al cortisol
Partiendo de estas conclusiones, los investigadores diseñaron una forma de inmunoterapia capaz de prosperar en un entorno rico en esteroides. Crearon células NK portadoras de un receptor quimérico de antígeno (CAR) que reconoce CEACAM5, una proteína frecuentemente presente en altos niveles en células de cáncer de pulmón. Estas CAR-NK mataron eficazmente líneas de cáncer de pulmón positivas para CEACAM5 en el laboratorio, pero su rendimiento cayó drásticamente cuando se añadió cortisol: mataron menos células tumorales, produjeron menos citocinas útiles y empezaron a mostrar marcadores de agotamiento. Para superar esto, el equipo empleó herramientas de edición génica para eliminar el gen del receptor de cortisol, NR3C1, creando CAR-NK resistentes al cortisol. Estas células modificadas mantuvieron una fuerte capacidad de destrucción, permanecieron activadas y evitaron el agotamiento incluso cuando estaban expuestas a cortisol o sometidas a condiciones similares a la hipoxia. Análisis detallados de vías mostraron que, a diferencia de las CAR-NK estándar, las células editadas preservaron rutas de señalización interna clave—especialmente PI3K–AKT y NF-κB—que impulsan la activación y supervivencia de las NK.
Mejor control tumoral en pulmones ricos en esteroides
Finalmente, los investigadores probaron tanto CAR-NK estándar como resistentes al cortisol en ratones con metástasis pulmonares de cáncer de pulmón humano. Para imitar la práctica clínica real, todos los ratones también recibieron un fármaco esteroideo sintético, modelando la situación de pacientes que necesitan glucocorticoides para el control de síntomas. En estas condiciones, solo las CAR-NK resistentes al cortisol lograron un control tumoral sólido y duradero, como mostraron imágenes y examen tisular; los tumores eran más pequeños y menos extendidos que en animales tratados con CAR-NK regulares. Es importante que las células diseñadas no causaron daño tisular notable ni niveles altos de citocinas inflamatorias en sangre, lo que sugiere un perfil de seguridad favorable.
Qué significa esto para la atención del cáncer en el futuro
Este trabajo identifica la señalización local del cortisol como una barrera importante y hasta ahora subestimada para el ataque inmunitario en el cáncer de pulmón. Los tumores pulmonares explotan tanto la producción como el reciclaje hormonal para mantener un nicho rico en cortisol y con bajo oxígeno que agota a las NK de su poder citotóxico. Al eliminar el receptor de cortisol de las CAR-NK, los investigadores crearon una terapia inmunitaria que permanece activa incluso cuando están presentes esteroides y el entorno tumoral es hostil. En el futuro, esas terapias celulares resistentes al cortisol podrían permitir a los médicos combinar inmunoterapia que salva vidas con tratamientos esteroideos necesarios, mejorando potencialmente los resultados en pacientes con tumores sólidos productores de esteroides, incluidos los de pulmón.
Cita: Chakraborty, S., Pramanik, J., Alviter-Raymundo, G. et al. Cortisol-resistant CAR-NK cells overcome steroid-induced immunosuppression in lung cancer. Sig Transduct Target Ther 11, 128 (2026). https://doi.org/10.1038/s41392-026-02638-z
Palabras clave: inmunoterapia del cáncer de pulmón, células asesinas naturales, cortisol y tumores, terapia con células CAR-NK, microambiente tumoral