Clear Sky Science · it
Recupero ecologico del vanadio da catalizzatori esausti della produzione di acido solforico
Trasformare un rifiuto industriale in una risorsa
Ogni anno, le fabbriche che producono acido solforico scartano migliaia di tonnellate di catalizzatore usato—pellet solidi che una volta agevolavano le reazioni chimiche nelle loro torri. Questi materiali di scarto sono ricchi di vanadio, un metallo prezioso per l’industria ma dannoso se rilasciato nell’aria, nel suolo e nelle acque. Questo studio esplora un metodo per recuperare il vanadio da quel rifiuto usando un acido relativamente delicato, di origine vegetale, trasformando un sottoprodotto pericoloso in una materia prima utile e riducendo la pressione sull’ambiente.
Perché il vanadio e l’acido solforico sono importanti
L’acido solforico è uno dei prodotti chimici più prodotti al mondo, impiegato in fertilizzanti, raffinazione dei carburanti, esplosivi, coloranti e batterie per auto. La sua produzione comporta la conversione dell’anidride solforosa in anidride solforica con l’aiuto di un catalizzatore a base di vanadio. Col tempo i granuli di catalizzatore perdono efficacia e vengono sostituiti, generando circa 40.000 tonnellate di materiale esausto a livello mondiale ogni anno. Queste scorte contengono ancora pentossido di vanadio, un composto apprezzato per le sue proprietà elettroniche e catalitiche ma noto anche per irritare i polmoni, danneggiare le piante e contaminare gli ecosistemi se non controllato.
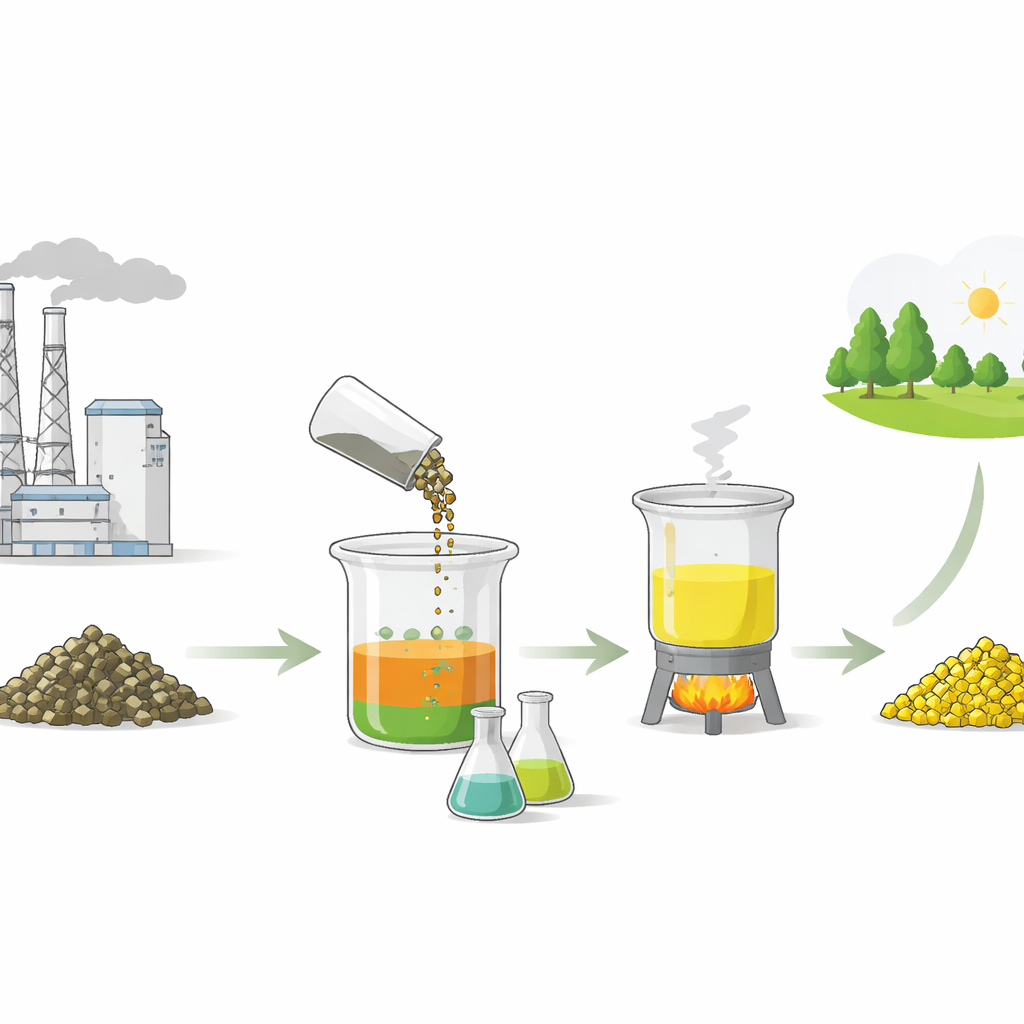
Trovare un modo più dolce per estrarre un metallo utile
Recuperare il vanadio dai rifiuti non è una novità, ma molti metodi esistenti fanno ricorso ad acidi minerali forti o a trattamenti alcalini aggressivi. Questi possono essere costosi, corrosivi e gravosi per l’ambiente. Gli autori si sono proposti di testare se semplici acidi organici—simili a quelli presenti in frutta o aceto—potessero svolgere lo stesso compito. Hanno macinato i pellet di catalizzatore esausto fino a ottenere particelle fini ed esposto i campioni a quattro diversi acidi: citrico, ossalico, tartarico e acetico. Regolando con cura la concentrazione dell’acido, i tempi di agitazione, la temperatura e il rapporto solido/liquido, hanno misurato quanto vanadio poteva essere disciolto in soluzione.
L’acido citrico si conferma un aiuto verde
Tra le quattro opzioni, l’acido citrico è emerso come il più efficace. A temperatura ambiente e a concentrazioni equivalenti, ha estratto molto più vanadio in soluzione rispetto agli altri. Il gruppo ha quindi esplorato le condizioni che massimizzavano l’azione dell’acido citrico. Aumentare la sua concentrazione fino a un molare ha migliorato progressivamente l’estrazione, dopo la quale il beneficio si è stabilizzato. Un tempo di reazione di circa due ore è risultato sufficiente; periodi più lunghi hanno fornito poco vantaggio aggiuntivo. Mantenere basso il rapporto solido/liquido ha facilitato l’accesso dell’acido a tutte le superfici delle particelle, e un riscaldamento moderato fino a 70 °C ha aumentato ulteriormente il recupero. Con la ricetta ottimale—acido citrico 1 molare, carico solido 2%, 70 °C, condizioni leggermente acide e una lisciviazione di due ore—il processo ha recuperato un impressionante 95% del vanadio presente.
Uno sguardo alla chimica
Per capire meglio i meccanismi in gioco, i ricercatori hanno impiegato strumenti che sondano la struttura e la composizione dei materiali. Misure ai raggi X hanno mostrato che, dopo il trattamento, il residuo solido perdeva i segnali associati ai composti di vanadio, confermando che quasi tutto il metallo era passato nella fase liquida. La spettroscopia infrarossa ha rivelato nuovi andamenti vibrazionali nella soluzione di acido citrico dopo il contatto con il catalizzatore, coerenti con la formazione di complessi stabili tra gli atomi di vanadio e le molecole di citrato. In termini semplici, l’acido citrico non soltanto libera il vanadio dal solido fornendo ioni idrogeno, ma lo avvolge anche in un “legame” molecolare che lo mantiene disciolto e disponibile per un successivo recupero.
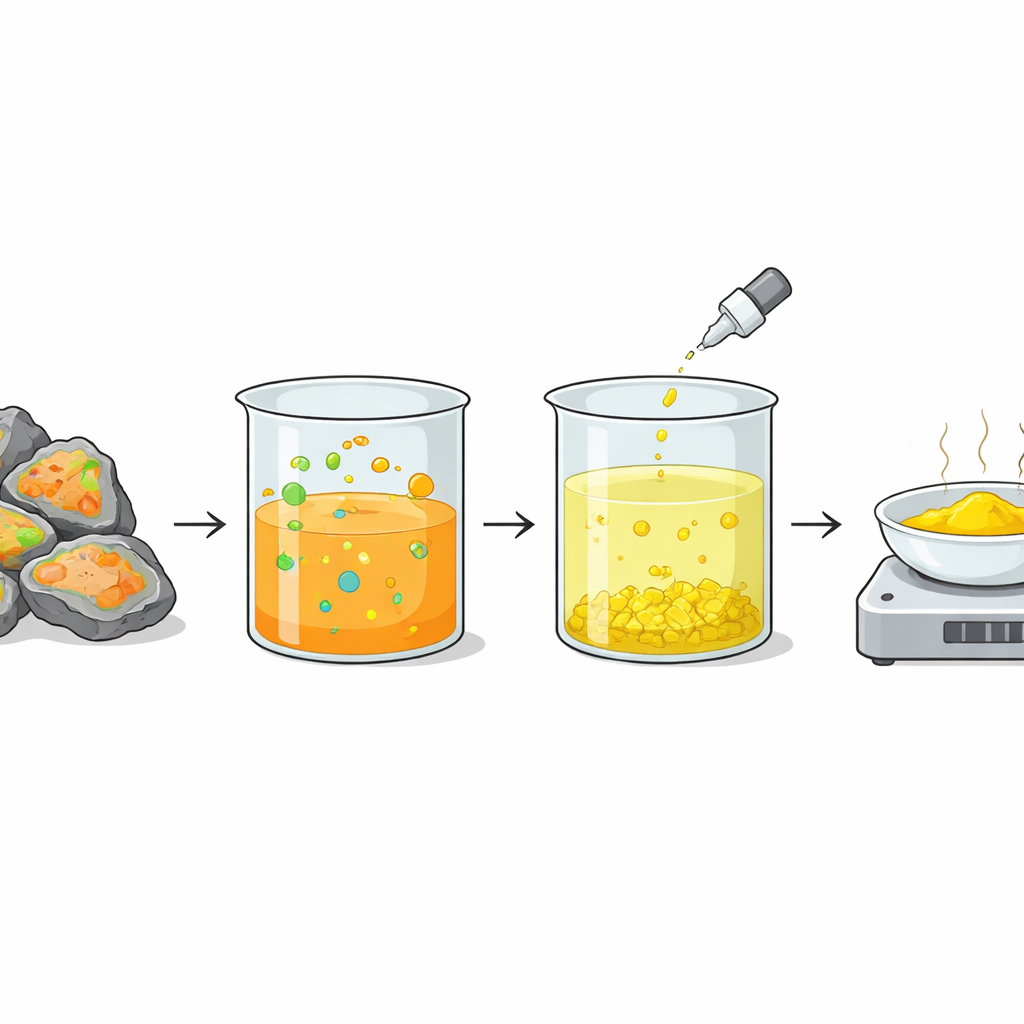
Dalla soluzione a un solido prezioso
Una volta che il vanadio era stato catturato in soluzione, il gruppo doveva ancora trasformarlo in un prodotto utile. Hanno aggiunto un comune sale contenente ioni ammonio e portato la soluzione a condizioni fortemente basiche. In queste condizioni, il vanadio precipitava sotto forma di un composto solido ammonico. Il riscaldamento di questo solido in aria ad alta temperatura lo ha trasformato in pentossido di vanadio—la polvere giallo brillante richiesta dall’industria. Questo passaggio finale chiude il ciclo: un rifiuto pericoloso della produzione di acido solforico viene convertito in un materiale di alto valore pronto per essere riutilizzato in batterie, catalizzatori o altre tecnologie.
Un percorso più pulito per i rifiuti da metalli pesanti
In termini pratici, questo lavoro dimostra che un acido relativamente delicato, simile al succo di agrumi, può aiutare a estrarre un metallo pericoloso ma prezioso dai residui industriali con efficienza molto elevata. Sostituendo sostanze chimiche più aggressive e catturando fino al 95% del vanadio, il metodo offre un modo per ridurre le discariche, diminuire l’inquinamento e recuperare una risorsa strategica che altrimenti verrebbe buttata. Se messo a scala, un approccio di recupero “verde” simile potrebbe aiutare molte industrie chimiche a considerare i loro materiali esausti non come rifiuti, ma come miniere secondarie proprio fuori dal cancello della fabbrica.
Citazione: Shaltout, A.A., El-Hallag, R.S.F. & Razek, T.M.A. Green recovery of vanadium from spent vanadium catalyst from sulfuric acid production. Sci Rep 16, 12869 (2026). https://doi.org/10.1038/s41598-026-47112-6
Parole chiave: recupero del vanadio, riciclo dei catalizzatori esausti, lisciviazione con acido citrico, industria dell'acido solforico, metallurgia verde