Clear Sky Science · es
Recuperación ecológica del vanadio de catalizadores agotados de la producción de ácido sulfúrico
Convertir los residuos industriales en un recurso
Cada año, las fábricas que producen ácido sulfúrico desechan miles de toneladas de catalizador usado: gránulos sólidos que en su día impulsaron las reacciones químicas dentro de sus torres. Estos materiales desechados son ricos en el metal vanadio, valioso para la industria pero dañino cuando se libera al aire, al suelo y al agua. Este estudio explora una forma de rescatar el vanadio de esos residuos usando un ácido relativamente suave de origen vegetal, transformando un subproducto peligroso en una materia prima útil y aliviando la presión sobre el medio ambiente.
Por qué importan el vanadio y el ácido sulfúrico
El ácido sulfúrico es uno de los productos químicos más producidos del mundo, utilizado en fertilizantes, refinado de combustibles, explosivos, tintes y baterías de automóvil. Su producción implica convertir dióxido de azufre en trióxido de azufre con la ayuda de un catalizador a base de vanadio. Con el tiempo, los granos del catalizador pierden eficacia y se reemplazan, generando alrededor de 40.000 toneladas de material agotado en todo el mundo cada año. Estos montones aún contienen óxido de vanadio (V), un compuesto apreciado por sus propiedades electrónicas y catalíticas, pero que también puede irritar los pulmones, dañar plantas y contaminar ecosistemas si no se controla.
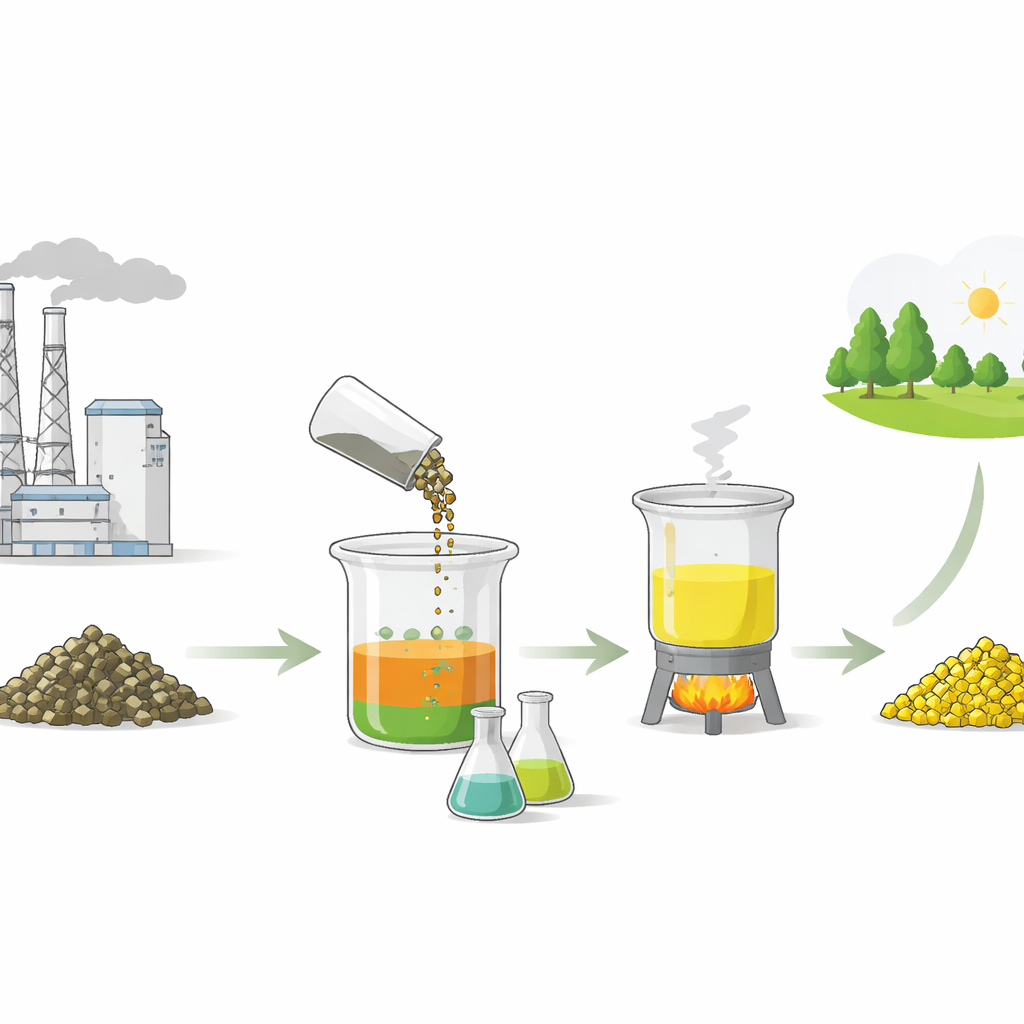
Buscar una forma más suave de extraer un metal útil
Recuperar vanadio de los residuos no es nuevo, pero muchos métodos existentes dependen de ácidos minerales fuertes o tratamientos alcalinos agresivos. Estos pueden ser costosos, corrosivos y con gran impacto ambiental. Los autores se propusieron probar si ácidos orgánicos sencillos—similares a los que hay en frutas o vinagre—podrían hacer el trabajo en su lugar. Molieron los pellets de catalizador agotado hasta obtener partículas finas y las expusieron a cuatro ácidos diferentes: cítrico, oxálico, tartárico y acético. Ajustando con cuidado la cantidad de ácido, el tiempo de agitación, la temperatura y la proporción sólido-líquido, midieron cuánto vanadio podía extraerse a la solución.
El ácido cítrico se impone como auxiliar ecológico
Entre las cuatro opciones, el ácido cítrico destacó. A temperatura ambiente y a igual concentración, extrajo mucho más vanadio a la solución que los demás. El equipo exploró entonces qué condiciones optimizaban su rendimiento. Aumentar su concentración hasta una molar mejoró de forma constante la extracción, tras lo cual la ganancia se estabilizó. Dejar reaccionar la mezcla durante aproximadamente dos horas fue suficiente; tiempos más largos aportaron poco beneficio adicional. Mantener baja la proporción sólido-líquido permitió que el ácido alcanzara todas las superficies de las partículas, y calentar suavemente la mezcla hasta 70 °C aumentó aún más la recuperación. Con la receta óptima—ácido cítrico 1 M, carga sólida del 2 %, 70 °C, condiciones ligeramente ácidas y un lavado de dos horas—el proceso recuperó un impresionante 95 % del vanadio presente.
Mirando dentro de la química
Para comprender lo que sucedía a un nivel más profundo, los investigadores usaron herramientas que analizan la estructura y la composición de los materiales. Mediciones por rayos X mostraron que, tras el tratamiento, el residuo sólido perdió las señales asociadas a los compuestos de vanadio, confirmando que casi todo el metal había pasado al líquido. La espectroscopía infrarroja reveló nuevos patrones de vibración en la solución de ácido cítrico una vez que hubo contactado con el catalizador, coherentes con la formación de complejos estables entre átomos de vanadio y moléculas de citrato. En términos sencillos, el ácido cítrico no solo afloja el vanadio del sólido al aportar iones hidrógeno, sino que también lo envuelve en una especie de “agarre” molecular, manteniéndolo disuelto y disponible para su recuperación posterior.
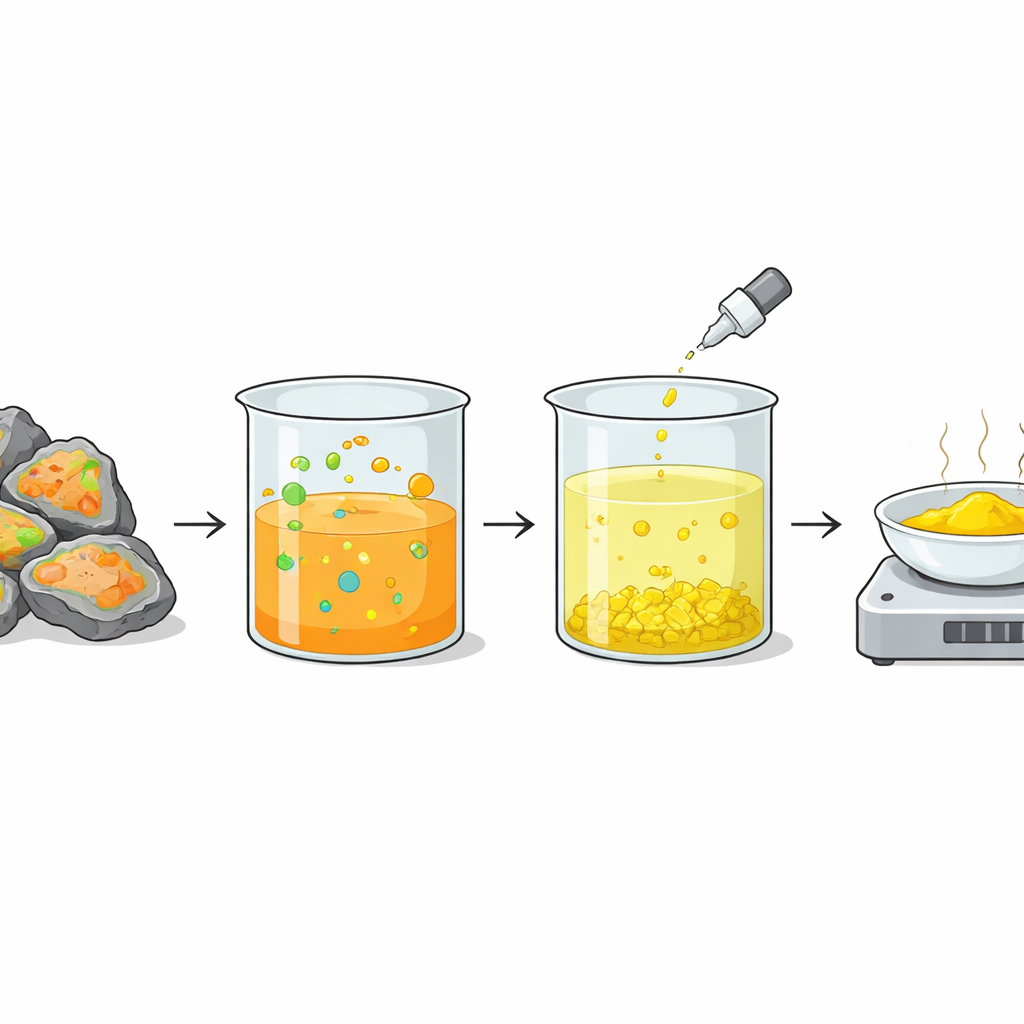
Del líquido de nuevo a un sólido valioso
Una vez que el vanadio quedó capturado en solución, el equipo aún necesitaba convertirlo en un producto útil. Hicieron esto añadiendo una sal común que contenía iones amonio y ajustando la mezcla a condiciones fuertemente básicas. Bajo estas condiciones, el vanadio precipitó como un compuesto sólido de amonio. Calentar este sólido en aire a alta temperatura lo transformó en óxido de vanadio, el polvo amarillo brillante que demanda la industria. Este paso final cierra el ciclo: un residuo peligroso de la producción de ácido sulfúrico se convierte en un material de alto valor listo para reutilizarse en baterías, catalizadores u otras tecnologías.
Un camino más limpio para los residuos de metales pesados
En términos cotidianos, este trabajo muestra que un ácido relativamente suave, de tipo cítrico, puede ayudar a extraer un metal peligroso pero valioso de los desechos industriales con muy alta eficiencia. Al reemplazar productos químicos más agresivos y capturar hasta el 95 % del vanadio, el método ofrece una vía para reducir montones de residuos, disminuir la contaminación y recuperar un recurso estratégico que de otro modo se tiraría. Si se escala, esquemas de recuperación “verdes” similares podrían ayudar a muchas plantas químicas a tratar sus materiales agotados no como basura, sino como una mina secundaria situada justo fuera de la puerta de la fábrica.
Cita: Shaltout, A.A., El-Hallag, R.S.F. & Razek, T.M.A. Green recovery of vanadium from spent vanadium catalyst from sulfuric acid production. Sci Rep 16, 12869 (2026). https://doi.org/10.1038/s41598-026-47112-6
Palabras clave: recuperación de vanadio, reciclaje de catalizadores agotados, lixiviación con ácido cítrico, industria del ácido sulfúrico, metalurgia verde