Clear Sky Science · fr
Récupération écologique du vanadium à partir du catalyseur usé de la production d’acide sulfurique
Transformer les déchets industriels en ressource
Chaque année, les usines qui produisent de l’acide sulfurique mettent au rebut des milliers de tonnes de catalyseur usagé — des pastilles solides qui facilitaient auparavant les réactions chimiques dans leurs tours. Ces matériaux jetés sont riches en vanadium, un métal précieux pour l’industrie mais nocif lorsqu’il se répand dans l’air, le sol et l’eau. Cette étude explore une méthode pour extraire le vanadium de ces déchets en utilisant un acide relativement doux d’origine végétale, transformant un sous‑produit dangereux en matière première utile tout en réduisant la pression sur l’environnement.
Pourquoi le vanadium et l’acide sulfurique comptent
L’acide sulfurique est l’un des produits chimiques les plus fabriqués au monde, utilisé dans les engrais, le raffinage des carburants, les explosifs, les colorants et les batteries de voiture. Sa production implique la conversion du dioxyde de soufre en trioxyde de soufre à l’aide d’un catalyseur à base de vanadium. Avec le temps, les grains de catalyseur perdent leur efficacité et sont remplacés, générant environ 40 000 tonnes de matériau usé dans le monde chaque année. Ces stocks contiennent encore du pentoxyde de vanadium, un composé recherché pour ses propriétés électroniques et catalytiques mais également connu pour irriter les poumons, nuire aux plantes et contaminer les écosystèmes s’il n’est pas maîtrisé.
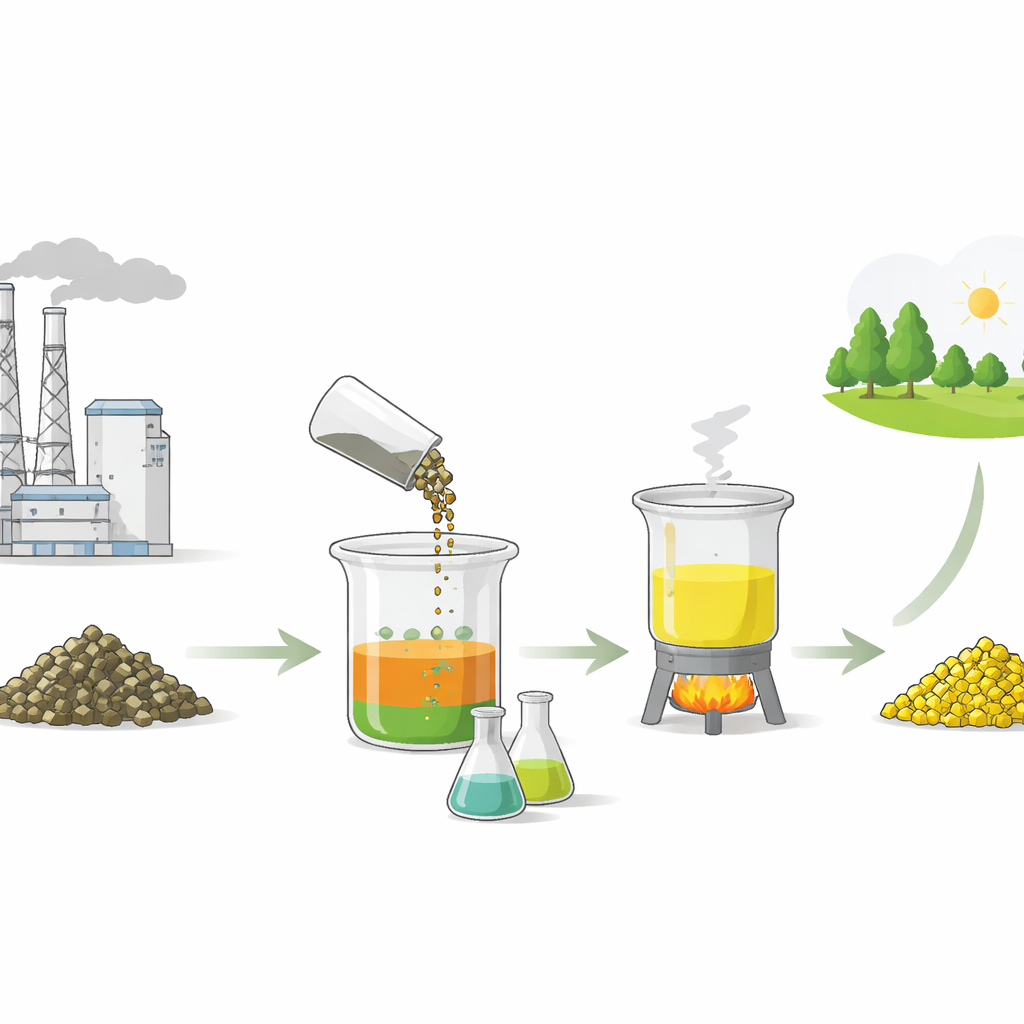
Chercher une voie plus douce pour extraire un métal utile
Récupérer le vanadium des déchets n’est pas nouveau, mais de nombreuses méthodes existantes reposent sur des acides minéraux forts ou des traitements alcalins agressifs. Ceux‑ci peuvent être coûteux, corrosifs et lourds pour l’environnement. Les auteurs ont voulu vérifier si de simples acides organiques — similaires à ceux que l’on trouve dans les fruits ou le vinaigre — pouvaient faire l’affaire à la place. Ils ont broyé les pastilles de catalyseur usé en particules fines et les ont exposées à quatre acides différents : citrique, oxalique, tartrique et acétique. En ajustant soigneusement la quantité d’acide, la durée d’agitation, la température et le rapport solide/liquide, ils ont mesuré la quantité de vanadium extraite en solution.
L’acide citrique s’impose comme aide écologique
Parmi les quatre options, l’acide citrique s’est distingué. À température ambiante et à concentration égale, il a extrait bien plus de vanadium que les autres. L’équipe a ensuite étudié les conditions optimales pour l’acide citrique. L’augmentation de sa concentration jusqu’à un mole par litre a amélioré progressivement l’extraction, au‑delà de quoi les gains se sont stabilisés. Un temps de réaction d’environ deux heures était suffisant ; des durées plus longues apportaient peu d’avantage supplémentaire. Un faible taux de charge solide‑liquide facilitait l’accès de l’acide à toutes les surfaces des particules, et un léger chauffage à 70 °C augmentait encore le rendement. Selon la recette optimale — acide citrique 1 molaire, charge solide 2 %, 70 °C, conditions légèrement acides et lixiviation de deux heures — le procédé a récupéré 95 % du vanadium présent.
Regarder au cœur de la chimie
Pour comprendre plus en profondeur ce qui se passait, les chercheurs ont utilisé des outils sondant la structure et la composition des matériaux. Les mesures par rayons X ont montré que, après traitement, le résidu solide avait perdu les signaux associés aux composés de vanadium, confirmant que presque tout le métal était passé en solution. La spectroscopie infrarouge a révélé de nouvelles bandes de vibration dans la solution d’acide citrique une fois mise en contact avec le catalyseur, compatibles avec la formation de complexes stables entre les atomes de vanadium et les molécules de citrate. En termes simples, l’acide citrique ne se contente pas de libérer le vanadium du solide en apportant des ions hydrogène, il l’enrobe aussi d’une « prise » moléculaire, le maintenant dissous et disponible pour une récupération ultérieure.
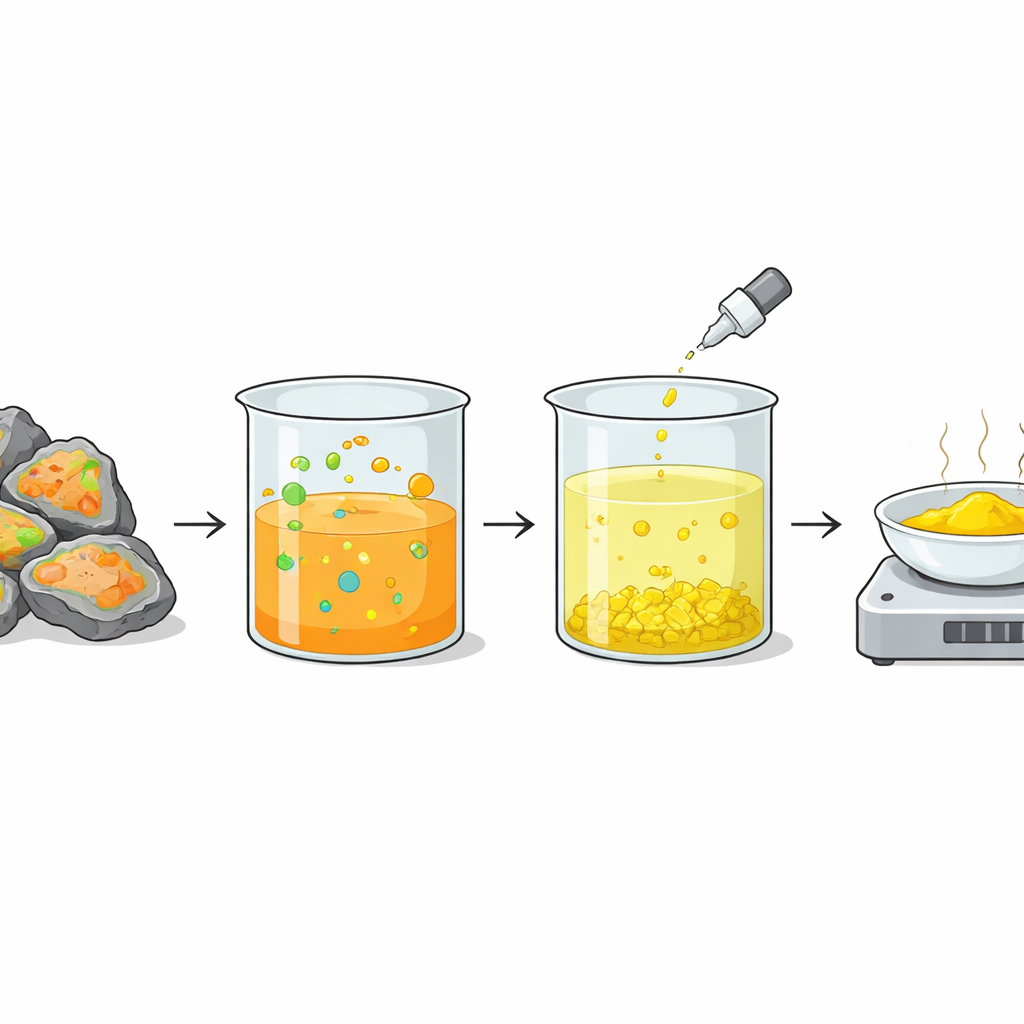
Du liquide à nouveau vers un solide de valeur
Une fois le vanadium capturé en solution, l’équipe devait encore le transformer en produit utile. Ils ont procédé en ajoutant un sel courant contenant des ions ammonium et en rendant le mélange fortement basique. Dans ces conditions, le vanadium s’est précipité sous forme d’un composé solide ammoniacal. Le chauffage de ce solide à haute température en présence d’air l’a transformé en pentoxyde de vanadium — la poudre jaune vif demandée par l’industrie. Cette étape finale boucle le cycle : un déchet dangereux issu de la production d’acide sulfurique est converti en un matériau de grande valeur prêt à être réutilisé dans des batteries, des catalyseurs ou d’autres technologies.
Une voie plus propre pour les déchets métalliques lourds
Concrètement, ce travail montre qu’un acide relativement doux, au goût d’agrumes, peut aider à extraire un métal dangereux mais précieux des résidus industriels avec une très haute efficacité. En remplaçant des produits chimiques plus agressifs et en capturant jusqu’à 95 % du vanadium, la méthode offre un moyen de réduire les tas de déchets, diminuer la pollution et récupérer une ressource stratégique qui serait autrement jetée. Si elle est montée en échelle, une telle approche de récupération « verte » pourrait aider de nombreuses usines chimiques à considérer leurs matériaux usés non pas comme des ordures, mais comme une mine secondaire située juste à la porte de l’usine.
Citation: Shaltout, A.A., El-Hallag, R.S.F. & Razek, T.M.A. Green recovery of vanadium from spent vanadium catalyst from sulfuric acid production. Sci Rep 16, 12869 (2026). https://doi.org/10.1038/s41598-026-47112-6
Mots-clés: récupération du vanadium, recyclage des catalyseurs usés, lixiviation à l’acide citrique, industrie de l’acide sulfurique, métallurgie verte