Clear Sky Science · it
Aggregati neutrofili-piastrinici CD177⁺ contribuiscono alla tromboinfiammazione tramite NET nel morbo necrotizzante dell’intestino
Perché i neonati molto piccoli affrontano un grosso problema intestinale
Il morbo necrotizzante dell’intestino è una malattia intestinale improvvisa e spesso letale che colpisce i neonati molto prematuri. I medici sanno che questi bambini sviluppano una forte infiammazione intestinale e talvolta pericolose coagulazioni, ma il modo in cui questi due processi si connettono è rimasto un mistero. Questo studio rivela una reazione a catena nascosta nei vasi sanguigni dell’intestino del lattante che aiuta a spiegare perché la malattia può peggiorare così rapidamente e suggerisce nuove modalità per diagnosticarla e possibilmente prevenirla. 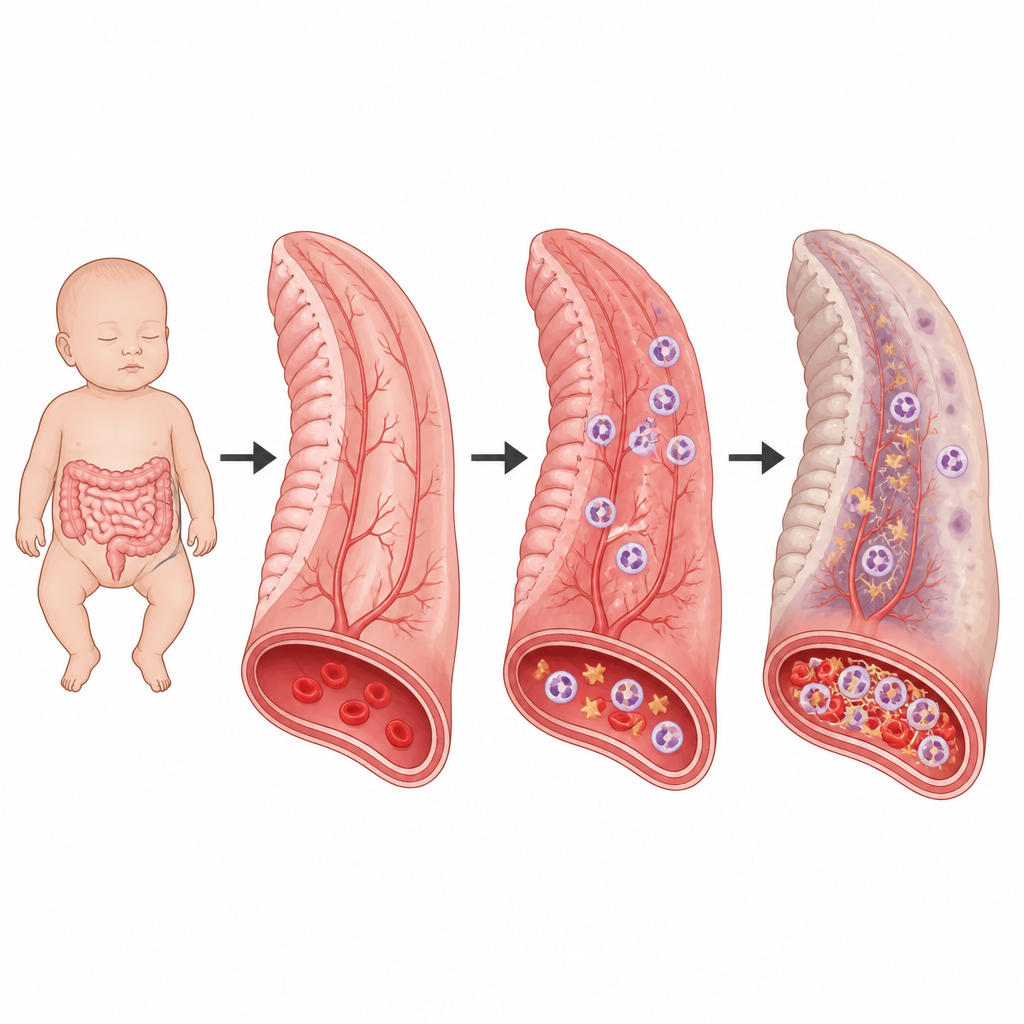
Quando difesa e coagulazione fanno squadra
I primi soccorritori del corpo contro infezioni e lesioni sono i globuli bianchi chiamati neutrofili e i minuscoli frammenti cellulari chiamati piastrine che favoriscono la coagulazione. Normalmente collaborano per intrappolare i germi in piccoli coaguli e impedirne la diffusione. Nel morbo necrotizzante dell’intestino, tuttavia, questa cooperazione diventa eccessiva. Gli autori hanno analizzato esami del sangue e tessuti di neonati colpiti e hanno riscontrato forti segni sia di infiammazione sia di alterazioni della coagulazione, tra cui marcatori di coagulazione elevati, piastrine basse e molti neutrofili. Al microscopio, i piccoli vasi intestinali erano spesso ostruiti da coaguli ricchi di neutrofili, piastrine e fibrina, le fibre proteiche che costituiscono il coagulo.
Un sottogruppo speciale di neutrofili al centro della scena
Utilizzando la tecnologia di lettura genica a singola cellula, i ricercatori hanno scoperto che non tutti i neutrofili si comportano allo stesso modo. Nei bambini con morbo necrotizzante dell’intestino, un sottogruppo che esprime un marcatore di superficie chiamato CD177 era fortemente ampliato sia nel sangue sia nel tessuto intestinale. Questi neutrofili CD177-positivi erano predisposti ad aderire alle pareti vascolari, interagire con le piastrine e attivare percorsi di coagulazione. In modelli murini della malattia, neutrofili marcati da CD177 simili erano arricchiti e mostravano attività genica collegata al movimento cellulare e al consolidamento del coagulo, suggerendo che questo sottogruppo è particolarmente efficiente nel costruire e rimodellare coaguli all’interno dei piccoli vasi intestinali.
Ammassi cellulari appiccicosi e mortali reti molecolari
Il gruppo ha poi esaminato come questi neutrofili specializzati interagiscono con le piastrine. Hanno scoperto che i neutrofili CD177-positivi si legano frequentemente alle piastrine formando ammassi misti di cellule chiamati aggregati neutrofili–piastrinici. Questi aggregati erano molto più comuni nei neonati malati e negli intestini malati dei topi e aumentavano con la gravità della malattia. All’interno di questi ammassi, i neutrofili rilasciavano reti di DNA e proteine note come trappole extracellulari dei neutrofili, o NET. Pur essendo utili per catturare i microbi, in questo contesto le NET si intrecciavano con piastrine e fibrina all’interno dei vasi, ispessendo i coaguli, bloccando il flusso sanguigno e aggravando la sofferenza da ossigeno nella parete intestinale. 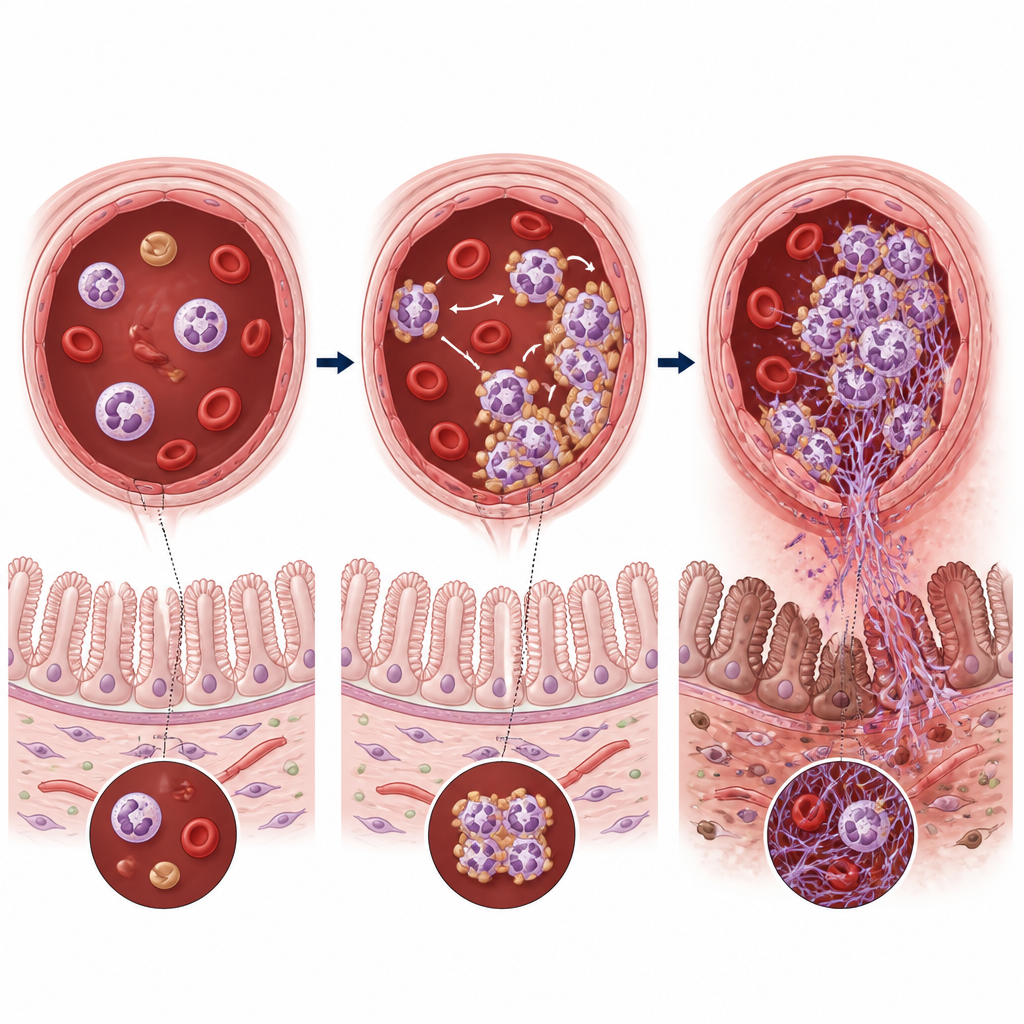
Abbassare il volume del ciclo dannoso
Per verificare se questi processi guidano effettivamente il danno piuttosto che accompagnarlo, i ricercatori li hanno manipolati intenzionalmente nei topi. La rimozione dei neutrofili o l’eliminazione specifica dei neutrofili CD177-positivi ha ridotto il numero di aggregati, diminuito la formazione di NET, attenuato il danno intestinale e migliorato la sopravvivenza. Farmaci che degradano direttamente le NET o ne bloccano la formazione hanno avuto effetti protettivi simili. L’eparina a basso peso molecolare, già utilizzata in molti ospedali, ha inoltre interferito con gli aggregati neutrofili–piastrinici, ridotto il carico di NET, calmato l’infiammazione e contribuito a preservare il tessuto intestinale quando somministrata preventivamente nei modelli animali.
Cosa potrebbe significare per i neonati fragili
In un piccolo gruppo di neonati, i livelli di neutrofili CD177-positivi, dei loro aggregati con piastrine e dei marcatori correlati alle NET aumentavano alla diagnosi e diminuivano con il miglioramento clinico, suggerendo che queste misurazioni potrebbero aiutare i medici a monitorare l’attività della malattia in tempo reale. Nel complesso, lo studio ritrae il morbo necrotizzante dell’intestino non solo come un’infiammazione intestinale, ma come un disturbo in cui cellule immunitarie e coagulazione si intrecciano in un circuito dannoso all’interno dei microvasi intestinali. Interrompere questo circuito colpendo i neutrofili CD177-positivi, i loro aggregati appiccicosi o le reti NET che producono potrebbe un giorno offrire modi più sicuri per prevedere, prevenire o attenuare questa malattia devastante nei neonati più vulnerabili.
Citazione: Lan, C., Tian, B., Shi, Y. et al. CD177⁺ neutrophil-platelet aggregates contribute to thromboinflammation via NETs in necrotizing enterocolitis. Nat Commun 17, 4167 (2026). https://doi.org/10.1038/s41467-026-70717-4
Parole chiave: morbo necrotizzante dell’intestino, aggregati neutrofili piastrinici, trappole extracellulari dei neutrofili, tromboinfiammazione, eparina a basso peso molecolare