Clear Sky Science · fr
Les agrégats neutrophiles-plaquettaires CD177⁺ contribuent à la thrombo‑inflammation via des NETs dans l’entérocolite nécrosante
Pourquoi les très petits bébés font face à un gros problème intestinal
L’entérocolite nécrosante est une maladie intestinale aiguë et souvent mortelle qui touche les nouveau‑nés très prématurés. Les médecins savent que ces nourrissons développent une inflammation intestinale intense et parfois une coagulation sanguine dangereuse, mais la façon dont ces deux processus sont liés restait énigmatique. Cette étude met au jour une réaction en chaîne cachée dans les vaisseaux sanguins de l’intestin du nourrisson qui aide à expliquer pourquoi la maladie peut s’aggraver si rapidement et suggère de nouvelles façons de la diagnostiquer et éventuellement de la prévenir. 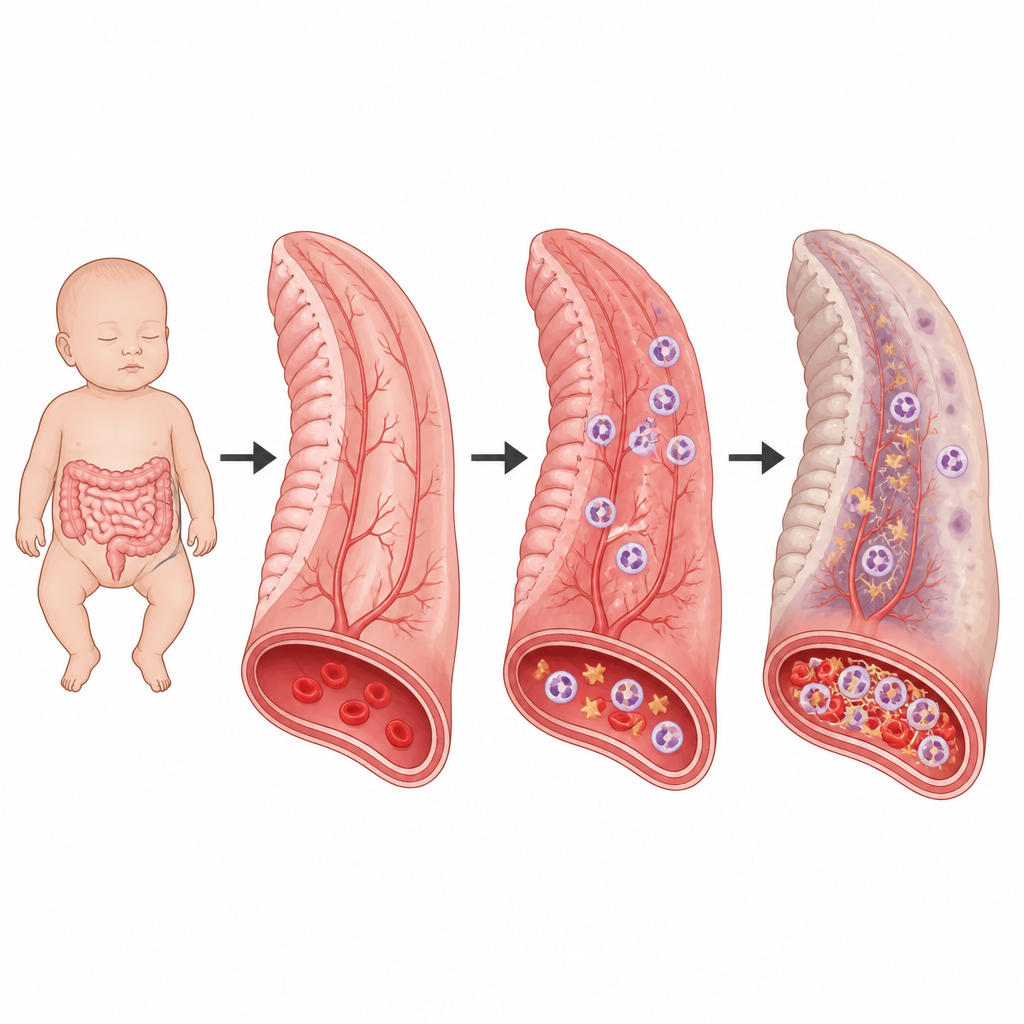
Quand défense et coagulation font équipe
Les premiers intervenants face à une infection ou une lésion sont des globules blancs appelés neutrophiles et de petites particules cellulaires, les plaquettes, qui favorisent la coagulation. Normalement, ils coopèrent pour piéger les germes dans de petits caillots et éviter leur propagation. Dans l’entérocolite nécrosante, toutefois, cette coopération devient excessive. Les auteurs ont analysé des tests sanguins et des tissus d’enfants atteints et ont trouvé de forts signes à la fois d’inflammation et de perturbations de la coagulation, notamment des marqueurs de coagulation élevés, une thrombocytopénie et un grand nombre de neutrophiles. Au microscope, de petits vaisseaux intestinaux étaient souvent bouchés par des caillots riches en neutrophiles, plaquettes et fibrine, les fils protéiques qui forment un caillot.
Un sous‑type de neutrophiles prend le devant de la scène
En utilisant la technologie de lecture génique cellule par cellule, les chercheurs ont découvert que tous les neutrophiles ne se comportent pas de la même manière. Chez les bébés atteints d’entérocolite nécrosante, un sous‑groupe exprimant un marqueur de surface appelé CD177 était fortement élargi dans le sang et le tissu intestinal. Ces neutrophiles CD177‑positifs étaient prêts à adhérer aux parois vasculaires, à interagir avec les plaquettes et à activer des voies de coagulation. Dans des modèles murins de la maladie, des neutrophiles marqués par CD177 étaient également enrichis et présentaient une activité génique liée au mouvement cellulaire et au resserrement des caillots, ce qui suggère que ce sous‑type est particulièrement apte à former et remodeler des caillots à l’intérieur des minuscules vaisseaux intestinaux.
Amas cellulaires collants et toiles moléculaires létales
L’équipe a ensuite examiné comment ces neutrophiles spécialisés se comportent avec les plaquettes. Ils ont constaté que les neutrophiles CD177‑positifs se liaient fréquemment aux plaquettes pour former des amas cellulaires mixtes appelés agrégats neutrophiles–plaquettes. Ces agrégats étaient beaucoup plus fréquents chez les nourrissons malades et dans les intestins malades des souris, et leur nombre augmentait à mesure que la maladie s’aggravait. À l’intérieur de ces agrégats, les neutrophiles libéraient des filets d’ADN et de protéines connus sous le nom de filets extracellulaires de neutrophiles (NETs). Si les NETs peuvent aider à capturer les microbes, dans ce contexte ils s’entremêlaient avec les plaquettes et la fibrine à l’intérieur des vaisseaux, épaississant les caillots, bloquant le flux sanguin et aggravant l’hypoxie de la paroi intestinale. 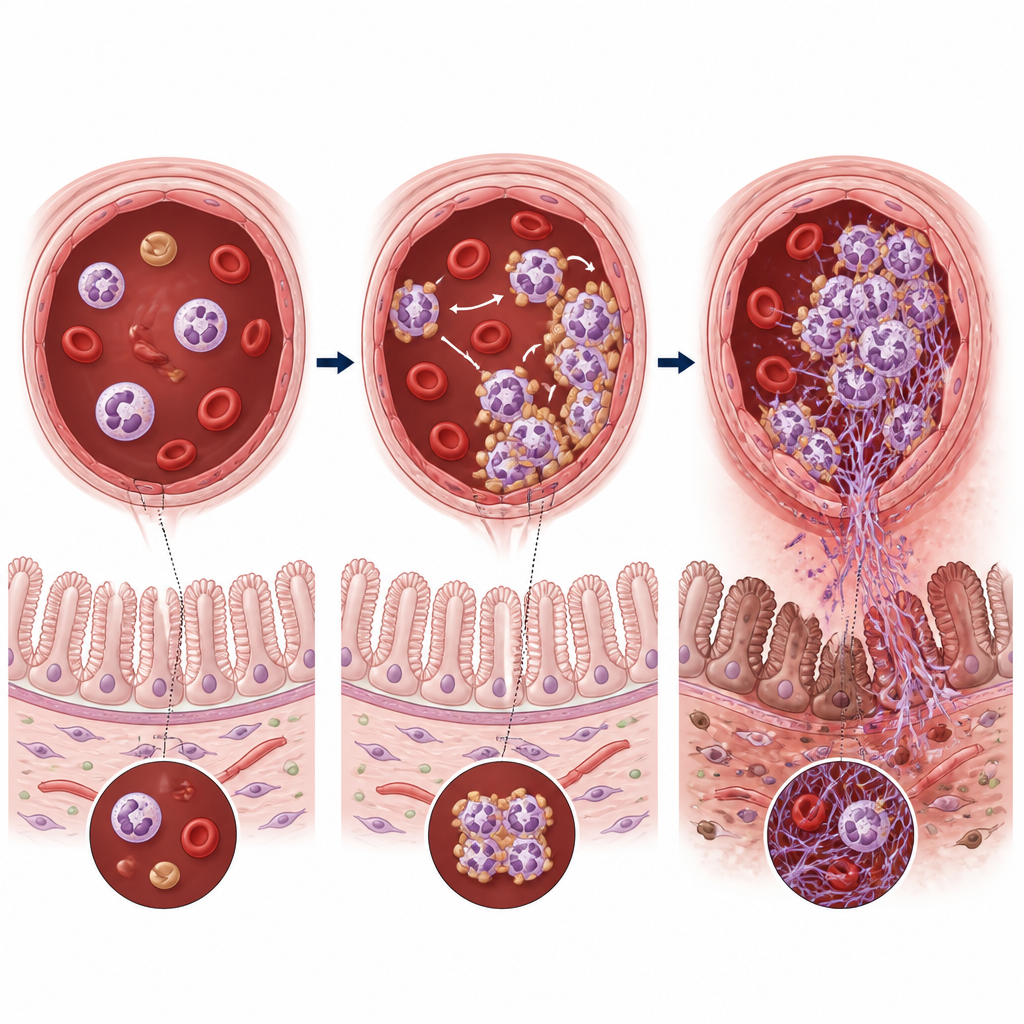
Atténuer le cercle vicieux néfaste
Pour vérifier si ces processus causent réellement les lésions plutôt que de simplement les accompagner, les chercheurs les ont délibérément modifiés chez la souris. L’élimination des neutrophiles ou la suppression spécifique des neutrophiles CD177‑positifs a réduit le nombre d’agrégats, diminué la formation de NETs, atténué les lésions intestinales et amélioré la survie. Des médicaments qui dégradent directement les NETs ou bloquent leur formation ont produit des effets protecteurs similaires. L’anticoagulant héparine de bas poids moléculaire, déjà utilisé dans de nombreux hôpitaux, a aussi perturbé les agrégats neutrophiles–plaquettes, réduit la charge en NETs, calmé l’inflammation et aidé à préserver le tissu intestinal lorsqu’il a été administré de façon préventive dans des modèles animaux.
Ce que cela pourrait signifier pour les nouveau‑nés fragiles
Dans un petit groupe de nourrissons, les niveaux de neutrophiles CD177‑positifs, leurs agrégats avec les plaquettes et les marqueurs liés aux NETs ont augmenté au moment du diagnostic puis diminué à l’amélioration des bébés, ce qui suggère que ces mesures pourraient aider les médecins à suivre l’activité de la maladie en temps réel. Dans l’ensemble, l’étude décrit l’entérocolite nécrosante non seulement comme une inflammation intestinale, mais comme un désordre où les cellules immunitaires et la coagulation s’enchevêtrent en une boucle dommageable à l’intérieur des microvaisseaux intestinaux. Briser cette boucle en ciblant les neutrophiles CD177‑positifs, leurs agrégats collants ou les toiles de NETs qu’ils forment pourrait un jour offrir des moyens plus sûrs de prédire, prévenir ou atténuer cette maladie dévastatrice chez les nouveau‑nés les plus vulnérables.
Citation: Lan, C., Tian, B., Shi, Y. et al. CD177⁺ neutrophil-platelet aggregates contribute to thromboinflammation via NETs in necrotizing enterocolitis. Nat Commun 17, 4167 (2026). https://doi.org/10.1038/s41467-026-70717-4
Mots-clés: entérocolite nécrosante, agrégats neutrophiles plaquettaires, filets extracellulaires de neutrophiles, thrombo‑inflammation, héparine de bas poids moléculaire