Clear Sky Science · it
Rilevazione ad alta risoluzione e ad alto rendimento della resistenza antibiotica nascosta con il saggio dilution-and-delay (DnD)
Perché i germi nascosti contano per la tua salute
Gli antibiotici sono pilastri della medicina moderna, ma non sempre funzionano come previsto. Anche quando i test di laboratorio indicano che un ceppo batterico è “sensibile”, il trattamento può comunque fallire perché una piccola frazione di cellule sopravvive silenziosamente. Questo articolo presenta un nuovo metodo di laboratorio, chiamato saggio dilution‑and‑delay (DnD), che può rivelare quei rari sopravvissuti a livelli anche di una su centomila milioni di cellule. Mostrando questa frazione nascosta, il metodo aiuta a spiegare fallimenti di trattamento inspiegabili e offre un modo più sfumato di pensare alla resistenza agli antibiotici.
Oltre i test antibiotici binari
Gli ospedali oggi si affidano a test semplici che pongono una domanda netta: una popolazione batterica cresce o non cresce a una certa dose di antibiotico? Il risultato viene riassunto in un unico numero, la concentrazione minima inibente (MIC), e poi trasformato in un’etichetta sì/no: sensibile o resistente. Questi test sono rapidi e pratici ma fanno una media su milioni di cellule, nascondendo le differenze all’interno della popolazione. In molte infezioni, solo una piccola minoranza di cellule è più robusta del resto—capace di tollerare o sopravvivere a livelli elevati di farmaco tramite meccanismi come l’eteroresistenza (una minoranza resistente), la persistenza (sopravvissuti dormienti) o la resistenza adattativa (indurimento indotto dal farmaco). I test standard sono in gran parte ciechi a queste cellule rare, nonostante esse possano innescare il fallimento del trattamento e alimentare la diffusione futura della resistenza pienamente sviluppata.
Due idee semplici: meno cellule e più tempo
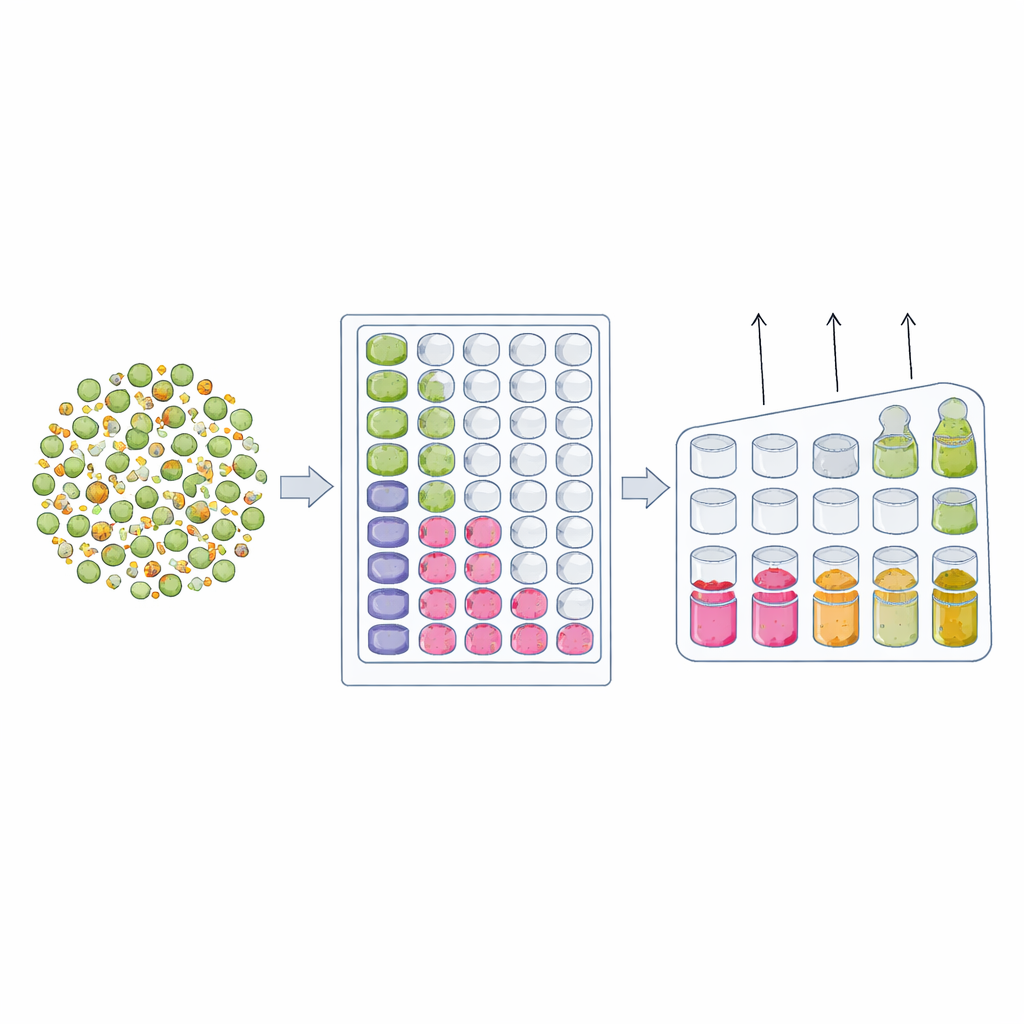
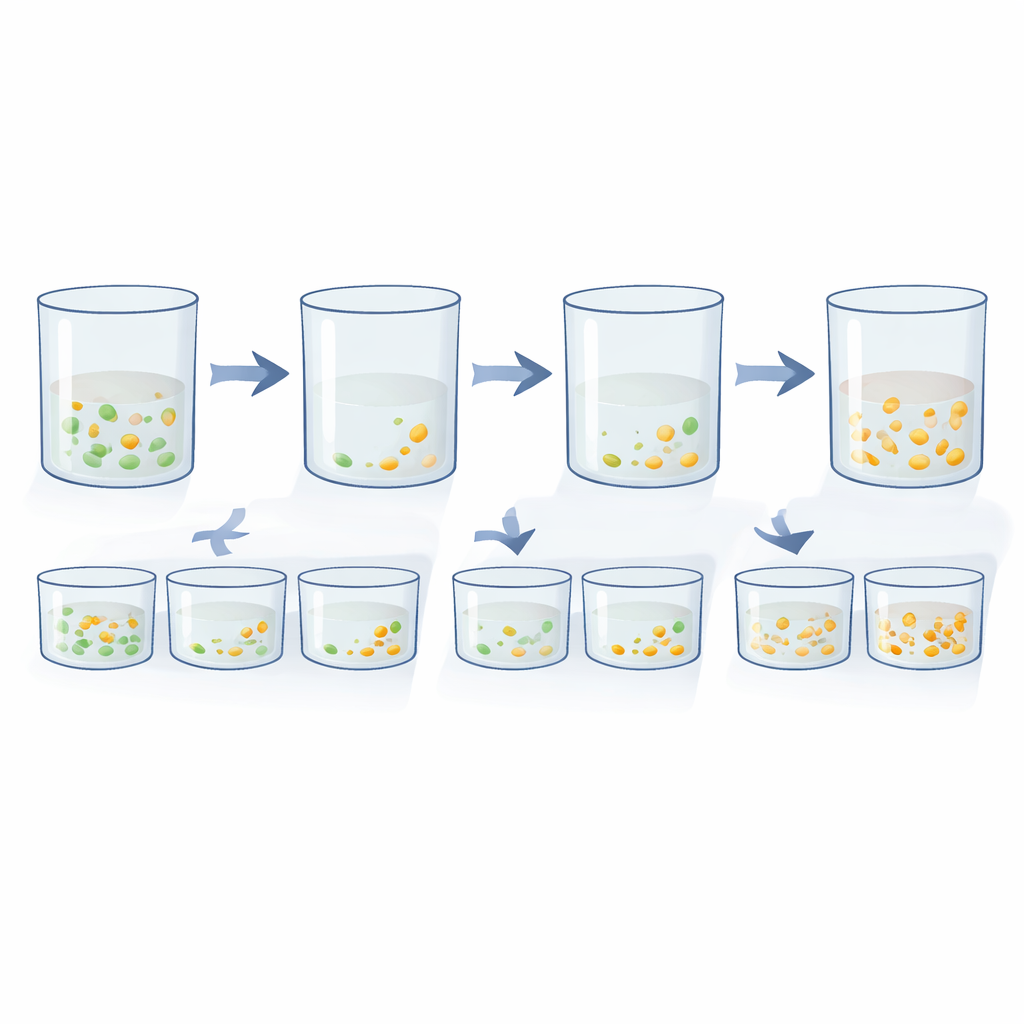
Il saggio DnD si basa su due principi intuitivi della crescita batterica. Il primo è la “diluzione fino all’estinzione”. Se hai una miscela di cellule per lo più sensibili e solo rarissime resistenti, la probabilità che una provetta contenga almeno una cellula resistente dipende da quante cellule metti. Preparando una serie di diluizioni decimali e verificando quali provette diventano torbide in presenza di antibiotici, i ricercatori possono individuare la diluizione in cui la crescita scompare. Confrontare questo punto di estinzione con e senza antibiotico rivela quante cellule resistenti erano nascoste nella coltura originale. Il secondo principio è il “ritardo nella crescita”. Quando una coltura viene esposta a un antibiotico, le cellule sensibili muoiono e la torbidità complessiva diminuisce. Se poche cellule resistenti sopravvivono, alla fine ricresceranno—ma solo dopo un ritardo evidente. Monitorando la torbidità nel tempo con un lettore di piastre e riavvolgendo matematicamente la curva di crescita fino al punto di partenza, il gruppo può stimare quante sopravvissute erano presenti all’inizio.
Combinare i segnali per vedere chiaramente i rari sopravvissuti
Poiché sia la diluzione‑fino‑all’estinzione sia il ritardo‑nella‑crescita usano lo stesso allestimento di base—una coltura in brodo in piastre a più pozzetti—gli autori le hanno unite in un unico quadro integrato DnD. Ogni piastra contiene una diluizione seriale del campione batterico e uno strumento standard misura automaticamente quanto ogni pozzetto diventa torbido nell’arco di molte ore. I pozzetti che non diventano mai torbidi definiscono dove le cellule resistenti finiscono, mentre i pozzetti che mostrano una ricrescita tardiva rivelano quanto tempo hanno impiegato i rari sopravvissuti a riprendersi. Mediando le informazioni lungo la serie di diluizioni, il metodo fornisce una stima precisa della frequenza di cellule insensibili all’antibiotico. Test con miscele controllate di ceppi completamente sensibili e completamente resistenti hanno mostrato che il DnD recupera fedelmente le frazioni note su molti ordini di grandezza, eguagliando o superando i metodi più vecchi e laboriosi basati sul conteggio su piastre.
Rivelare uno spettro, non un interruttore
Una volta convalidato, il saggio DnD è stato applicato a isolati clinici reali provenienti da diversi patogeni ospedalieri comuni e a cinque antibiotici importanti. I risultati sono stati sorprendenti: quasi uno su cinque combinazioni ceppo‑farmaco si è collocata tra chiaramente sensibile e chiaramente resistente, formando un ampio plateau di comportamento “intermedio”. Molti isolati presentavano inoltre sottopopolazioni minoritarie in grado di persistere dopo esposizioni antibiotiche intense, con frequenze distribuite su cinque ordini di grandezza. Questi schemi hanno mostrato che ciò che chiamiamo “resistenza” non è uno stato acceso/spento netto ma un continuum di probabilità di sopravvivenza. Lo studio ha inoltre dimostrato che la soglia MIC ampiamente usata riflette principalmente i limiti di rilevamento degli saggi convenzionali: è il punto in cui le minoranze resistenti diventano così rare che un inoculo di dimensione standard è improbabile contenga anche un solo sopravvissuto.
Cosa significa per i pazienti e la medicina
Per un non specialista, il messaggio chiave è che le infezioni possono nascondere una piccola ma pericolosa riserva di batteri che i test standard non riescono a vedere. Il saggio DnD offre un modo pratico e scalabile per misurare quante di queste sopravvivenze nascoste esistono, molto prima che prendano il sopravvento e spingano un ceppo verso la resistenza evidente. Pur essendo necessari ulteriori studi clinici per collegare queste misure dettagliate agli esiti dei pazienti, il lavoro pone le basi per scelte antibiotiche più informate, un migliore monitoraggio dell’evoluzione precoce della resistenza e linee guida aggiornate che trattino la suscettibilità agli antibiotici come uno spettro anziché come una semplice etichetta sì/no.
Citazione: Ma, M., Kim, M. High-resolution, high-throughput detection of hidden antibiotic resistance with the dilution-and-delay (DnD) susceptibility assay. Nat Commun 17, 3641 (2026). https://doi.org/10.1038/s41467-026-70174-z
Parole chiave: resistenza agli antibiotici, eteroresistenza, persistenza batterica, test di suscettibilità, microbiologia clinica