Clear Sky Science · de
Hochauflösende, hochdurchsatzfähige Erkennung versteckter Antibiotikaresistenz mit dem Dilutions‑und‑Verzögerungs (DnD)-Suszeptibilitätsassay
Warum versteckte Keime für Ihre Gesundheit wichtig sind
Antibiotika sind Eckpfeiler der modernen Medizin, funktionieren aber nicht immer wie erwartet. Selbst wenn Labortests einen Bakterienstamm als „sensibel“ einstufen, kann die Behandlung scheitern, weil ein winziger Bruchteil der Zellen stillschweigend überlebt. Diese Arbeit stellt eine neue Labormethode vor, den Dilutions‑und‑Verzögerungs‑(DnD‑)Assay, die jene seltenen Überlebenden bis zu Häufigkeiten von einem in hundert Millionen Zellen sichtbar machen kann. Indem die Methode diese versteckte Fraktion aufdeckt, hilft sie, rätselhafte Therapieversager zu erklären, und bietet eine nuanciertere Sicht auf Antibiotikaresistenz.
Über einfache Ja‑/Nein‑Antibiotikatests hinaus
Krankenhäuser verlassen sich derzeit auf einfache Tests, die eine grobe Frage stellen: wächst eine Bakterienpopulation bei einer gegebenen Antibiotikadosis oder nicht? Das Ergebnis wird als einzelne Zahl zusammengefasst, die minimale Hemmkonzentration (MHK oder MIC), und dann in ein Ja‑/Nein‑Etikett verwandelt: sensibel oder resistent. Diese Tests sind schnell und praktikabel, mitteln jedoch über Millionen von Zellen und verbergen Unterschiede innerhalb der Population. Bei vielen Infektionen ist nur eine kleine Minderheit der Zellen robuster als der Rest—sie toleriert oder überlebt hohe Wirkstoffkonzentrationen durch Mechanismen wie Heteroresistenz (eine resistente Minderheit), Persistenz (dormante Überlebende) oder adaptive Resistenz (durch das Medikament induzierte Verhärtung). Standardtests sind gegenüber diesen seltenen Zellen weitgehend blind, obwohl sie Therapieversagen auslösen und die spätere Ausbreitung vollständiger Resistenz antreiben können.
Zwei einfache Ideen: weniger Zellen und mehr Zeit
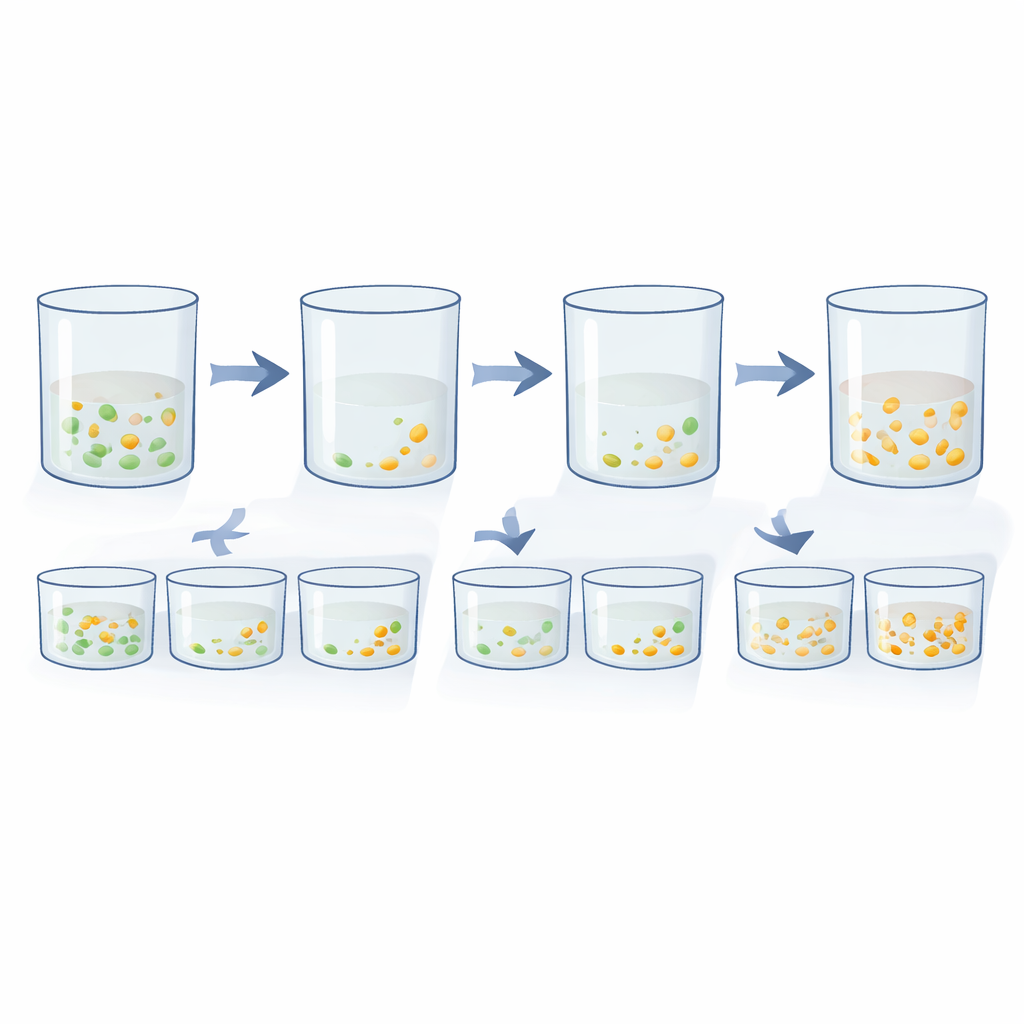
Der DnD‑Assay baut auf zwei intuitiven Prinzipien des bakteriellen Wachstums auf. Das erste ist „Dilution‑to‑extinction“ (Verdünnung bis zur Auslöschung). Wenn Sie eine Mischung aus überwiegend sensiblen Zellen und sehr wenigen resistenten haben, hängt die Wahrscheinlichkeit, dass ein Reaktionsgefäß mindestens eine resistente Zelle enthält, davon ab, wie viele Zellen Sie hineingeben. Durch die Herstellung einer Serie zehnfacher Verdünnungen und die Überprüfung, welche Gefäße in Gegenwart von Antibiotika trüb werden, können die Forschenden die Verdünnung bestimmen, bei der das Wachstum verschwindet. Der Vergleich dieses Auslöschungs‑Punktes mit und ohne Antibiotikum zeigt, wie viele resistente Zellen ursprünglich versteckt waren. Das zweite Prinzip ist „Delay‑to‑growth“ (Verzögerung bis zum Wachstum). Wenn eine Kultur einem Antibiotikum ausgesetzt wird, sterben empfindliche Zellen ab und die Gesamttrübung sinkt. Überleben ein paar resistente Zellen, werden sie schließlich wieder wachsen—aber erst nach einer spürbaren Verzögerung. Indem die Trübung über die Zeit mit einem Plattenleser verfolgt und die Wachstumskurve mathematisch zurückgerechnet wird, kann das Team abschätzen, wie viele Überlebende zu Beginn vorhanden waren.
Signale kombinieren, um seltene Überlebende klar zu sehen
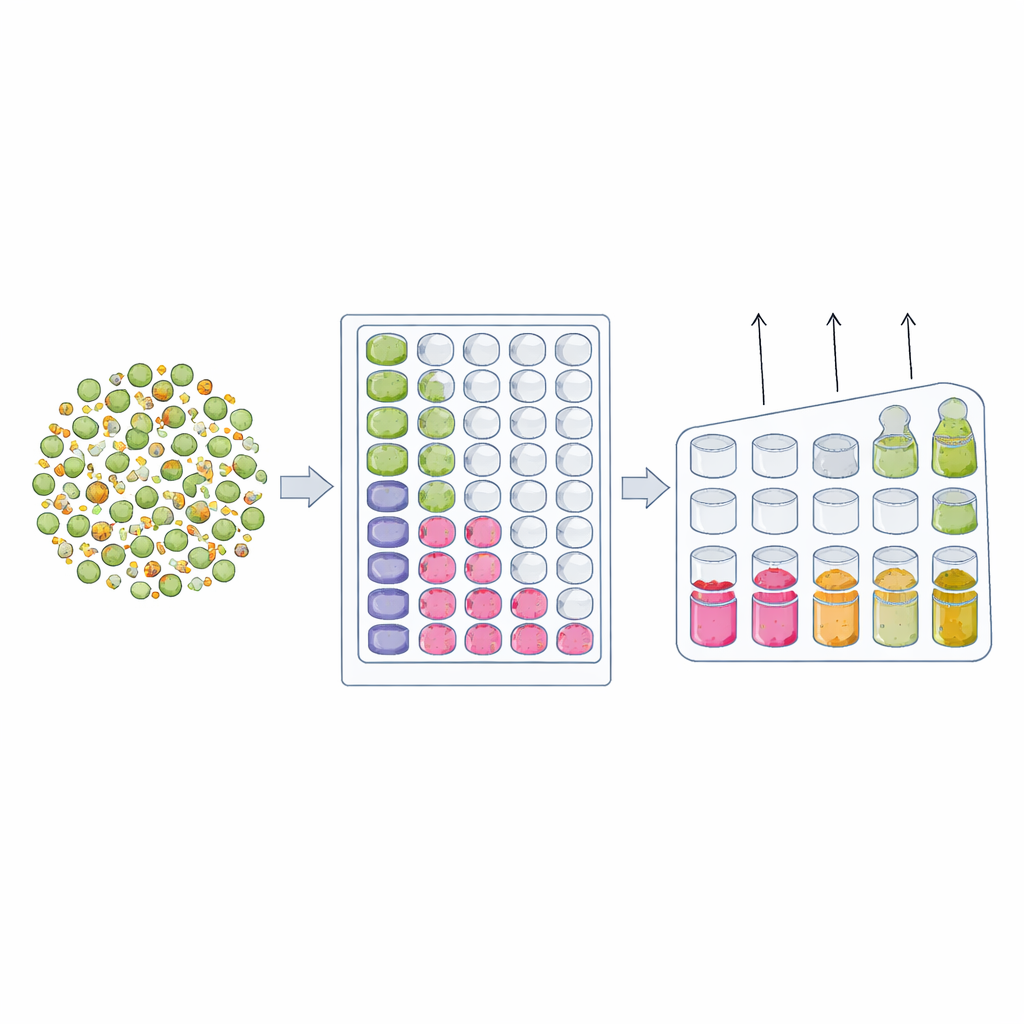
Da sowohl Dilution‑to‑extinction als auch Delay‑to‑growth auf derselben Grundanordnung—einer Brühekultur in Multiwell‑Platten—beruhen, kombinierten die Autorinnen und Autoren sie zu einem integrierten DnD‑Framework. Jede Platte enthält eine serielle Verdünnung der bakteriellen Probe, und ein Standardgerät misst automatisch, wie trüb jede Vertiefung über viele Stunden wird. Vertiefungen, die niemals trüb werden, definieren, wo resistente Zellen ausgehen, während Vertiefungen mit später Neuansiedlung zeigen, wie lange seltene Überlebende zum Wiederaufschwung brauchten. Durch das Mittelwertbilden der Informationen über die Verdünnungsserie liefert die Methode eine präzise Schätzung der Häufigkeit antibiotika‑insensitiver Zellen. Tests mit kontrollierten Mischungen vollständig sensitiver und vollständig resistenter Stämme zeigten, dass DnD bekannte Anteile über viele Größenordnungen zuverlässig rekonstruierte und dabei mit älteren, arbeitsaufwändigen Plattzählmethoden mithalten oder sie übertreffen konnte.
Ein Kontinuum zeigen, statt eines Schalters
Nach der Validierung wurde der DnD‑Assay an realen klinischen Isolaten mehrerer häufiger Krankenhauspathogene und fünf wichtiger Antibiotika angewandt. Die Ergebnisse waren auffällig: Fast eine von fünf Stamm‑Wirkstoff‑Kombinationen lag zwischen eindeutig sensibel und eindeutig resistent und bildete ein breites Plateau „dazwischenliegendes“ Verhaltens. Viele Isolate trugen außerdem Minderheitsunterpopulationen, die nach intensiver Antibiotikabehandlung persistieren konnten, deren Häufigkeiten sich über fünf Größenordnungen erstreckten. Diese Muster zeigten, dass das, was wir als „Resistenz“ bezeichnen, kein scharfes An‑/Aus‑Merkmal ist, sondern ein Kontinuum von Überlebenswahrscheinlichkeiten. Die Studie demonstrierte ferner, dass die weithin verwendete MIC‑Schwelle hauptsächlich die Nachweisgrenzen konventioneller Tests widerspiegelt: Sie markiert den Punkt, an dem resistente Minderheiten so selten werden, dass eine standardgroße Inokulumwahrscheinlichkeit unwahrscheinlich ist, auch nur einen Überlebenden zu enthalten.
Was das für Patientinnen, Patienten und die Medizin bedeutet
Für Nicht‑Fachleute lautet die zentrale Botschaft, dass Infektionen eine kleine, aber gefährliche Reservearmee von Bakterien verbergen können, die Standardtests nicht sehen. Der DnD‑Assay bietet eine praktische, skalierbare Möglichkeit, abzuschätzen, wie viele solcher versteckter Überlebender existieren, lange bevor sie die Oberhand gewinnen und einen Stamm in offensichtliche Resistenz treiben. Obwohl weitere klinische Studien nötig sind, um diese detaillierten Messungen mit Patientenergebnissen zu verknüpfen, schafft die Arbeit die Grundlage für fundiertere Antibiotikaentscheidungen, besseres Monitoring der frühen Resistenzentwicklung und aktualisierte Leitlinien, die Antibiotikasensitivität als Spektrum statt als einfaches Ja‑/Nein behandeln.
Zitation: Ma, M., Kim, M. High-resolution, high-throughput detection of hidden antibiotic resistance with the dilution-and-delay (DnD) susceptibility assay. Nat Commun 17, 3641 (2026). https://doi.org/10.1038/s41467-026-70174-z
Schlüsselwörter: Antibiotikaresistenz, Heteroresistenz, bakterielle Persistenz, Empfindlichkeitstest, klinische Mikrobiologie