Clear Sky Science · it
I batteri filamentosi segmentati sono commensali intestinali umani presenti in tutto il mondo
Aiutanti nascosti nel nostro intestino
Nel profondo dell’intestino umano vive un gruppo poco noto di microrganismi chiamati batteri filamentosi segmentati, o SFB. Lungi dall’essere studiati solo nei topi, questi strani batteri a filo plasmano potentemente il sistema immunitario. Fino ad ora non si sapeva quanto fossero comuni negli esseri umani, né se esistesse una vera versione umana. Questo studio combina microscopia, sequenziamento del genoma e vaste indagini globali sul DNA per mostrare che gli SFB sono veri residenti dell’intestino umano presenti in tutti i continenti abitati, soprattutto nella prima infanzia.
Conosci i filamenti ad uncino
Gli SFB non assomigliano ai batteri tondeggianti o a bastoncello più familiari. Al microscopio appaiono come lunghi filamenti fatti di segmenti, con un’estremità sottile che forma una punta ad uncino usata per aggrapparsi saldamente al rivestimento dell’intestino tenue. I ricercatori hanno esaminato feci di bambini in Mali, Kenya e Gambia e hanno trovato filamenti con esattamente questa forma distintiva: un segmento sottile e liscio che termina in una punta, regioni spesse e bulbose dove si staccano nuove cellule e spore che aiutano i batteri a sopravvivere in condizioni avverse. Immagini elettroniche ad alta risoluzione hanno confermato che questi filamenti umani condividono lo stesso piano corporeo segmentato e la struttura ad uncino degli SFB classici osservati nei topi da laboratorio.
Una nuova specie umana con una dieta speciale
Per andare oltre l’aspetto morfologico, il team ha ricostruito i genomi di questi SFB africani a partire dai campioni di feci. Il DNA ha mostrato che costituiscono una nuova specie, che gli autori nominano Anisomitus miae, e che appartiene saldamente alla più ampia famiglia degli SFB osservata in molti animali. Come i loro cugini animali, questi batteri hanno genomi piccoli e snelli e sembrano strettamente adattati alla vita sulla superficie intestinale. Tuttavia possiedono anche caratteristiche uniche: un set completo di enzimi per degradare amido e glicogeno e importare le catene di zuccheri risultanti, oltre a difese aggiuntive contro lo stress ossidativo e altre sollecitazioni ambientali. Questi tratti suggeriscono che gli SFB umani sfruttano fonti energetiche specifiche derivate dalla dieta e dall’ospite e sono attrezzati per resistere alle condizioni variabili dell’intestino.
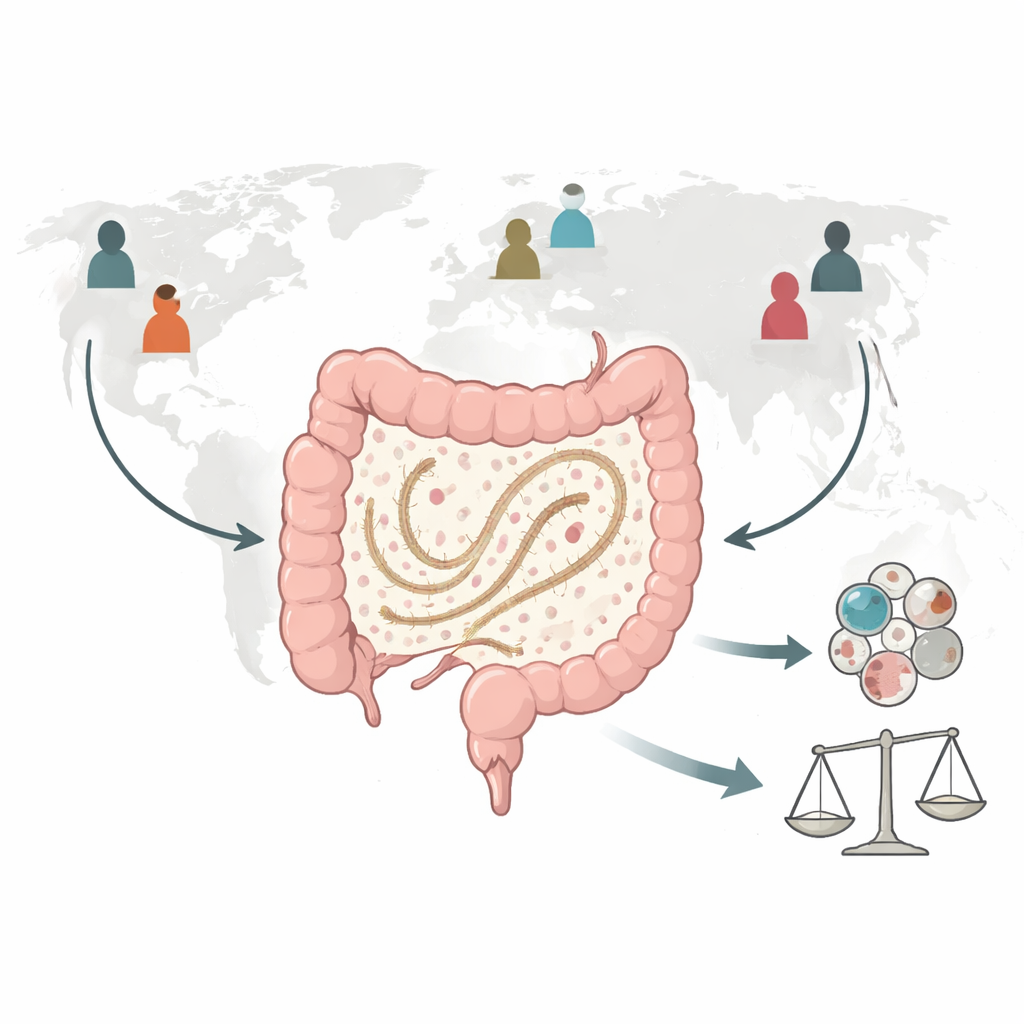
Sei lignaggi che si diffondono nel mondo
Gli autori hanno quindi setacciato migliaia di dataset di DNA pubblicamente disponibili, concentrandosi sul gene 16S rRNA, una barcode standard per identificare i batteri. Definendo con cura quanto deve essere simile una sequenza per essere conteggiata come SFB, hanno scoperto segnature simili agli SFB in campioni di persone di oltre quaranta paesi. I dati si raggruppano in almeno quattro lignaggi umani principali e due minori. Un lignaggio, corrispondente alla nuova specie africana, domina nell’Africa subsahariana ed è presente anche in gruppi indigeni del Sud America. Altri sono più strettamente correlati agli SFB osservati in topi, ratti o polli e sono comuni in alcune parti dell’Asia e dell’Europa. In alcuni individui coesistono più di un lignaggio, il che significa che le persone possono ospitare una piccola miscela di tipi di SFB.
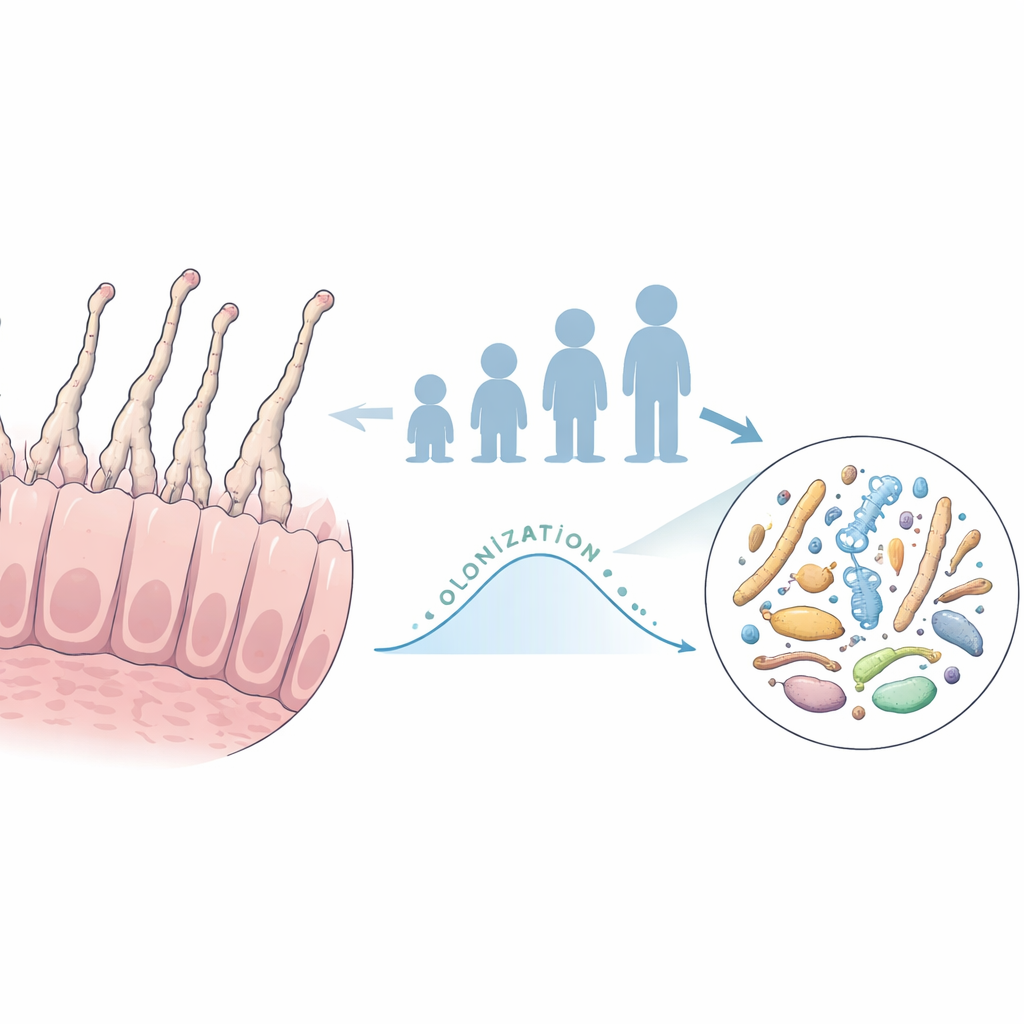
Una visita breve ma potente nell’infanzia
Emergono pattern sorprendenti guardando all’età. In diversi studi longitudinali su bambini in Africa, Sud America, Europa e Asia, gli SFB sono raramente osservati nei lattanti, aumentano tra circa uno e due anni d’età—spesso subito dopo lo svezzamento—e poi tornano a livelli molto bassi. Questo picco è di breve durata, dell’ordine di un mese, ma durante di esso gli SFB possono diventare da centinaia a migliaia di volte più abbondanti rispetto ad altri momenti. Negli adulti, gli SFB sono di solito presenti, se lo sono, a livelli così bassi che solo il sequenziamento ultra‑profondo riesce a rilevarli, sebbene siano relativamente arricchiti sui tessuti intestinali rispetto alle feci. Analisi familiari indicano che i bambini sono più propensi a ospitare SFB se la madre li possiede, suggerendo una trasmissione madre‑figlio. Esperimenti che trasferivano feci umane ricche di SFB in topi privi di germi non sono riusciti a stabilire gli SFB nei roditori, suggerendo che gli SFB umani sono selettivi rispetto all’ospite.
Perché questi batteri rari contano
Benché gli SFB costituiscano solo una piccola frazione del microbiota intestinale, studi nei topi mostrano che possono stimolare fortemente le cellule immunitarie, incluse quelle che pattugliano le superfici mucose e aiutano a respingere le infezioni. Il nuovo studio stabilisce che gli esseri umani ospitano più specie di SFB, che questi microrganismi sono diffusi ma generalmente rari, e che attivano un brusco aumento di colonizzazione durante la finestra sensibile dello svezzamento nella prima infanzia. Poiché quella stessa finestra è critica per l’addestramento del sistema immunitario, gli SFB umani potrebbero avere un ruolo sproporzionato nel plasmare l’immunità a vita e la suscettibilità alle malattie — dalle infezioni ai disturbi infiammatori. Comprendere quando, dove e quali lignaggi di SFB si stabiliscono nell’intestino umano apre la porta per esplorare come questo partner insolito influenzi la salute in tutto il mondo.
Citazione: Kiran, S., Cruz, A.R., Daniau, A. et al. Segmented filamentous bacteria are worldwide human gut commensals. Nat Commun 17, 4174 (2026). https://doi.org/10.1038/s41467-026-70010-4
Parole chiave: microbioma intestinale, batteri filamentosi segmentati, immunità infantile, microrganismi intestinali, diversità globale del microbiota