Clear Sky Science · fr
Les bactéries filamenteuses segmentées sont des commensales humaines intestinales présentes dans le monde entier
Aides discrètes dans nos intestins
Deep à l’intérieur de l’intestin humain réside un groupe de microbes peu connus appelés bactéries filamenteuses segmentées, ou BFS. Longtemps étudiées chez la souris, ces bactéries étranges et filiformes sont de puissants façonneurs du système immunitaire. Jusqu’à présent, on ignorait leur fréquence chez l’homme, voire si une véritable version humaine existait. Cette étude combine microscopie, séquençage de génomes et vastes enquêtes mondiales d’ADN pour montrer que les BFS sont de véritables résidentes de l’intestin humain, présentes sur tous les continents habités, en particulier pendant la petite enfance.
Rencontrez les fils crochus
Les BFS ne ressemblent pas aux bactéries rondes ou en bâtonnet familières. Au microscope, elles apparaissent comme de longs filaments constitués de segments, avec une extrémité fine qui forme une pointe en forme de crochet utilisée pour s’accrocher fermement à la muqueuse de l’intestin grêle. Les chercheurs ont examiné des selles d’enfants au Mali, au Kenya et en Gambie et ont trouvé des filaments présentant exactement cette forme caractéristique : un segment lisse et fin se terminant par une pointe, des régions épaisses et bulbeuses où de nouvelles cellules bourgeonnent, et des spores qui aident les bactéries à survivre à des conditions difficiles. Des images électroniques à haute résolution ont confirmé que ces filaments humains partagent le même plan corporel segmenté et la même structure en crochet que les BFS classiques observées chez la souris de laboratoire.
Une nouvelle espèce humaine avec un régime particulier
Pour aller au‑delà de l’apparence, l’équipe a reconstruit les génomes de ces BFS africaines à partir d’échantillons de selles. L’ADN montre qu’il s’agit d’une nouvelle espèce, que les auteurs nomment Anisomitus miae, et qu’elle appartient fermement à la famille plus large des BFS observée chez de nombreux animaux. Comme leurs cousines animales, ces bactéries possèdent des génomes petits et épurés et semblent étroitement adaptées à la vie à la surface de l’intestin. Elles présentent cependant des traits uniques : un ensemble complet d’outils pour dégrader l’amidon et le glycogène et importer les chaînes de sucres résultantes, ainsi que des défenses supplémentaires contre le stress oxydatif et d’autres stress environnementaux. Ces caractéristiques suggèrent que les BFS humaines exploitent des sources d’énergie alimentaires et dérivées de l’hôte spécifiques et qu’elles sont équipées pour supporter les conditions changeantes de l’intestin.
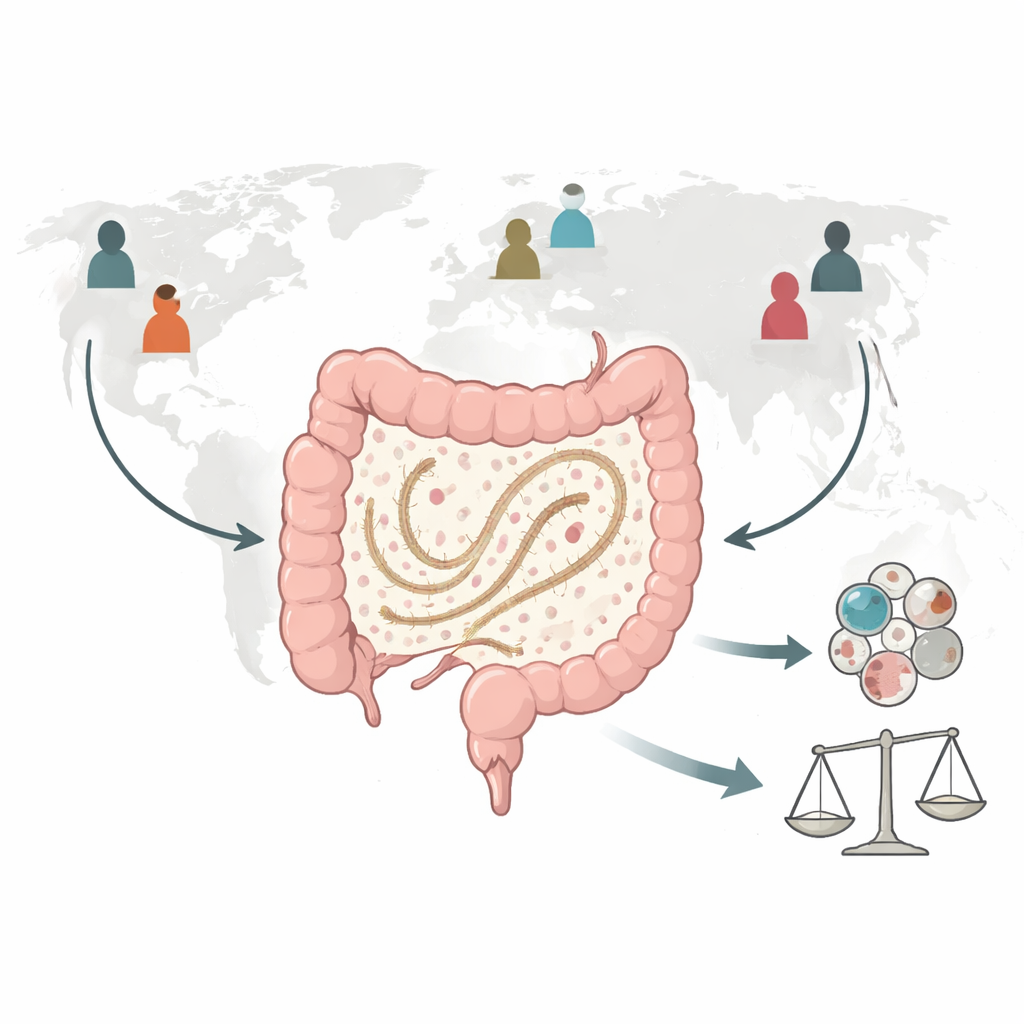
Six lignées réparties dans le monde
Les auteurs ont ensuite exploité des milliers de jeux de données d’ADN disponibles publiquement, en se concentrant sur le gène 16S rRNA, une barre d’identification standard pour les bactéries. En définissant soigneusement le degré de similarité d’une séquence pour la classer comme BFS, ils ont découvert des signatures de type BFS dans des échantillons provenant de plus de quarante pays. Les données se regroupent en au moins quatre lignées humaines majeures et deux mineures. Une lignée, correspondant à la nouvelle espèce africaine définie, domine en Afrique subsaharienne et se retrouve aussi chez des populations autochtones d’Amérique du Sud. D’autres sont plus proches des BFS observées chez la souris, le rat ou le poulet et sont communes dans certaines régions d’Asie et d’Europe. Chez certains individus, plusieurs lignées coexistent simultanément, ce qui signifie que les personnes peuvent porter une petite mixture de types de BFS.
Une visite brève mais puissante pendant l’enfance
Un schéma frappant émerge lorsque les auteurs examinent l’âge. Dans plusieurs cohortes d’enfants suivies à long terme en Afrique, Amérique du Sud, Europe et Asie, les BFS sont rarement détectées chez les nourrissons, augmentent fortement entre environ un et deux ans — souvent juste après le sevrage — puis retombent à des niveaux très faibles. Ce pic est de courte durée, de l’ordre d’un mois, mais pendant cette période les BFS peuvent devenir des centaines à des milliers de fois plus abondantes qu’à d’autres moments. Chez l’adulte, les BFS sont généralement présentes, si elles le sont, à des niveaux si bas que seul un séquençage ultra‑profond peut les détecter, bien qu’elles soient relativement enrichies sur le tissu intestinal par rapport aux selles. Les analyses familiales indiquent que les enfants ont davantage de chances de porter des BFS si leur mère en porte, ce qui suggère une transmission mère‑enfant. Des expériences transférant des selles humaines riches en BFS dans des souris exemptes de germes n’ont pas permis d’établir ces BFS chez la souris, suggérant que les BFS humaines sont sélectives quant à leur hôte.
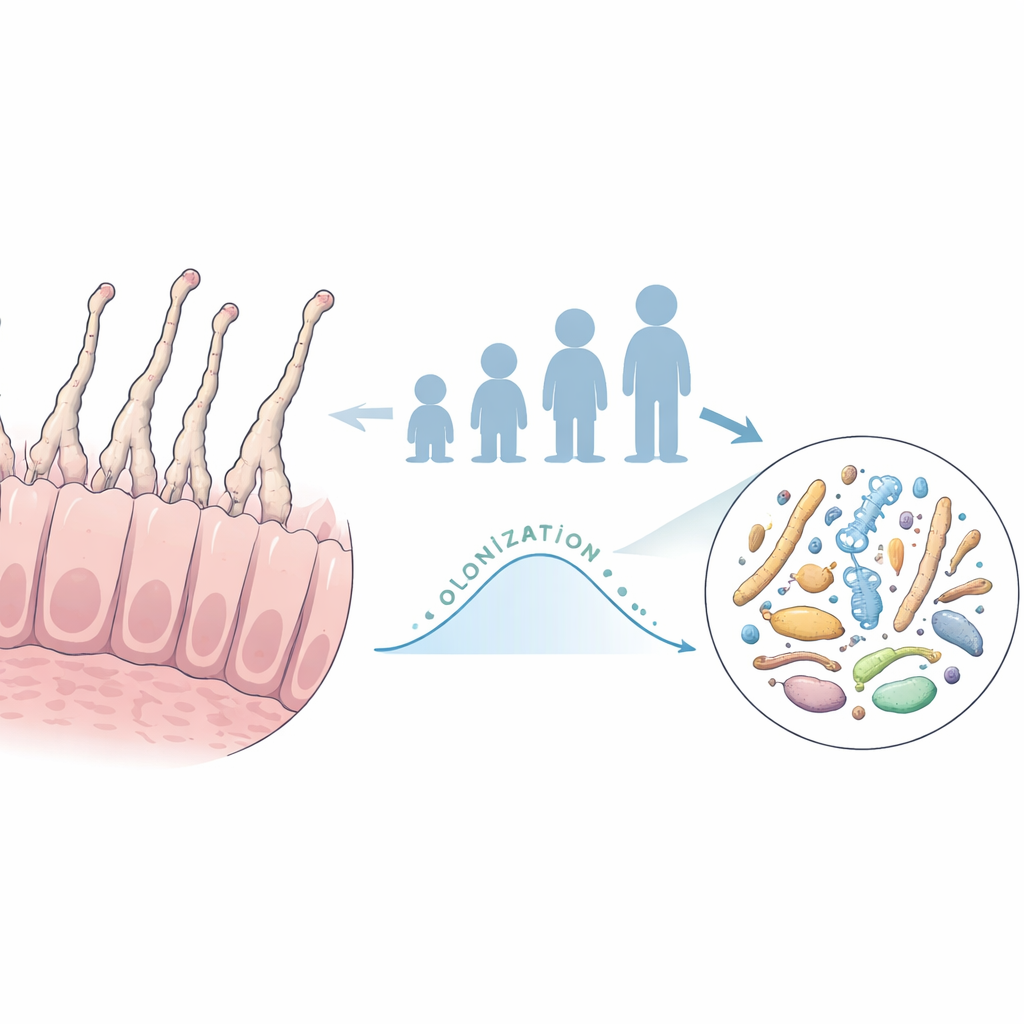
Pourquoi ces bactéries rares sont importantes
Bien que les BFS ne représentent qu’une fraction infime du microbiote intestinal, des travaux chez la souris montrent qu’elles peuvent fortement stimuler les cellules immunitaires, y compris celles qui patrouillent les surfaces muqueuses et aident à repousser les infections. La nouvelle étude établit que l’homme héberge plusieurs espèces de BFS, que ces microbes sont répandus mais généralement rares, et qu’ils provoquent une brusque explosion de colonisation durant la fenêtre sensible du sevrage en début de vie. Comme cette même période est cruciale pour l’apprentissage du système immunitaire, les BFS humaines pourraient jouer un rôle disproportionné dans la formation de l’immunité à vie et la susceptibilité aux maladies — des infections aux troubles inflammatoires. Comprendre quand, où et quelles lignées de BFS s’installent dans l’intestin humain ouvre la voie à l’exploration de la manière dont ce partenaire inhabituel influence la santé à travers le monde.
Citation: Kiran, S., Cruz, A.R., Daniau, A. et al. Segmented filamentous bacteria are worldwide human gut commensals. Nat Commun 17, 4174 (2026). https://doi.org/10.1038/s41467-026-70010-4
Mots-clés: microbiome intestinal, bactéries filamenteuses segmentées, immunité infantile, microbes intestinaux, diversité mondiale du microbiote