Clear Sky Science · he
אימונוהיסטוכימיה כמותית ושימוש במכיילים תאיים לקביעת מספר קולטני HER2
מדוע ספירת אותות בתאים חשובה
כשרופאים בודקים דגימת סרטן שד עבור הסמן HER2, התוצאה יכולה להכריע האם המטופלת תקבל תרופות ממוקדות עוצמתיות או לא. עם זאת, מבחן הצביעה הסטנדרטי, המכונה אימונוהיסטוכימיה, מתנהג עדיין יותר כמו אמנות מאשר כהתמרה מדידה: מעבדות שונות עשויות לקבל תוצאות שונות, ואותות חלשים במיוחד קלים להחמצה. המחקר הזה מראה כיצד להפוך את הצביעה הצבעונית למספר ממשי — על ידי הוספת תאים שהוכנו במיוחד שמשמשים כסרט מדידה מובנה לכמות ה‑HER2 הנמצאת על כל תא גידול.
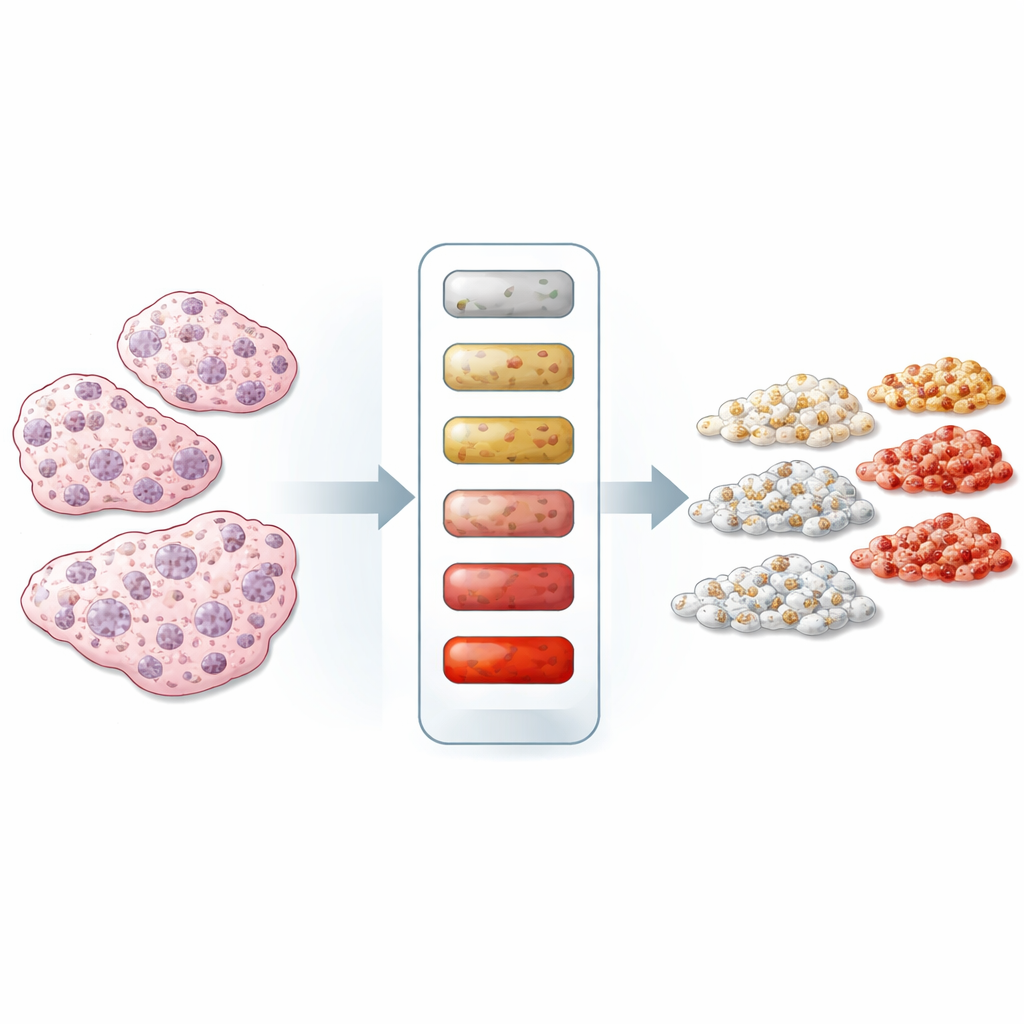
ממעבר-או-לא למספרים ממשיים
מרבית הבדיקות המבוססות צביעה מסווגות כיום את ה‑HER2 במדרגות רחבות כגון “0”, “1+”, “2+” או “3+”. קטגוריות אלה שימושיות אך גסות; הן אינן אומרות כמה קולטני HER2 באמת נמצאים על כל תא סרטני, במיוחד בקבוצות החשובות החדשות של "HER2‑low" ו"HER2‑ultralow". המחברים טוענים שהסיבה העיקרית לשיעורי טעויות גבוהים היא היעדר סרגלים כמותיים בתוך תהליך הצביעה עצמו. בדיקות מעבדה אחרות, כמו אימונואסאי בדם, נסמכות שגרתי על תקנים ובקרות איכות מוכנות בקפידה. הבאת משמעת דומה לצביעת רקמה יכולה להפוך את קריאות הפתולוגים ליותר עקביות ולאפשר דירוג עדין יותר של רמות HER2.
בניית סרטי מדידה מבוססי-תאים
כדי ליצור תקנים כאלה בחרה הקבוצה פנל של שורות תאי סרטן שד הנושאות באופן טבעי כמויות שונות של HER2, החל בכמעט אפס ועד לרמה גבוהה מאוד. הם השתמשו בשתי טכנולוגיות עצמאיות — אימונואסאי אלקטרוכמולומינסצנטי, שמודד HER2 בתאים מפורקים, וזרימת תאים (flow cytometry), שמספרת קולטנים על תאים שלמים — כדי לייחס לכל שורה מספר ממוצע של קולטני HER2 לכל תא. רוב שורות התאים היו בתיאום טוב בין שתי השיטות, מה שאישר שההיררכיה בכמות ה‑HER2 שלהן ידועה בביטחון, אם כי שורות עם ה‑HER2 הגבוה ביותר הראו חוסר התאמה מסוים בין הטכניקות. שורות תאים מאופיינות אלה הפכו אז ל"מכיילים תאיים" שניתן לעבד ולצבוע בדיוק כמו רקמת המטופל.
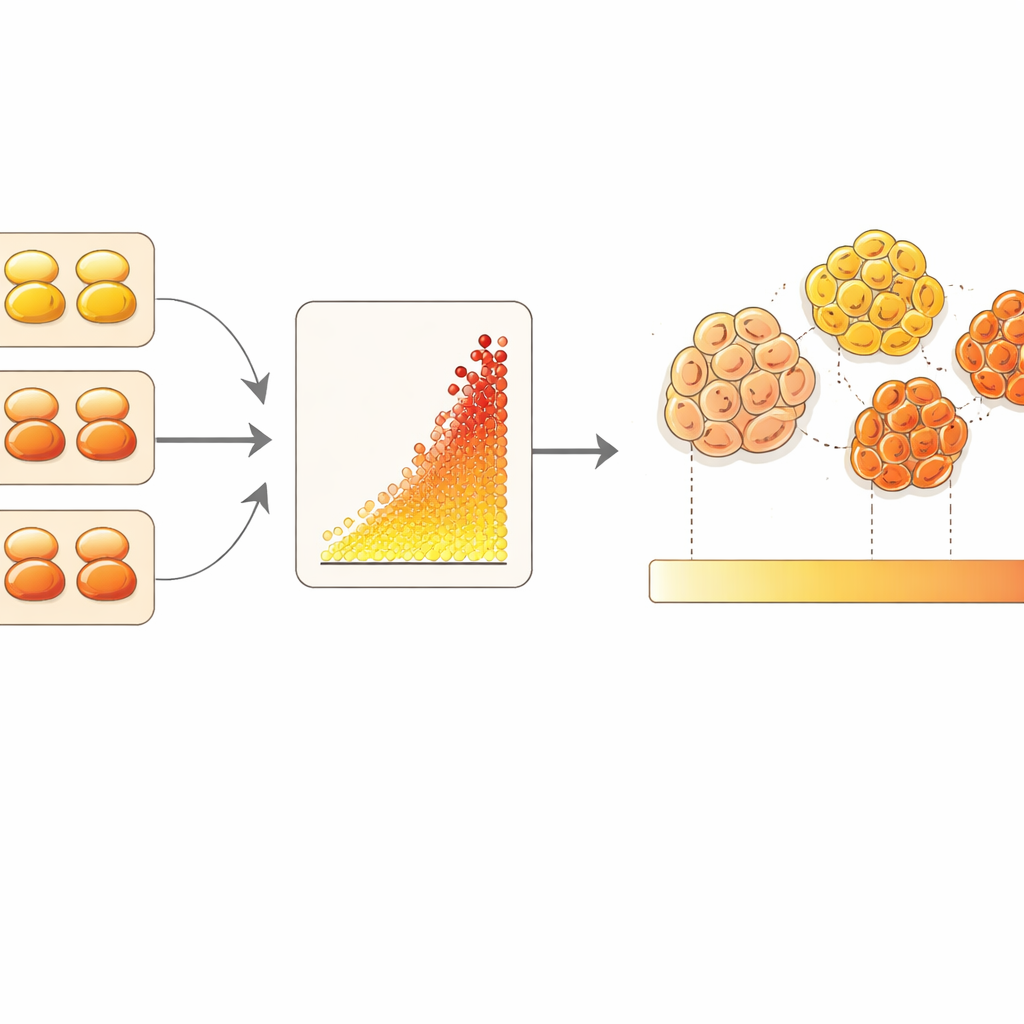
הפיכת תמונות מיקרוסקופ לספירות
החוקרים הטמיעו את תאי המכיילים בתוך בלוק שעווה, חיתכו פרוסות וצבעו אותן לצד מיקרואריי של 85 גידולי סרטן שד באמצעות גרסה פלואורסצנטית רגישת של מבחן HER2. כלי ניתוח תמונה מבוסס למידת מכונה אומן לזהות תאי גידול על בסיס צביעה נפרדת לחלבוני מבנה ולמדוד רק את אות ה‑HER2 סביב תאים אלה. על ידי שרטוט המספרים הידועים של הקולטנים של תאי המכיילים מול הבהירות הנמדדת שלהם, הקבוצה בנתה עקומת כיול. לאחר מכן השתמשו בעקומה זו כדי לתרגם את הבהירות הממוצעת של תאי הגידול של כל מטופלת לאומדן מספר קולטני HER2 לכל תא, בטווח שימושי של בערך מעשר ועד כמעט מאה ושמונים אלף קולטנים.
מה המספרים החדשים מגלים
כאשר השוו את ספירות ה‑HER2 הכמותיות הללו עם הדירוגים הקליניים הסטנדרטיים (בעזרת נוגדן נפוץ בשם 4B5), הקשר היה מפתיע והפוך: גידולים עם מספר קולטנים גבוה יותר שלעתים נשאו ציונים מסורתיים נמוכים יותר, ולהפך. דגימות רבות המסומנות כ"HER2 אפס" בפועל הופיעו עם רמות HER2 הניתנות למדידה בבהירות בשיטה החדשה. המחברים מזהירים שהאסאי שלהם עדיין לא מאומת במלואו ושהשונות בין גידול לגידול, הבדלים בנוגדנים ופרטים טכניים עשויים כולם לתרום לחוסר ההתאמה. עם זאת, הממצאים מדגישים כיצד קטגוריות חצי‑כמותיות יכולות להסתיר ספקטרום רציף של ביטוי HER2 בסרטנים אמיתיים.
הבטחה ומכשולים לשיפור בדיקות הסרטן
בסך הכל, העבודה מראה כי שימוש בתאים שלמים כמכיילים יכול להפוך את צביעת ה‑HER2 לבדיקה מספרית שדומה יותר לבדיקות מעבדה מוסדרות אחרות. משום שתאי המכיילים מדמים רקמה אמיתית — יש להם ממברנות, מבנים פנימיים וניתנים לצביעה באותו אופן — הם מספקים סרגל מדידה ריאלי לשיטות כמותיות עתידיות. יחד עם זאת, הגישה דורשת מאמץ: היא תלויה בשורות תאים מאופיינות היטב, בדיקות שיקוף קפדניות עם פלטפורמות מדידה מרובות, ותקנים ברורים לדיוק ולשחזור. המחברים טוענים שאם אימונוהיסטוכימיה כמותית כזו עתידה להנחות החלטות טיפוליות, הנחיות אימות פורמליות והוכחות לתועלת קלינית יהיו חיוניות, אך מכיילים מבוססי-תאים מציעים נתיב מעשי להשגת המטרה הזו.
ציטוט: McKinski, K., Chen, B. Quantitative immunohistochemistry and the use of cellular calibrators for HER2 receptor number determination. Sci Rep 16, 14573 (2026). https://doi.org/10.1038/s41598-026-42898-x
מילות מפתח: HER2 סרטן השד, אימונוהיסטוכימיה, מכיילים תאיים, כימות ביומרקרים, איכות בדיקות אבחון