Clear Sky Science · de
Quantitative Immunhistochemie und der Einsatz zellulärer Kalibratoren zur Bestimmung der HER2-Rezeptoranzahl
Warum das Zählen von Zelldignalen wichtig ist
Wenn Ärzte eine Brustkrebsprobe auf den Marker HER2 testen, kann das Ergebnis darüber entscheiden, ob eine Patientin leistungsfähige zielgerichtete Medikamente erhält oder nicht. Dennoch verhält sich der Standardfärbetest, die Immunhistochemie, oft eher wie eine Kunst denn wie eine messbare Größe: Verschiedene Labore können zu unterschiedlichen Ergebnissen kommen, und sehr schwache Signale lassen sich besonders leicht übersehen. Diese Studie zeigt, wie man diese Farbreaktion in eine tatsächliche Zahl verwandelt – indem speziell präparierte Zellen hinzugefügt werden, die als eingebaute Maßstäbe dafür dienen, wie viel HER2 auf jeder Tumorzelle vorhanden ist.
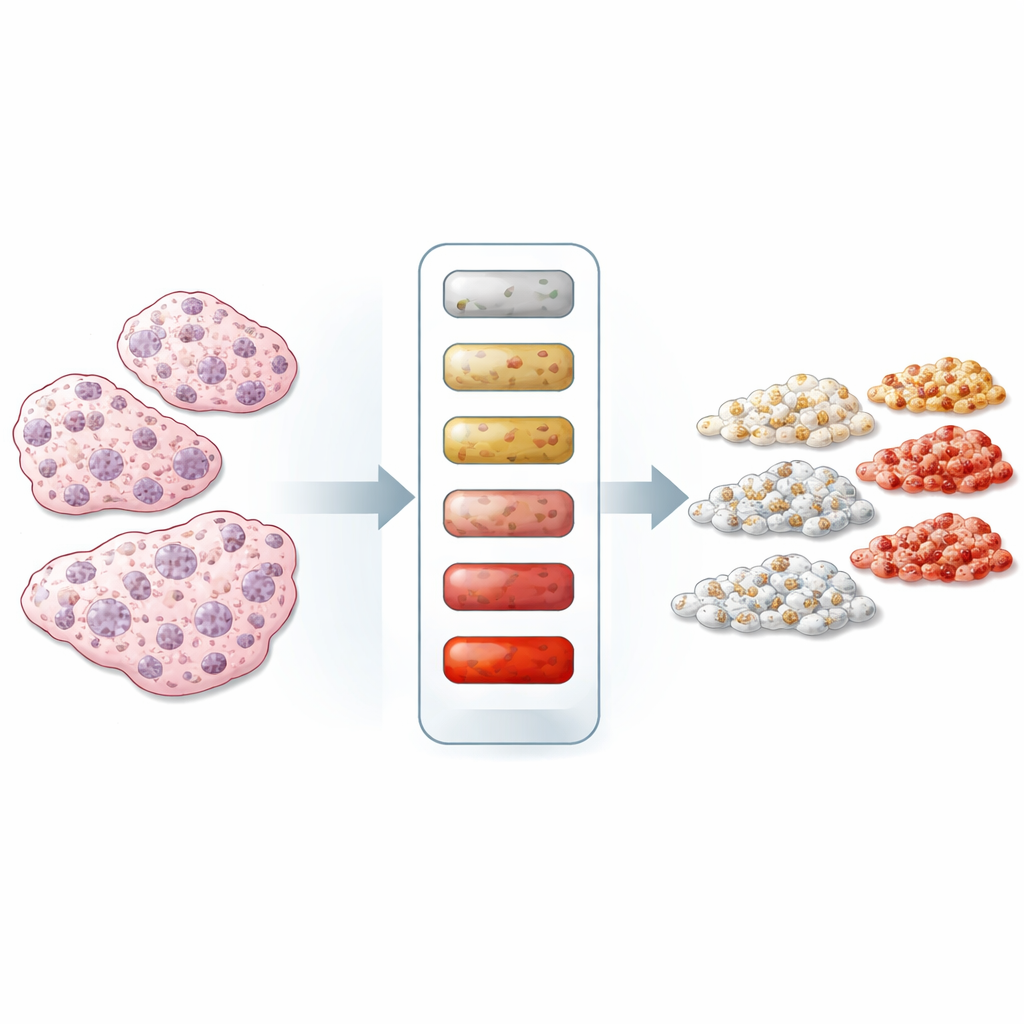
Von Ja‑oder‑Nein zu echten Zahlen
Die meisten derzeitigen färbebasierten Tests klassifizieren HER2 in groben Stufen wie „0“, „1+“, „2+“ oder „3+“. Diese Kategorien sind nützlich, aber grob; sie geben nicht an, wie viele HER2-Rezeptoren auf jeder Krebszelle sitzen, insbesondere in den neuerdings wichtigen Gruppen „HER2-low“ und „HER2-ultralow“. Die Autoren führen an, dass der Hauptgrund für hohe Fehlerquoten das Fehlen quantitativer Maßstäbe innerhalb des Färbeprozesses selbst ist. Andere Labortests, etwa blutbasierte Antikörperassays, stützen sich routinemäßig auf sorgfältig hergestellte Standards und Qualitätskontrollen. Dieselbe Disziplin auf Gewebefärbungen anzuwenden, könnte die Befunde von Pathologen konsistenter machen und eine viel feinere Einstufung der HER2‑Spiegel ermöglichen.
Aufbau zellbasierter Messstäbe
Um solche Standards zu schaffen, wählte das Team ein Panel von Brustkrebszelllinien, die natürlich unterschiedliche Mengen an HER2 tragen, von nahezu keiner bis sehr hoher Expression. Sie nutzten zwei unabhängige Technologien – einen elektrochemilumineszenten Immunoassay, der HER2 in aufgebrochenen Zellen misst, und die Durchflusszytometrie, die Rezeptoren an intakten Zellen zählt –, um jeder Linie eine mittlere Anzahl von HER2‑Rezeptoren pro Zelle zuzuordnen. Die meisten Zelllinien stimmten zwischen den beiden Methoden gut überein, was bestätigte, dass ihr HER2‑Gehalt mit entsprechendem Vertrauen bekannt war, obwohl die Zellen mit sehr hoher HER2‑Expression zwischen den Techniken teilweise abwichen. Diese charakterisierten Zelllinien wurden dann zu „zellulären Kalibratoren“, die genauso verarbeitet und gefärbt werden konnten wie Patientenmaterial.
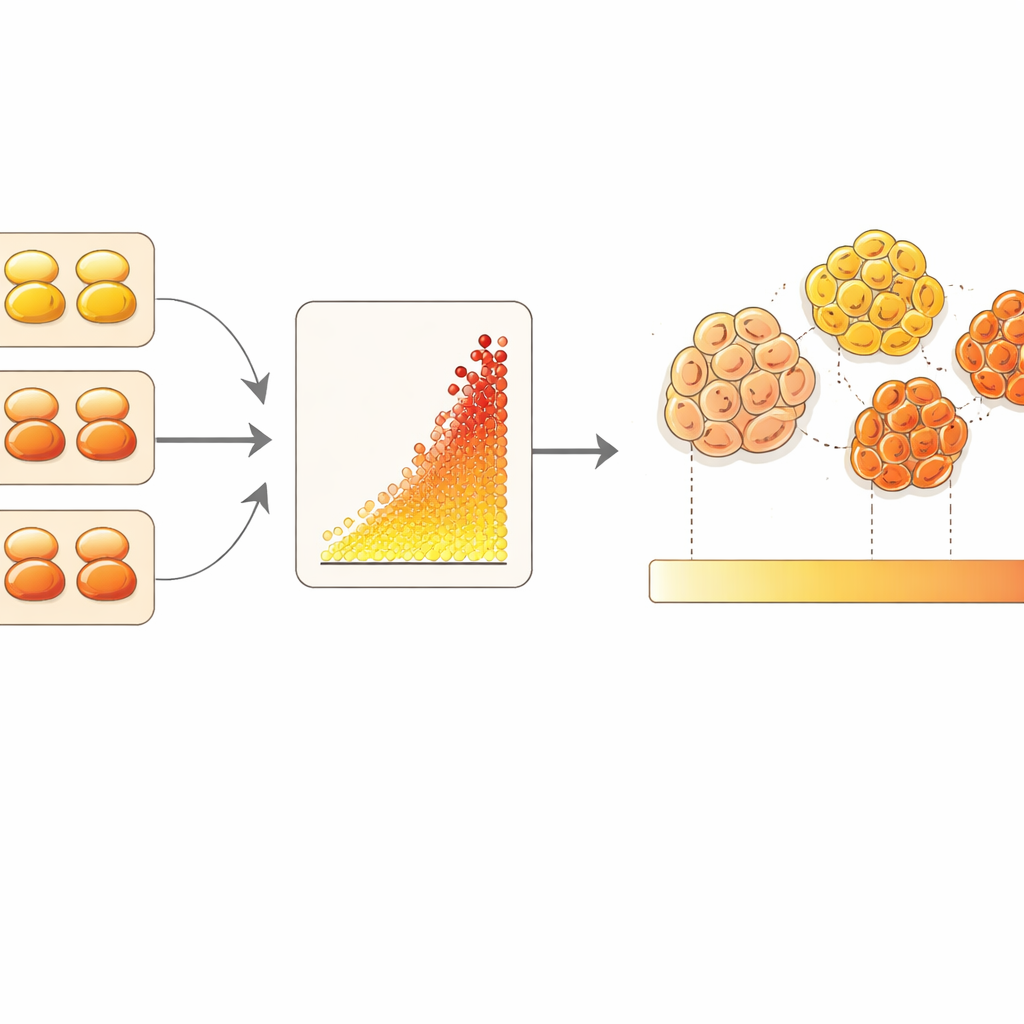
Mikroskopbilder in Zählwerte umwandeln
Die Forscher betteten die Kalibratorzellen in einen Paraffinblock ein, schnitten Schnittpräparate und färbten diese neben einem Microarray von 85 Brustkrebstumoren mit einer sensiblen fluoreszenten Variante des HER2‑Tests. Ein maschinelles Lernverfahren zur Bildanalyse wurde darauf trainiert, Tumorzellen anhand einer separaten Färbung für Strukturproteine zu erkennen und ausschließlich das HER2‑Signal rund um diese Zellen zu messen. Indem sie die bekannten Rezeptorzahlen der Kalibratorzellen gegen deren gemessene Helligkeit auftrugen, erstellte das Team eine Kalibrierkurve. Diese Kurve nutzten sie dann, um die durchschnittliche Helligkeit der Tumorzellen jeder Patientin in eine geschätzte Anzahl von HER2‑Rezeptoren pro Zelle zu übersetzen, über einen brauchbaren Bereich von grob zehn bis nahezu zweihunderttausend Rezeptoren.
Was die neuen Zahlen offenbaren
Als sie diese quantitativen HER2‑Zählungen mit den standardmäßigen klinischen Scores verglichen (unter Verwendung eines häufig eingesetzten Antikörpers namens 4B5), zeigte sich eine überraschend teils invertierte Beziehung: Tumoren mit höherer gemessener Rezeptoranzahl trugen manchmal niedrigere traditionelle Scores und umgekehrt. Viele Proben, die als „HER2 Null“ bezeichnet wurden, wiesen mit der neuen Methode tatsächlich klar messbare HER2‑Level auf. Die Autoren mahnen, dass ihr Assay noch nicht vollständig validiert ist und dass Tumor‑zu‑Tumor‑Variabilität, Unterschiede zwischen Antikörpern und technische Details alle zur Diskrepanz beitragen könnten. Dennoch unterstreichen die Befunde, wie semi‑quantitative Kategorien ein kontinuierliches Spektrum der HER2‑Expression in realen Tumoren verschleiern können.
Versprechen und Hürden für bessere Krebsdiagnostik
Insgesamt zeigt die Arbeit, dass der Einsatz ganzer Zellen als Kalibratoren die HER2‑Färbung in einen numerischen Test verwandeln kann, der anderen regulierten Laborassays ähnlicher ist. Da diese Kalibratorzellen echtes Gewebe nachahmen – sie besitzen Membranen, innere Strukturen und lassen sich auf gleiche Weise färben – bieten sie einen realistischen Maßstab für künftige quantitative Methoden. Gleichzeitig ist der Ansatz anspruchsvoll: er hängt von gut charakterisierten Zelllinien, sorgfältigen Gegenprüfungen mit mehreren Messplattformen sowie klaren Standards für Genauigkeit und Präzision ab. Die Autoren argumentieren, dass, wenn eine solche quantitative Immunhistochemie Behandlungsentscheidungen leiten soll, formale Validierungsrichtlinien und Nachweise für klinischen Nutzen unerlässlich sind, doch zellbasierte Kalibratoren bieten einen praktischen Weg zu diesem Ziel.
Zitation: McKinski, K., Chen, B. Quantitative immunohistochemistry and the use of cellular calibrators for HER2 receptor number determination. Sci Rep 16, 14573 (2026). https://doi.org/10.1038/s41598-026-42898-x
Schlüsselwörter: HER2 Brustkrebs, Immunhistochemie, zelluläre Kalibratoren, Biomarker-Quantifizierung, Qualität diagnostischer Tests