Clear Sky Science · he
CLWD: מאגר פתולוגיה היסטולוגית סיני לסיווג תת‑סוגים של אדנו‑סרטן הריאה
מדוע אוסף תמונות ריאה חדש חשוב
סרטן הריאה נשאר אחד הסרטנים הקטלניים ביותר בעולם, ובסין הוא נוגע ליותר אנשים מאשר בכל מקום אחר. כיום ידוע לרופאים שצורה נפוצה אחת, אדנו‑סרטן הריאה, אינה מחלה יחידה אלא מארג של דפוסי גידול שונים שנושאים סיכונים שונים מאוד לחולה. הבחנה בין דפוסים אלו תחת המיקרוסקופ קשה, אפילו למומחים, ודורשת זמן. מאמר זה מציג מאגר פתוח חדש של תמונות רקמת ריאה איכותיות ממטופלים סינים, שנועד לעזור לחוקרים לבנות כלים ממוחשבים היכולים לזהות את הדפוסים העדינים האלה בעקביות רבה יותר ולתמוך בסופו של דבר באבחון וטיפול מדויקים יותר.
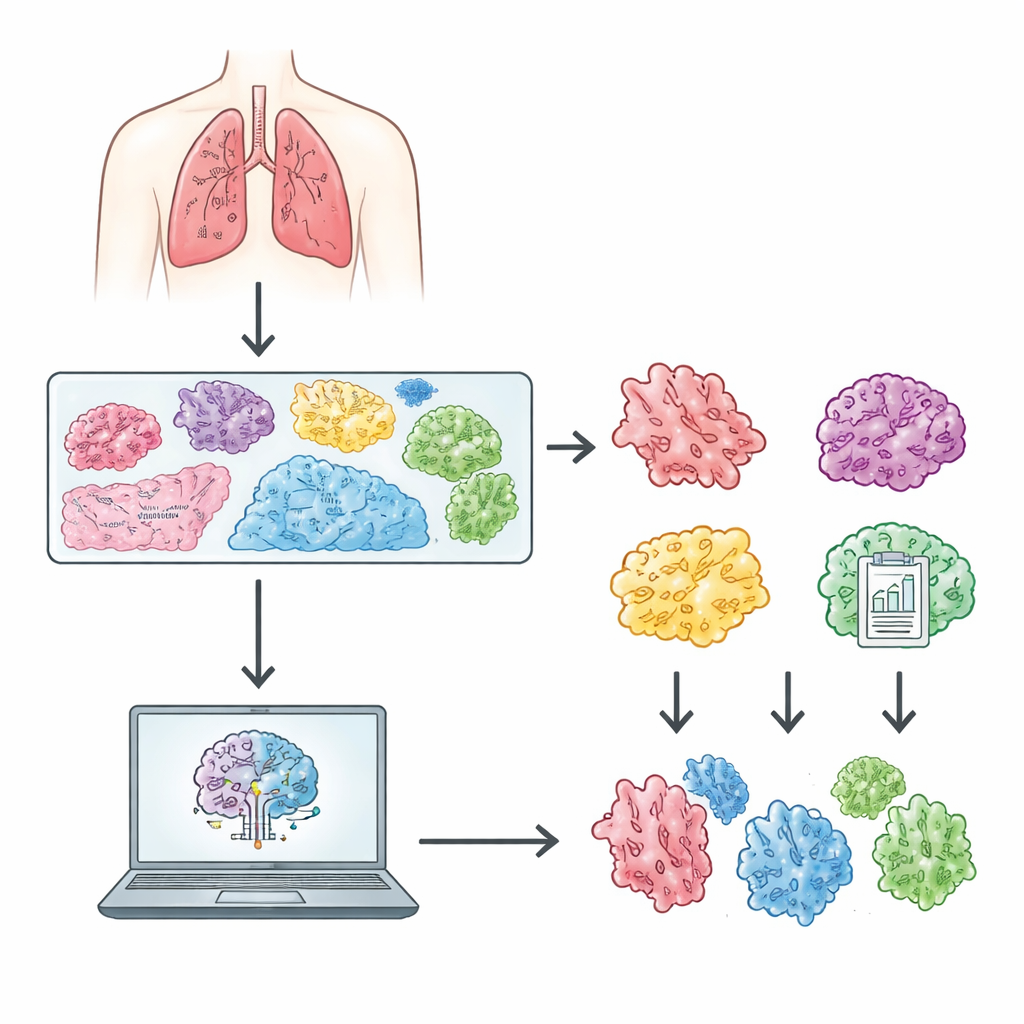
האתגר בתוך הריאה
כאשר מסירים גידול ריאתי מחולה, הפתולוגים חותכים את הרקמה לפרוסות דקות, מצביעים אותן ובוחנים את הפריטים על המיקרוסקופ. באדנו‑סרטן הריאה, הפרוסות הללו חושפות מספר דרכים מובחנות שבהן תאי הגידול גדלים וחודרים: חלק מהדפוסים יחסית עדינים ומשויכים לתוצאים טובים יותר, בעוד אחרים אגרסיביים ומקושרים לסיכונים גבוהים יותר לשחלוף המחלה. ההנחיות הבינלאומיות הנוכחיות מקבצות דפוסים אלה לקטגוריות כגון in situ, acinar, papillary, lepidic, micropapillary, solid ו‑cribriform. זיהוי נכון של הדפוס השולט בגידול מסייע לרופאים להעריך סיכון ולהחליט עד כמה לעקוב או לטפל בחולה. עם זאת, תהליך זה גוזל זמן והוא חשוף לחילוקי דעות בין מומחים.
הפיכת פרוסות זכוכית לנתונים דיגיטליים
התקדמות בסורקי דיגיטציה מאפשרת כיום ללכוד פרוסות מיקרוסקופ בשלמותן כתמונות עצומות ומפורטות שניתן לנתח במחשב. בניית כלים אמינים של בינה מלאכותית דורשת, עם זאת, מאגרים גדולים ותויתיים בקפדנות המשקפים פרקטיקה קלינית אמיתית. המחברים יצרו את מאגר CLWD (Chinese Lung Adenocarcinoma WSI Dataset) על‑ידי איסוף 408 פרוסות צבועות מ‑210 מטופלים שטופלו בבית חולים מרכזי במחוז יונאן בין 2020 ל‑2023. כל פרוסה סורקה בהגדלה גבוהה מאוד, תוך מתן רמת פירוט השווה לזו שמראה פתולוג במיקרוסקופ. פתולוגים מנוסים בתחום סרטן הריאה בחרו מדורים ייצוגיים, אימתו את איכות הצביעה ושלמות הרקמה, והוציאו מכלל שימוש פרוסות שהיו עמומות או שניתן לבלבלן. לצד התמונות רוכזה מידע מנותק מזהות כמו גיל, מין, קטגוריית אבחון ותוויות דפוסי גידול מפורטות התואמות הן למיון ארגון הבריאות העולמי משנת 2015 והן לשנת 2021.
כיצד מחשבים לומדים מהפרוסות
התמונות ב‑CLWD כה גדולות שאי‑אפשר להזין אותן לרשת עצבית בבת אחת. במקום זאת, כל תמונת פרוסה שלמה נחתכת אוטומטית להרבה חתיכות מרובעות קטנות המכילות רק רקמה, תוך סינון רקע ריק ואומללים של סריקה. המחקר משתמש בגישה הידועה כלמידת מופעים מרובים (multiple‑instance learning), שבה כל החתיכות מפרוסה מטופלות כקבוצה. רשת עצבית שאומנה מראש מחלצת תחילה תכונות חזותיות מכל חתיכה, ואז מודלים ייעודיים לומדים לשלב תכונות אלה כדי להחליט איזו תווית תת‑הסוג מתאימה לכל הפרוסה כולה. המחברים העריכו שלוש שיטות מודרניות מבוססות תשומת לב—CLAM, TransMIL ו‑Graph Transformer—כל אחת מתוכננת להתמקד באזורים המידעיים ביותר ובמערכות היחסים בין החתיכות. מסגרת זו מחקה את האופן שבו מומחה בן‑אדם סורק חזותית אזורים שונים של פרוסה לפני קבלת שיפוט כולל.
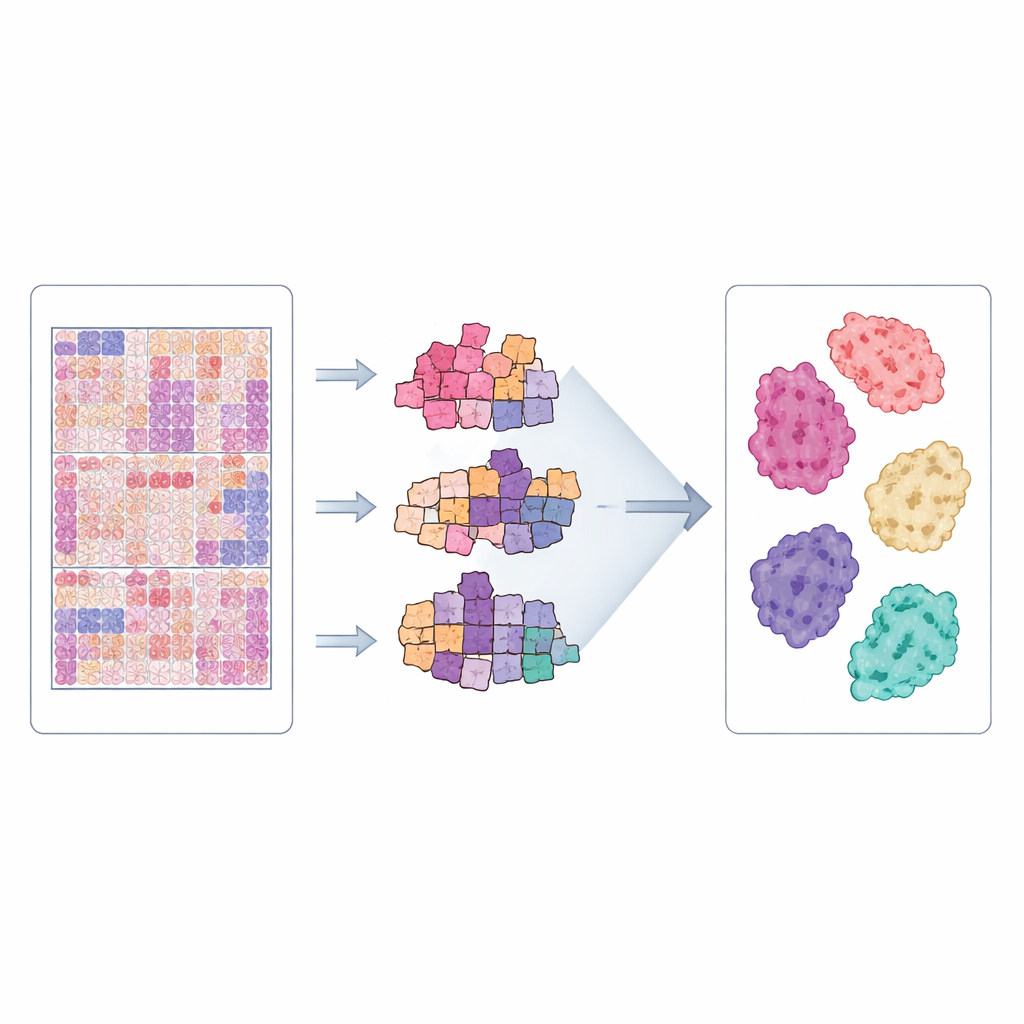
בחינת המאגר במבחן
כדי לבדוק האם CLWD אכן שימושי לאבחון בסיוע מחשב, הצוות ערך ניסויים נרחבים. הם חילקו את המטופלים לקבוצות נפרדות לאימון ולמבחן כך שתמונות מאותו אדם לא יופיעו בשתי הקבוצות, והשתמשו בחצוי‑לצליבת חוזר על מנת לצמצם תנודות אקראיות. שלושת המודלים אומנו להבחין בין שבעה דפוסי גידול וקיבוצים אבחנתיים קשורים. הביצועים נמדדו באמצעות מדדי סטנדרט שבודקים עד כמה המודלים מבדילים תת‑סוג אחד מהאחרים. לאורך ריצות מרובות השיגו המודלים הבחנה גבוהה, במיוחד עבור דפוסים מוגדרים היטב כמו in situ וכמה צורות חודרות, מה שמראה שהמאגר מכיל אותות חזותיים עקביים ולימודיים. כאשר אותן שיטות יושמו על מאגר קיים מארצות הברית Dartmouth, CLWD לעיתים הניב תוצאות שוות או טובות יותר, דבר המצביע על כך שהוא תקן חזק ותוספת חשובה להשוואות בין‑ארציות.
מה המשמעות עבור מטופלים וחוקרים
אוסף ה‑CLWD מציע סט פתוח ומסודר היטב של תמונות סרטן ריאה ממטופלים סינים, וממלא פער במשאבים הקיימים שנבנו בעיקר על גבי קוהורטים מערביים. בזיווג מידע קליני עשיר עם תוויות פרוסה שנבדקו בקפידה, הוא מעניק לחוקרים בסיס מוצק לפיתוח והשוואת מערכות בינה מלאכותית לגילוי מוקדם ולהעמקת תתי‑הסיווג של אדנו‑סרטן הריאה. אמנם למאגר יש מגבלות — הוא מגיע מבית חולים יחיד, חלק מתתי‑הסוגים נדירים יותר ורק צביעה סטנדרטית נכללה — אך הוא עדיין מייצג צעד משמעותי לקראת פתולוגיה מונעת נתונים שכוללת יותר אוכלוסיות. ככל שכלים עתידיים המאומנים על CLWD ומאגרים דומים יתפתחו, הם עשויים לסייע לפתולוגים לזהות דפוסים בעלי סיכון גבוה ביתר אמינות, לכוון מעקב וטיפול, ולשפר בסופו של דבר תוצאות עבור אנשים המתמודדים עם סרטן ריאה.
ציטוט: Chen, Y., Zhao, H., Wang, L. et al. CLWD: a Chinese histopathology dataset for lung adenocarcinoma subtype classification. Sci Data 13, 599 (2026). https://doi.org/10.1038/s41597-026-06906-z
מילות מפתח: אדנו‑סרטן ריאה, פתולוגיה דיגיטלית, דימות היסטופתולוגי, למידה עמוקה, תת‑סוגי סרטן