Clear Sky Science · he
המבנה והדינמיקה של PARP1-HPF1 על דנ"א עם חתכים מרמזים על מנגנון של ADP-ריבוזילציה חדה וממוקדת
כיצד תאים חשים שברים זעירים ב‑DNA שלהם
כל תא בגופך נתון כל הזמן לפגיעות שגורמות לקרעים או לשחיקה ב‑DNA. אם נזקי אלו לא יזוהו ויתוקנו במהירות, הם עלולים להוביל למוטציות ולבסוף לסרטן. המחקר הזה מגלה כיצד אחד מהמשתתפים הראשונים במערך התיקון של התא — חלבון בשם PARP1 העובד יחד עם חלבון שותף HPF1 — מזהה קרע זעיר ב‑DNA ואז מעמיד במהירות תגיות כימיות על חלבונים בסביבה. תגיות אלה פועלות כמו אות חזק, או אות אש, המטיל וקליטת צוות התיקון בדיוק במקום שבו הוא נדרש.
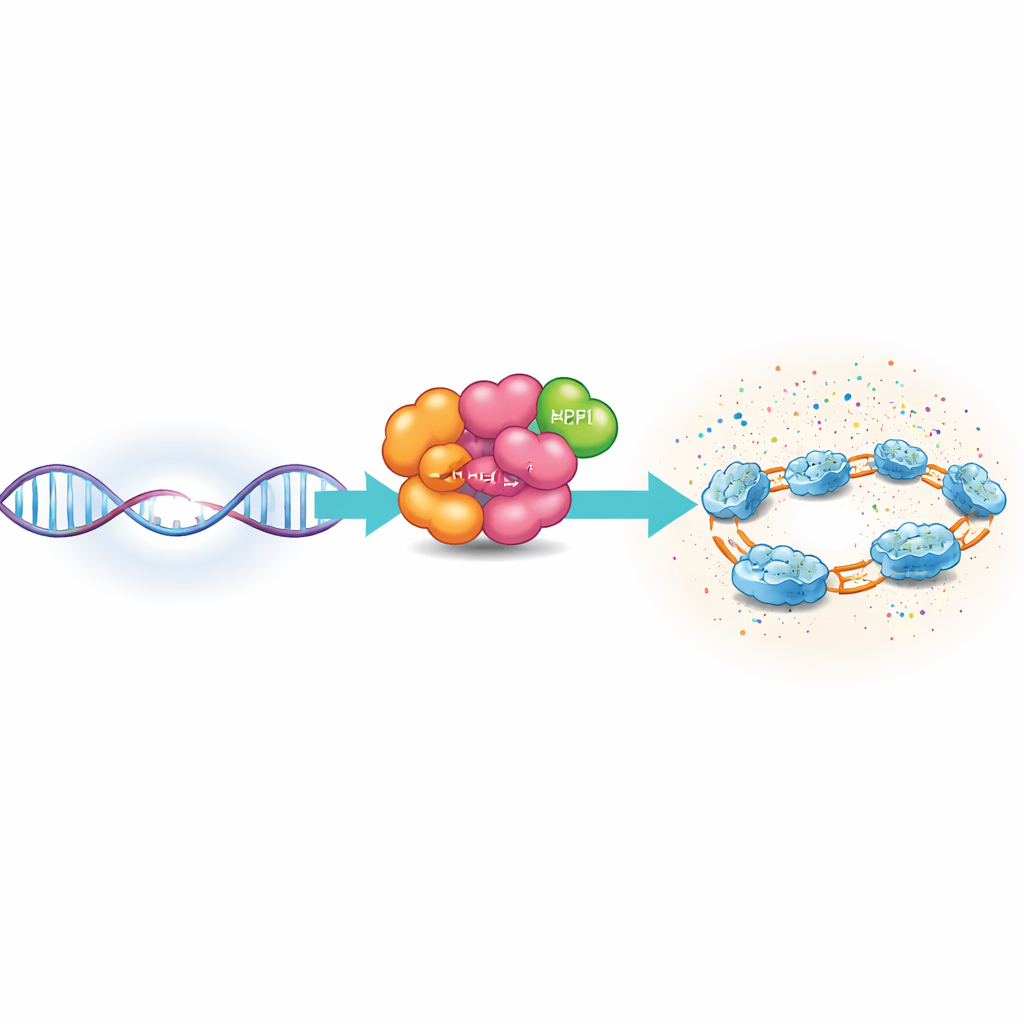
משהו כמגיב ראשון מולקולרי בפעולה
PARP1 הוא חלבון שומר בשפע שסורק את ה‑DNA אחרי נזק. כשהוא נתקל בסדק של גדיל בודד — חתך רק באחד משני גדילי ה‑DNA — PARP1 מתיישב על החתך באמצעות מספר אזורים מיוחדים המחזיקים את ה‑DNA. לאחר הפעלתו משתמש PARP1 במולקולת דלק תאית, NAD+, כדי לבנות שרשראות של ADP‑ריבוז על עצמו ועל חלבונים סמוכים, בעיקר על היסטונים שמסייעים באריזת ה‑DNA לכרומטין. המודיפיקציות הללו מרפות באופן זמני את מבנה הכרומטין המקומי ומושכות גורמי תיקון, ויוצרות אזור תיקון ממוקד בחוזקה סביב האתר הפגוע.
לראות את המכשיר המלא על ה‑DNA השבור
עד כה, רוב הצילומי המבנה של PARP1 הראו רק חלקים מהחלבון, והשאירו פתוחה השאלה כיצד המולקולה המלאה מורכבת על קרע ב‑DNA יחד עם שותפיה. החוקרים השתמשו בקריו‑אלקטרון מיקרוסקופיה של חלקיקים בודדים, טכניקה שמדמת מולקולות קפואות ברזולוציה כמעט אטומית, כדי להציף את תמונת PARP1 המלא קשור ליצירת דנ"א חתוכה יחד עם HPF1 וקוטרן של חלבון שותף נוסף בשם Timeless. הם שילבו תמונות אלה עם ניסויי פלואורסצנציה לחלקיק יחיד ומדידות פיזור בפתרון כדי להבין לא רק את המבנה, אלא גם את התנועה של המורכב בפעולה.
כיפוף ה‑DNA וארגון התשתית
התמונות מגלה כי מספר אזורים של PARP1 מהדקים סביב החתך וכופפים בחדות את ה‑DNA בכ־75 מעלות. שלושה מקטעי אצבע‑אבץ (zinc‑finger) ודומיין WGR יוצרים סקלפט רופף אך מתואם שמעגן את PARP1 ישירות על הקרע. אזור סמוך שנקרא הדומיין ההלי כלי (helical domain) מצטרף להרכבה זו ועוזר לייצב את המצב הקשור ל‑DNA. יחד החלקים הללו יוצרים עוגן קשיח באתר הנזק, בעוד שחלקים אחרים של PARP1 — ובפרט דומיין BRCT שנמצא יותר במרכז החלבון — נשארים גמישים ולעתים בלתי נראים בתמונות, מה שמעיד שהם נעים בחופשיות גם כאשר ליבת הקשירה ל‑DNA נעולה במקומה.
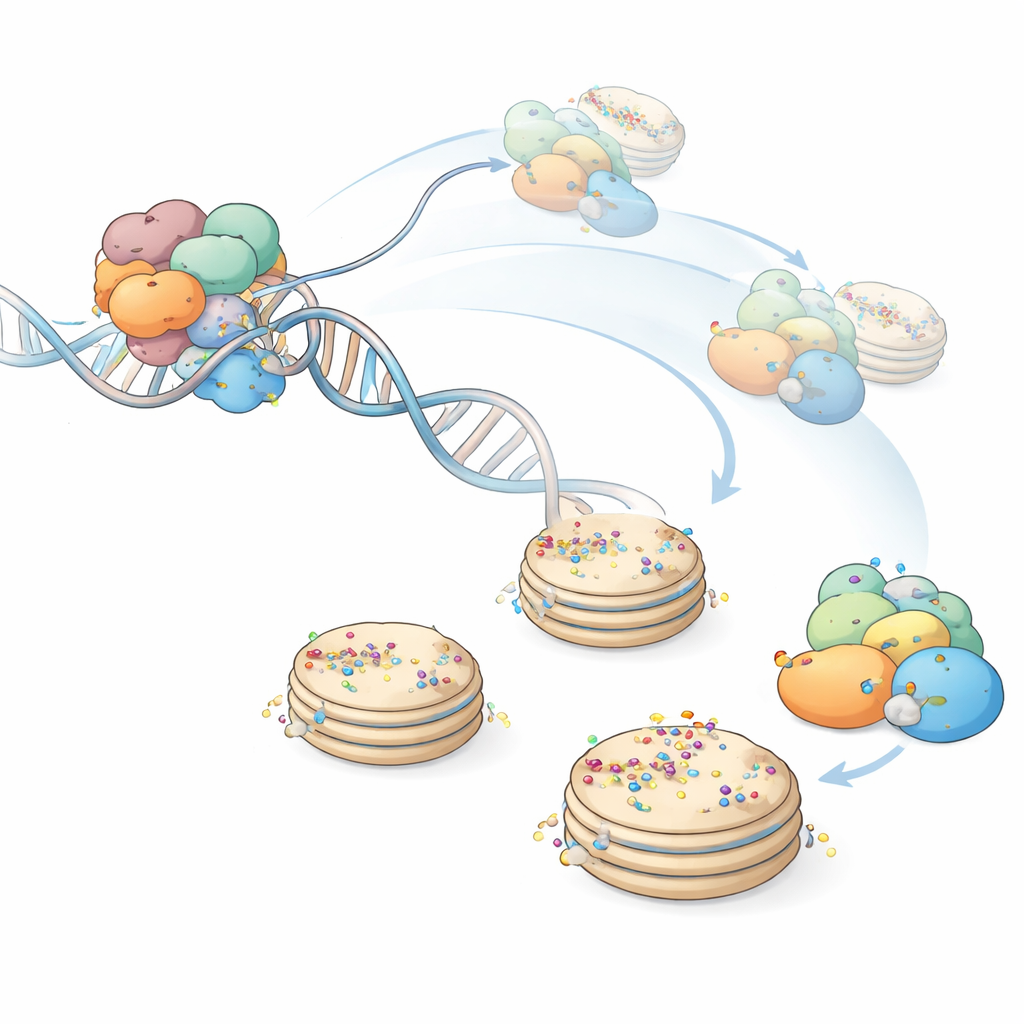
זרוע קטליטית על רצועה גמישה
הממצא הבולט ביותר הוא מה שקורה לאזור הקטליטי של PARP1, החלק שבאופן מעשי בונה את שרשראות ה‑ADP‑ריבוז. במבני קריסטל מוקדמים אזור זה ישב דבוק צמוד לדומיין ההלי כלי במצב "כבוי" שחסם גישה ל‑NAD+. בתצפיות הקריו‑EM החדשות, ברגע ש‑PARP1 מאורגן במלואו על דנ"א חתוך, הבלוק הקטליטי מתנתק במידה רבה משכנו ההלי כלי והופך לנייד מאד, כשהוא נשאר מחובר רק באמצעות קישורים גמישים. HPF1 נקשר ישירות לאזור הקטליטי הנייד הזה ומעצב מחדש את האתר הפעיל כך שסרינים בהיסטונים הופכים למטרות מועדפות. מדידות פלואורסצנציה של חלקיק יחיד מאששות כי קשירת תרכובת המדמה NAD+ גם מייצבת את PARP1 על ה‑DNA וגם מפחיתה תנודות בכיפוף ה‑DNA, בהתאם למצב מושהה אך דינמי של הזרוע הקטליטית.
להבה כימית מקומית אך חזקה
על ידי שילוב הדמיה מבנית, דינמיקות של חלקיק יחיד ופיזור בפתרון, החוקרים מציעים מודל שבו הקשירה לקרע ב‑DNA מארגנת את חצי הנקודה N‑ של PARP1 לקלאמפ קשיח בעוד שהיא משחררת את האזור הקטליטי בקצה האחר כדי להתנודד על "רצועה". זרוע קטליטית ניידת אך פעילה ללא הרף זו, בשותפות עם HPF1, יכולה לתייג במהירות את PARP1 עצמו ואת היסטונים סמוכים בשרשראות ADP‑ריבוז בטווח מוגבל סביב החתך. התוצאה היא פרץ אותות חד אך ממוקד מאוד שמעצב מחדש את הכרומטין ומגייס גורמי תיקון בדיוק במקום הנדרש, מסייעת לתאים לשמור על יציבות הגנום תוך מזעור הפרעה מיותרת באזורים אחרים בגרעין.
ציטוט: Sverzhinsky, A., Xue, H., Langelier, MF. et al. PARP1-HPF1 structure and dynamics on nicked DNA suggest a mechanism for acute and localized ADP-ribosylation. Nat Commun 17, 2825 (2026). https://doi.org/10.1038/s41467-026-69375-3
מילות מפתח: תיקון DNA, PARP1, ADP-ריבוזילציה, קריו-EM, כרומטין