Clear Sky Science · fr
Deux solvants avec des forces de coordination différentes pour des électrolytes localement à haute concentration dans les batteries au lithium métallique
De meilleures batteries pour la vie quotidienne
Les batteries au lithium métallique promettent des téléphones dont la charge tient plusieurs jours et des voitures électriques qui parcourent bien plus de distance entre deux arrêts. Pourtant, ces batteries puissantes sont freinées par le liquide qui les traverse — l’électrolyte — qui peut endommager progressivement les composants internes. Cet article explore une nouvelle recette d’électrolyte pour permettre aux batteries au lithium métallique de fonctionner à des tensions plus élevées, de fournir plus d’énergie et de supporter des centaines de cycles charge–décharge sans défaillir.
Pourquoi le lithium métallique est si difficile à maîtriser
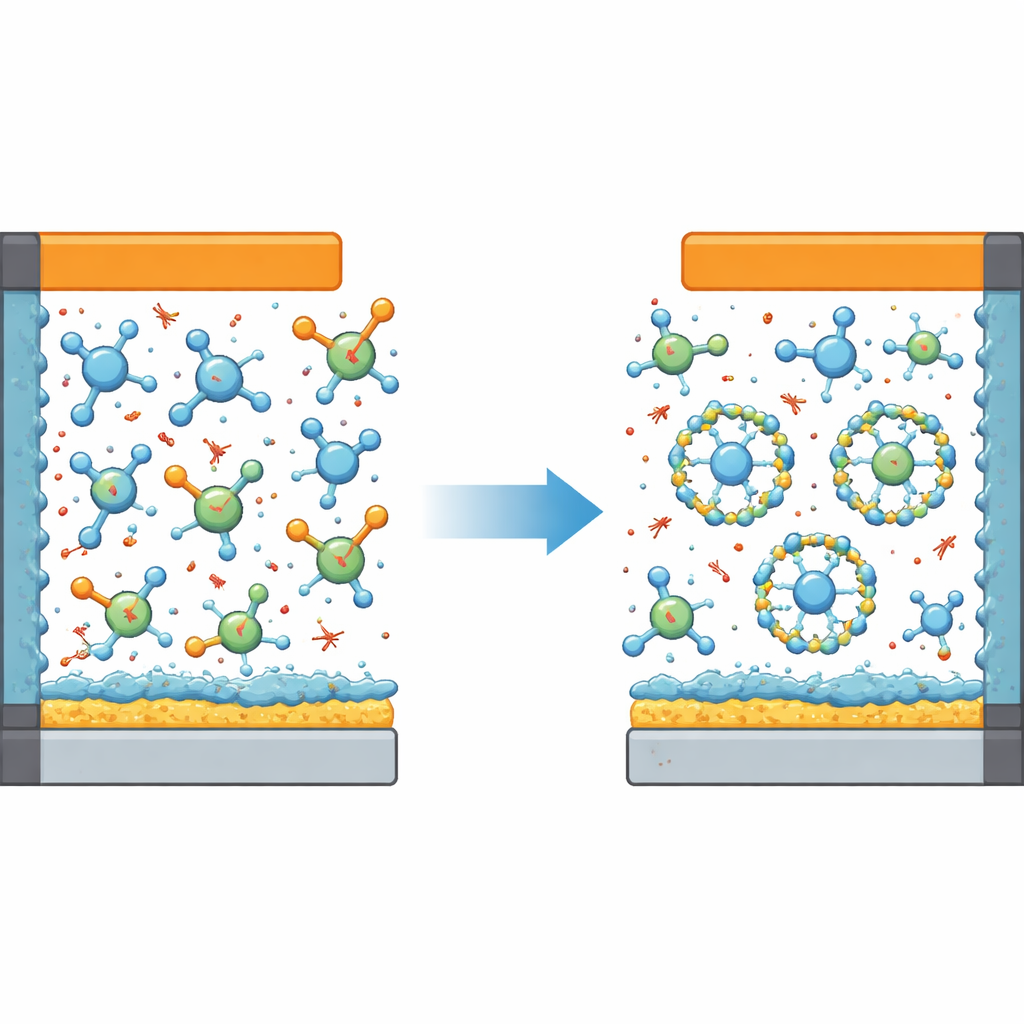
Le lithium métallique est un matériau de batterie idéal car il stocke beaucoup d’énergie dans un volume et un poids faibles. Mais il est aussi très réactif. Lors des cycles de charge et de décharge, le lithium métallique peut croître en structures en aiguilles et réagir avec le liquide qui l’entoure, gaspillant du lithium et risquant des courts‑circuits. Les conceptions modernes cherchent à contrôler ce comportement en ajustant finement l’électrolyte pour qu’il forme des couches protectrices minces à la fois sur l’anode au lithium et sur la cathode à haute tension. Une approche populaire, appelée électrolyte localement à haute concentration, rassemble les anions négatifs près des ions lithium, favorisant la formation de films protecteurs riches en composés inorganiques robustes comme le fluorure de lithium et l’oxyde de lithium.
Le problème caché d’un solvant de référence
Beaucoup de ces électrolytes avancés reposent sur un solvant courant, le diméthoxyéthane (DME), qui solvate très bien les ions lithium et facilite la charge rapide. Malheureusement, le DME se dégrade facilement aux tensions élevées utilisées avec des cathodes à haute densité énergétique, comme le NCM811 riche en nickel. Dans les formulations conventionnelles, certaines molécules de DME ne sont pas fortement liées au lithium ; elles errent librement, en particulier près de la cathode et du collecteur de courant en aluminium. Là, elles se décomposent ou provoquent la corrosion des surfaces métalliques, consommant de la capacité et raccourcissant la durée de vie de la batterie. Réduire simplement la teneur en DME n’est pas suffisant, car trop peu de DME ralentit le mouvement des ions et nuit aux performances de la batterie.
Un troisième ingrédient qui remet de l’ordre
Les chercheurs ont abordé ce dilemme en ajoutant un troisième liquide soigneusement conçu : un éther fortement fluoré à coordination faible appelé HFMTFP. Leur nouvel électrolyte « ternaire » combine le DME, un diluant fluoré non solvatisant et le HFMTFP. Des simulations informatiques et des mesures spectroscopiques montrent que le HFMTFP modifie subtilement l’environnement microscopique autour des ions lithium. Le DME reste enfermé dans le voisinage immédiat du lithium, tandis que le HFMTFP concurrence juste assez pour ralentir les échanges constants de molécules de DME entrant et sortant. Cette hiérarchie énergétique supprime la population de molécules de DME libres qui, autrement, erreraient et se décomposeraient à haute tension.
Des couches protectrices auto‑formées sur les deux électrodes
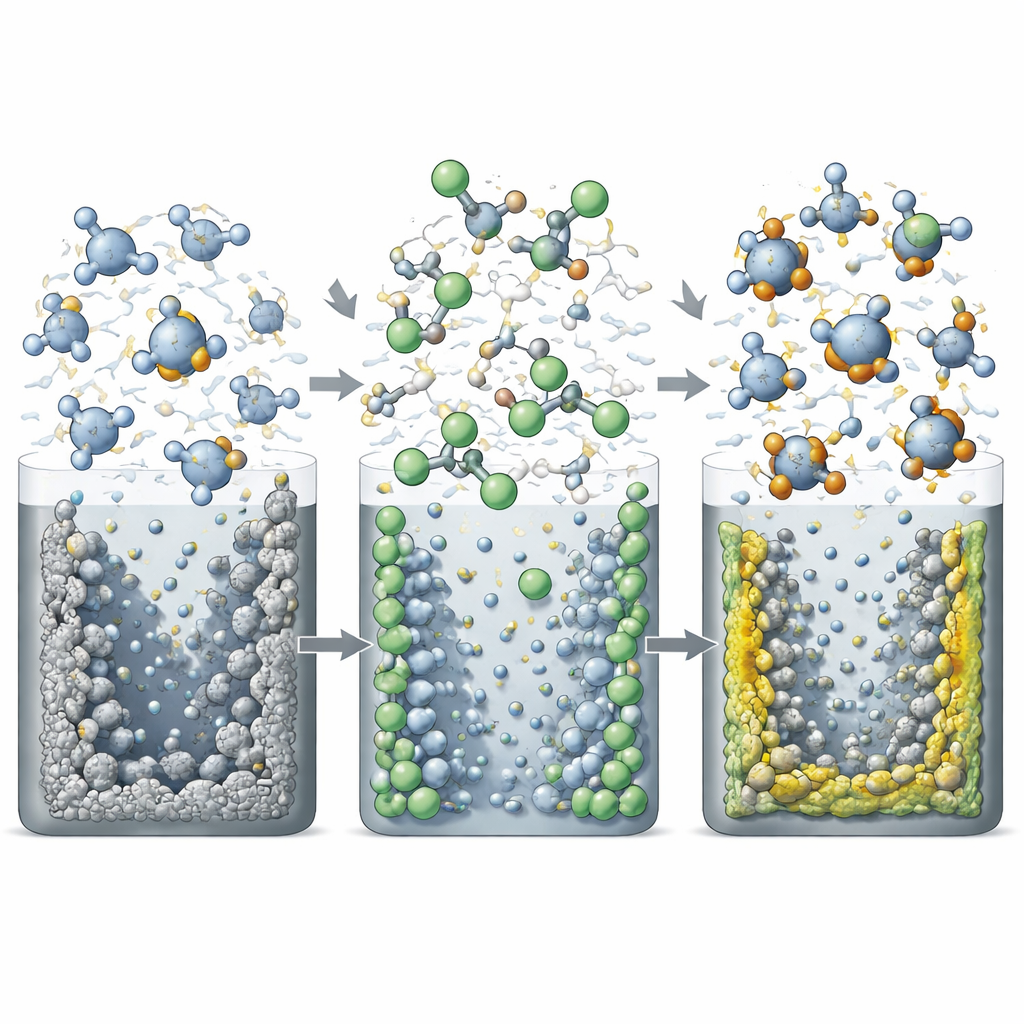
Le HFMTFP joue aussi un second rôle crucial. En raison de sa structure fluorée et de son comportement différent lorsqu’il est libre par rapport à lié au lithium, il se décompose préférentiellement sur les deux électrodes d’une manière qui s’avère bénéfique. À la surface du lithium métallique, le HFMTFP coordonné et l’anion du sel se décomposent en composés inorganiques riches en fluorure de lithium et en oxyde de lithium, formant une couche protectrice mince, uniforme et mécaniquement résistante. À la cathode NCM811 à haute tension, le HFMTFP libre s’oxyde pour former un revêtement riche en fluor qui protège le matériau actif de l’électrolyte agressif. Les mesures confirment que ces revêtements sont plus inorganiques et plus riches en fluor que ceux formés dans des électrolytes standard, et la microscopie montre que les dépôts de lithium restent compacts plutôt que de croître en structures fragiles et mousseuses.
Des performances durables sous contrainte réaliste
Pour vérifier si cet ajustement moléculaire a un impact réel, l’équipe a testé des cellules complètes au lithium métallique avec des cathodes NCM811 dans des conditions exigeantes : haute tension (jusqu’à 4,4 V), courant élevé (le double du taux normal) et charge en matériau actif réaliste. Par rapport à des électrolytes plus simples, la formulation ternaire a fortement réduit la corrosion de l’aluminium et les réactions secondaires à haute tension. Les cellules utilisant le nouvel électrolyte ont conservé plus de 90 % de leur capacité initiale après 250 cycles rapides de charge–décharge, tandis que les versions conventionnelles perdaient bien en dessous de ce seuil beaucoup plus tôt. Des sondes structurelles de la cathode ont révélé que son réseau cristallin stratifié est resté remarquablement intact, indiquant que le revêtement protecteur a efficacement bloqué les changements dommageables à l’intérieur du matériau.
Ce que cela signifie pour les appareils futurs
En substance, l’étude montre qu’ajouter un cosolvant fluoré à interaction modérée à l’électrolyte peut canaliser un solvant réactif mais utile comme le DME, l’empêchant de se comporter mal tout en transformant son partenaire en constructeur de films protecteurs. En concevant la manière dont les molécules s’organisent autour des ions lithium, les chercheurs ont créé un électrolyte qui résiste à la dégradation à haute tension et forme naturellement des peaux solides et inorganiques sur les électrodes de la batterie. Cette stratégie rapproche les batteries au lithium métallique d’une utilisation quotidienne dans des véhicules électriques longue portée et des appareils portables haut de gamme, où la durabilité et la sécurité doivent être à la hauteur de leur remarquable densité énergétique.
Citation: Kim, J., Lee, K., Kim, I. et al. Dual solvents with different coordination strengths for localized high concentration electrolytes in lithium metal batteries. npj Energy Mater. 1, 2 (2026). https://doi.org/10.1038/s44456-025-00002-0
Mots-clés: batteries au lithium métallique, conception d’électrolyte, cathodes à haute tension, solvants fluorés, durée de vie des batteries