Clear Sky Science · de
Duale Lösungsmittel mit unterschiedlicher Koordinationsstärke für lokal hochkonzentrierte Elektrolyte in Lithium‑Metall‑Batterien
Bessere Batterien für den Alltag
Lithium‑Metall‑Batterien versprechen Smartphone‑Ladungen, die mehrere Tage halten, und Elektroautos mit deutlich größerer Reichweite zwischen den Ladestopps. Dennoch werden diese leistungsstarken Batterien durch die Flüssigkeit in ihrem Inneren — den Elektrolyten — ausgebremst, die die inneren Bauteile langsam schädigen kann. Diese Arbeit untersucht eine neue Rezeptur für diesen Elektrolyten, damit Lithium‑Metall‑Batterien mit höheren Spannungen betrieben werden können, mehr Energie liefern und Hunderte Lade‑/Entladezyklen überstehen, ohne auszufallen.
Warum Lithium‑Metall so schwer zu bändigen ist
Lithium‑Metall ist ein ideales Batterie‑Material, weil es viel Energie in einem kleinen, leichten Paket speichert. Gleichzeitig ist es sehr reaktiv. Beim Laden und Entladen kann sich Lithium in nadelartige Strukturen ausbilden und mit der umgebenden Flüssigkeit reagieren, wodurch Lithium verschwendet wird und Kurzschlüsse drohen. Moderne Konzepte versuchen, dieses Verhalten zu kontrollieren, indem der Elektrolyt so abgestimmt wird, dass sich dünne Schutzschichten auf sowohl der Lithiumanode als auch der Hochvolt‑Kathode bilden. Ein populärer Ansatz, der als lokal hochkonzentrierter Elektrolyt bezeichnet wird, bringt negativ geladene Ionen dicht an Lithiumionen heran und fördert so Schutzfilme, die reich an widerstandsfähigen anorganischen Verbindungen wie Lithiumfluorid und Lithiumoxid sind.
Das verborgene Problem eines Standard‑Lösungsmittels
Viele dieser fortgeschrittenen Elektrolyte beruhen auf einem gebräuchlichen Lösungsmittel, Dimethoxyethan (DME), das Lithiumionen sehr gut solvatisiert und schnelles Laden unterstützt. Unglücklicherweise zersetzt sich DME bei den hohen Spannungen, die bei energiedichten Kathoden wie nickelreichen NCM811 verwendet werden, leicht. In konventionellen Formulierungen sind einige DME‑Moleküle nicht fest an Lithium gebunden; sie bewegen sich frei, besonders in der Nähe der Kathode und des Aluminium‑Stromsammelns. Dort zersetzen sie sich oder korrodieren Metalloberflächen, was Kapazität mindert und die Lebensdauer verkürzt. Eine bloße Reduzierung des DME‑Anteils reicht nicht aus, denn zu wenig DME verlangsamt den Ionentransport und verschlechtert die Batterieleistung.
Eine dritte Zutat, die Ordnung schafft
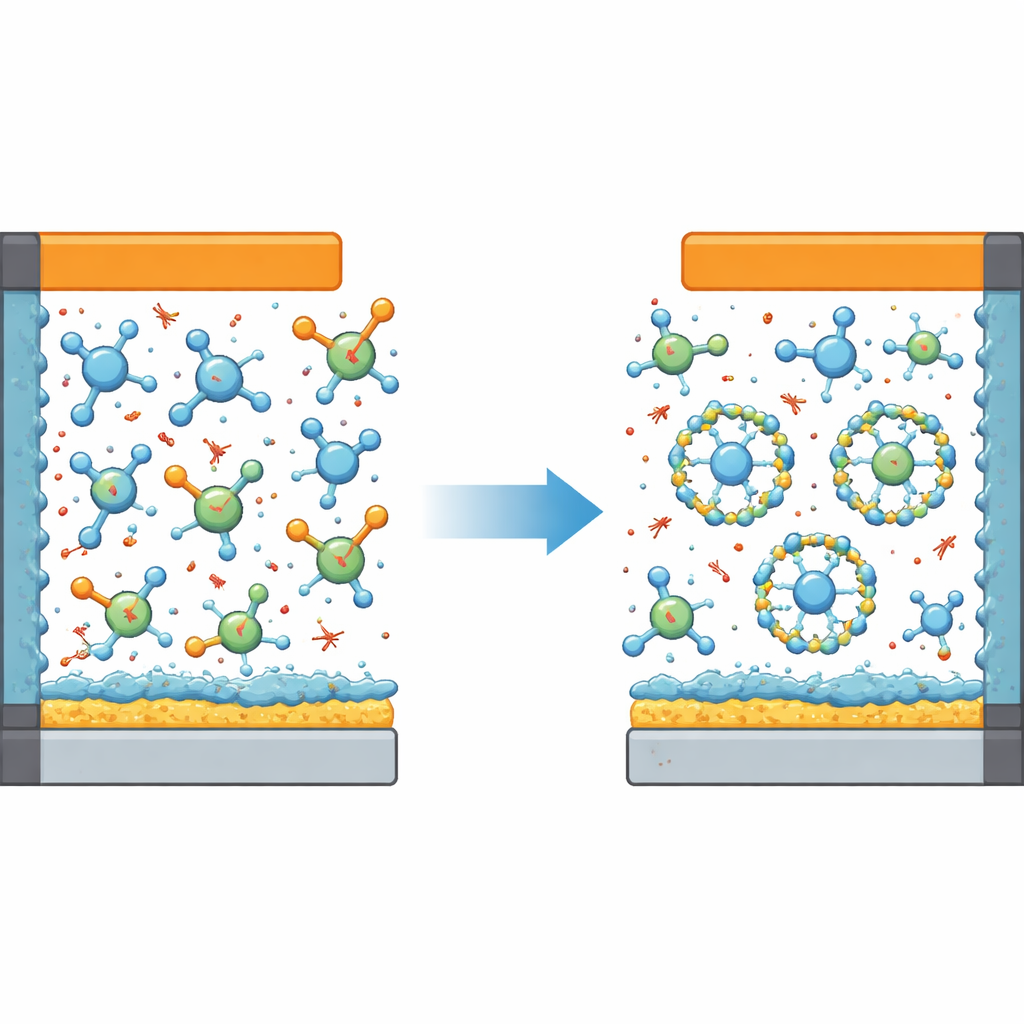
Die Forschenden gingen dieses Dilemma an, indem sie der Mischung eine gezielt gestaltete dritte Flüssigkeit hinzufügten: einen schwach koordinierenden, stark fluorierten Ether namens HFMTFP. Der neue „ternäre“ Elektrolyt kombiniert DME, ein nicht‑lösungsmittel‑wirksames fluoriertes Verdünnungsmittel und HFMTFP. Computersimulationen und spektroskopische Messungen zeigen, dass HFMTFP die mikroskopische Umgebung um Lithiumionen subtil umgestaltet. DME bleibt in der unmittelbaren Umgebung des Lithiums gebunden, während HFMTFP gerade genug konkurriert, um das ständige Austauschen von DME‑Molekülen hinein und heraus zu verlangsamen. Diese energetische Hierarchie unterdrückt die Population freier DME‑Moleküle, die andernfalls umherschweifen und bei hohen Spannungen zerfallen würden.
Selbstbildende Schutzschichten an beiden Elektroden
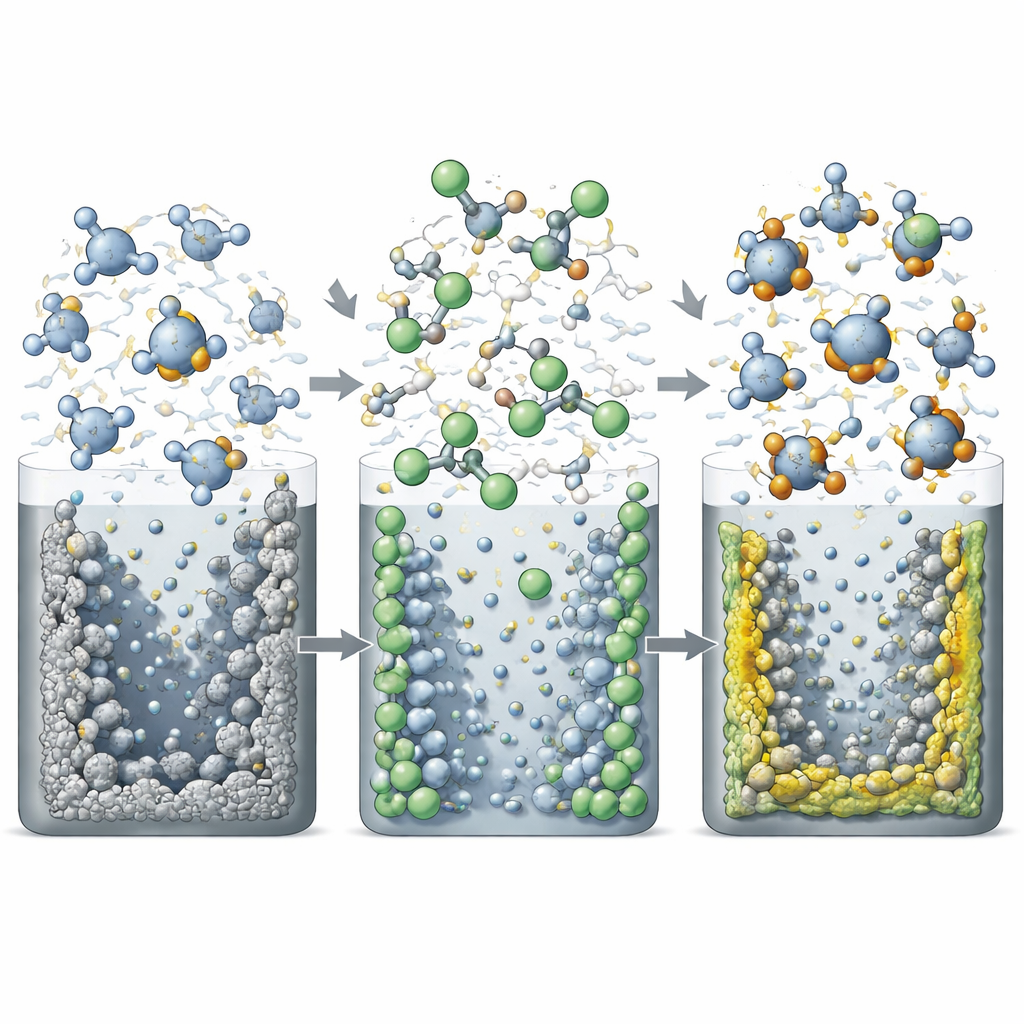
HFMTFP erfüllt zudem eine zweite, entscheidende Funktion. Wegen seiner fluorierten Struktur und seines unterschiedlichen Verhaltens, wenn es frei gegenüber gebunden an Lithium vorliegt, zersetzt es sich bevorzugt an beiden Elektroden auf eine Weise, die tatsächlich nützlich ist. An der Oberfläche des Lithium‑Metalls zerfallen koordiniertes HFMTFP und das Anion im Salz zu anorganischen Verbindungen, die reich an Lithiumfluorid und Lithiumoxid sind, und bilden eine dünne, gleichmäßige und mechanisch stabile Schutzschicht. An der hochvoltigen NCM811‑Kathode oxidiert freies HFMTFP zu einer fluorreichen Beschichtung, die das aktive Material vor dem aggressiven Elektrolyten abschirmt. Messungen bestätigen, dass diese Beschichtungen anorganischer und fluorreicher sind als die in Standard‑Elektrolyten gebildeten, und die Mikroskopie zeigt, dass Lithiumablagerungen kompakt bleiben, statt in fragil‑moosartige Strukturen zu wachsen.
Langlebige Performance unter realistischen Belastungen
Um zu prüfen, ob diese molekulare Feineinstellung in der Praxis tatsächlich relevant ist, testete das Team vollständige Lithium‑Metall‑Zellen mit NCM811‑Kathoden unter anspruchsvollen Bedingungen: hoher Spannung (bis zu 4,4 V), hohem Strom (doppelte Normalrate) und realistischer Beschickung des aktiven Materials. Im Vergleich zu einfacheren Elektrolyten reduzierte die ternäre Formulierung die Aluminiumkorrosion und hochvoltige Nebenreaktionen deutlich. Zellen mit dem neuen Elektrolyten behielten nach 250 schnellen Lade‑/Entladezyklen mehr als 90 % ihrer ursprünglichen Kapazität, während konventionelle Varianten deutlich früher weit darunter lagen. Strukturuntersuchungen der Kathode zeigten, dass ihr geschichtetes Kristallgerüst bemerkenswert intakt blieb, was darauf hinweist, dass die Schutzschicht schädliche Veränderungen tief im Material erfolgreich blockierte.
Was das für zukünftige Geräte bedeutet
Im Kern zeigt die Studie, dass ein mäßig wechselwirkendes, fluoriertes Kovolvent dem Elektrolyten beigemischt werden kann, um ein reaktives, aber nützliches Lösungsmittel wie DME zu bändigen — es daran zu hindern, sich fehlzuverhalten — und gleichzeitig dessen Partner in den Bau schützender Filme zu verwandeln. Durch das gezielte Gestalten der molekularen Anordnung um Lithiumionen schufen die Forschenden einen Elektrolyten, der sowohl dem Abbau bei hohen Spannungen widersteht als auch auf natürliche Weise starke, anorganische Schichten auf den Elektroden bildet. Diese Strategie rückt Lithium‑Metall‑Batterien einen Schritt näher an den Alltagseinsatz in Reichweitenstarken Elektrofahrzeugen und hochwertigen tragbaren Geräten, wo Haltbarkeit und Sicherheit mit ihrer beeindruckenden Energiedichte mithalten müssen.
Zitation: Kim, J., Lee, K., Kim, I. et al. Dual solvents with different coordination strengths for localized high concentration electrolytes in lithium metal batteries. npj Energy Mater. 1, 2 (2026). https://doi.org/10.1038/s44456-025-00002-0
Schlüsselwörter: Lithium‑Metall‑Batterien, Elektrolyt‑Design, Hochvolt‑Kathoden, fluorierte Lösungsmittel, Batterie‑Zyklenfestigkeit