Clear Sky Science · es
Disolventes duales con diferentes fuerzas de coordinación para electrolitos de alta concentración localizada en baterías de litio metálico
Mejores baterías para la vida cotidiana
Las baterías de litio metálico prometen cargas de teléfono que duran días y coches eléctricos que recorren mucho más entre paradas. Sin embargo, estas baterías potentes están limitadas por el líquido en su interior —el electrolito— que puede dañar lentamente las partes internas de la batería. Este artículo explora una nueva receta para ese electrolito para que las baterías de litio metálico funcionen a voltajes más altos, entreguen más energía y sobrevivan a cientos de ciclos de carga y descarga sin fallar.
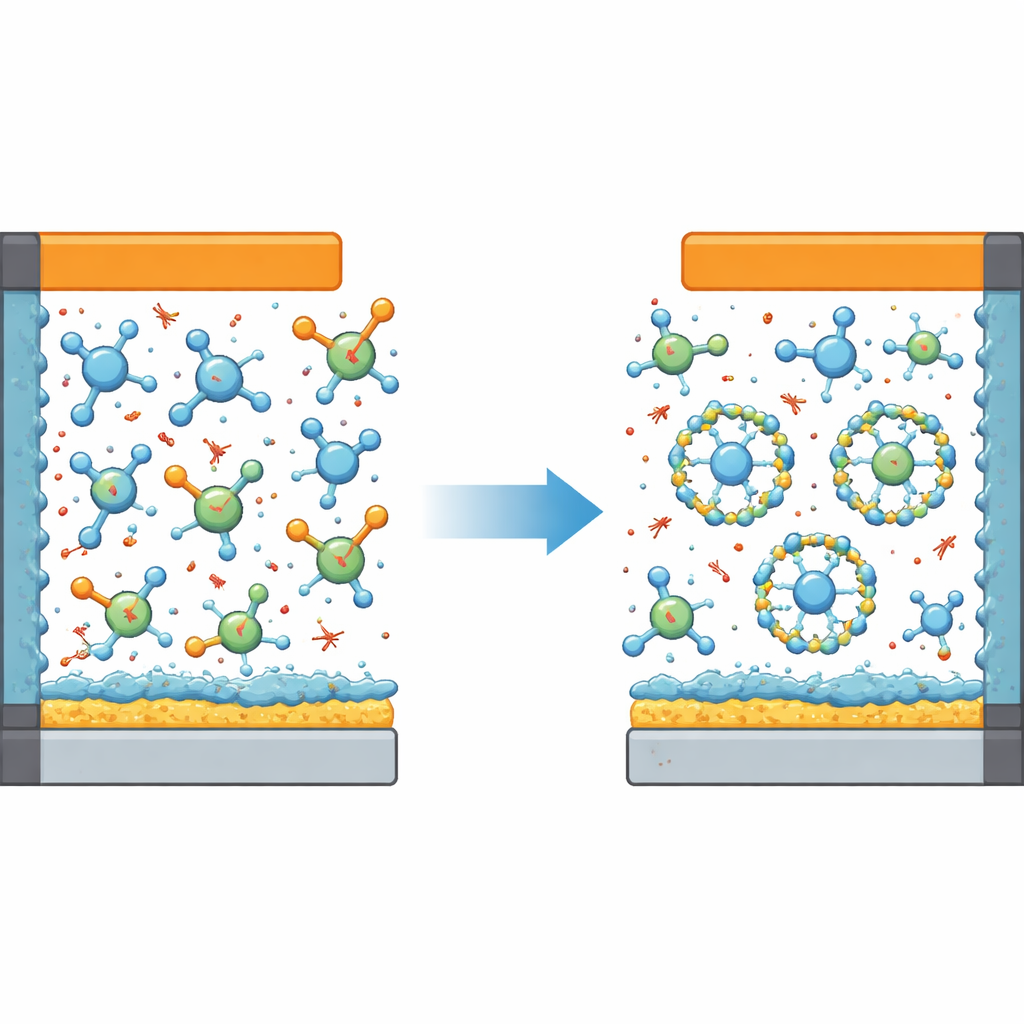
Por qué el litio metálico es tan difícil de domar
El litio metálico es un material de batería ideal porque almacena mucha energía en un paquete pequeño y ligero. Pero también es muy reactivo. Cuando una batería carga y descarga, el litio metálico puede crecer en estructuras en forma de aguja y reaccionar con el líquido que lo rodea, desperdiciando litio y arriesgando cortocircuitos. Los diseños modernos intentan controlar este comportamiento ajustando cuidadosamente el electrolito para que forme capas protectoras finas tanto en el ánodo de litio como en el cátodo de alto voltaje. Un enfoque popular, llamado electrolito de alta concentración localizada, acerca iones cargados negativamente a los iones de litio, favoreciendo que estas películas protectoras sean ricas en compuestos inorgánicos resistentes como fluoruro de litio y óxido de litio.
El problema oculto con un disolvente habitual
Muchos de estos electrolitos avanzados dependen de un disolvente común, dimetoxietano (DME), que solva bien los iones de litio y facilita la carga rápida. Desafortunadamente, el DME se descompone con facilidad a los altos voltajes usados con cátodos de gran densidad energética como el NCM811 rico en níquel. En formulaciones convencionales, algunas moléculas de DME no están fuertemente ligadas al litio; vagan libremente, especialmente cerca del cátodo y del colector de corriente de aluminio. Allí se descomponen o corroen superficies metálicas, consumiendo capacidad y acortando la vida útil de la batería. Reducir simplemente el contenido de DME no basta, porque muy poco DME ralentiza el movimiento iónico y perjudica el rendimiento.
Un tercer ingrediente que aporta orden
Los investigadores abordaron este dilema añadiendo un tercer líquido cuidadosamente diseñado a la mezcla: un éter altamente fluorado y de débil coordinación llamado HFMTFP. Su nuevo electrolito “ternario” combina DME, un diluyente fluorado no solvante y HFMTFP. Simulaciones por ordenador y mediciones espectroscópicas muestran que HFMTFP remodela sutilmente el entorno microscópico alrededor de los iones de litio. El DME permanece anclado en la vecindad inmediata del litio, mientras que HFMTFP compite lo justo para ralentizar el intercambio constante de moléculas de DME dentro y fuera de esa esfera. Esta jerarquía energética suprime la población de moléculas libres de DME que de otro modo vagarían y se descompondrían a alto voltaje.
Capas protectoras autoformadas en ambos electrodos
HFMTFP también desempeña un segundo papel crucial. Debido a su estructura fluorada y su comportamiento distinto cuando está libre frente a cuando está ligada al litio, se descompone de manera preferente en ambos electrodos en formas que resultan útiles. En la superficie del litio metálico, HFMTFP coordinado y el anión de la sal se degradan en compuestos inorgánicos ricos en fluoruro de litio y óxido de litio, formando una capa protectora fina, uniforme y mecánicamente resistente. En el cátodo NCM811 de alto voltaje, el HFMTFP libre se oxida para formar un recubrimiento rico en flúor que protege el material activo del electrolito agresivo. Las medidas confirman que estos recubrimientos son más inorgánicos y ricos en flúor que los formados en electrolitos estándar, y la microscopía muestra que los depósitos de litio permanecen compactos en lugar de crecer en estructuras frágiles y musgosas.
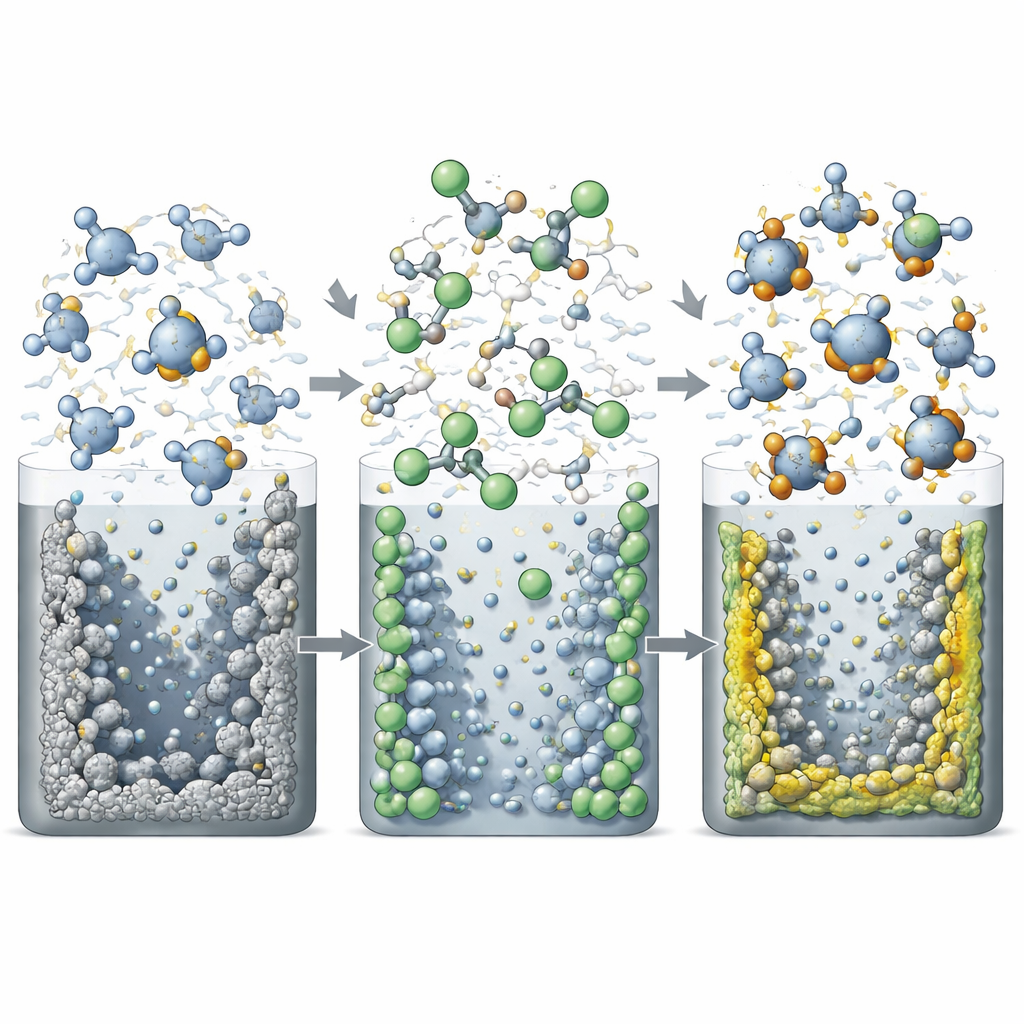
Rendimiento duradero bajo estrés realista
Para comprobar si este ajuste molecular realmente importa en la práctica, el equipo probó celdas completas de litio metálico con cátodos NCM811 en condiciones exigentes: alto voltaje (hasta 4,4 V), alta corriente (el doble de la tasa normal) y una carga de material activo realista. En comparación con electrolitos más simples, la formulación ternaria redujo drásticamente la corrosión del aluminio y las reacciones colaterales a alto voltaje. Las celdas que usaron el nuevo electrolito conservaron más del 90 % de su capacidad original tras 250 ciclos rápidos de carga y descarga, mientras que las versiones convencionales se degradaron mucho antes por debajo de ese nivel. Sondas estructurales del cátodo revelaron que su marco cristalino en capas permaneció notablemente intacto, lo que indica que el recubrimiento protector bloqueó con éxito los cambios dañinos en el interior del material.
Qué significa esto para dispositivos futuros
En esencia, el estudio muestra que añadir un cosolvente fluorado de interacción moderada al electrolito puede controlar un disolvente reactivo pero útil como el DME, evitando que se comporte mal y convirtiendo a su compañero en un constructor de películas protectoras. Al diseñar cómo se disponen las moléculas alrededor de los iones de litio, los investigadores crearon un electrolito que resiste la degradación a alto voltaje y forma de forma natural pieles fuertes e inorgánicas en los electrodos de la batería. Esta estrategia acerca un paso más a las baterías de litio metálico a su uso cotidiano en vehículos eléctricos de larga autonomía y en dispositivos portátiles de gama alta, donde la durabilidad y la seguridad deben estar a la altura de su impresionante densidad energética.
Cita: Kim, J., Lee, K., Kim, I. et al. Dual solvents with different coordination strengths for localized high concentration electrolytes in lithium metal batteries. npj Energy Mater. 1, 2 (2026). https://doi.org/10.1038/s44456-025-00002-0
Palabras clave: baterías de litio metálico, diseño de electrolitos, cátodos de alto voltaje, disolventes fluorados, vida útil de la batería