Clear Sky Science · fr
Une atlas transcriptomique spatiotemporelle du développement précoce des gonades femelles du porc (Sus scrofa)
Pourquoi le développement précoce des ovules compte
Avant la naissance de toute femelle mammifère, ses futurs ovules sont déjà mis en place à l’intérieur de petits organes appelés gonades. Comprendre comment ces tout premiers stades se déroulent est essentiel pour combattre l’infertilité, améliorer l’élevage et développer en toute sécurité des ovules cultivés en laboratoire. Cette étude construit une « carte » détaillée en espace et en temps de la formation et de l’organisation des précurseurs d’ovules dans les ovaires d’embryons de porc — un substitut puissant pour l’humain, car le développement porcin y ressemble fortement.
Construire une carte cellulaire dans l’espace et le temps
Les chercheurs ont utilisé une méthode à haute résolution appelée transcriptomique spatiale, qui lit des milliers de gènes tout en conservant la position de chaque cellule dans le tissu. Ils ont examiné les gonades femelles de porc à cinq jours embryonnaires clés, depuis l’arrivée des cellules germinales jusqu’au début de la division particulière qui crée les ovules. En analysant plus de 50 000 petits pixels de tissu, ils ont classé huit types cellulaires majeurs, notamment les cellules germinales, plusieurs types de cellules de soutien, des cellules interstitielles, des cellules vasculaires et des cellules mésenchymateuses formant des frontières. Cela leur a permis de dresser un atlas fin montrant la position de chaque type cellulaire et comment ces positions évoluent au fur et à mesure de la formation de l’ovaire.
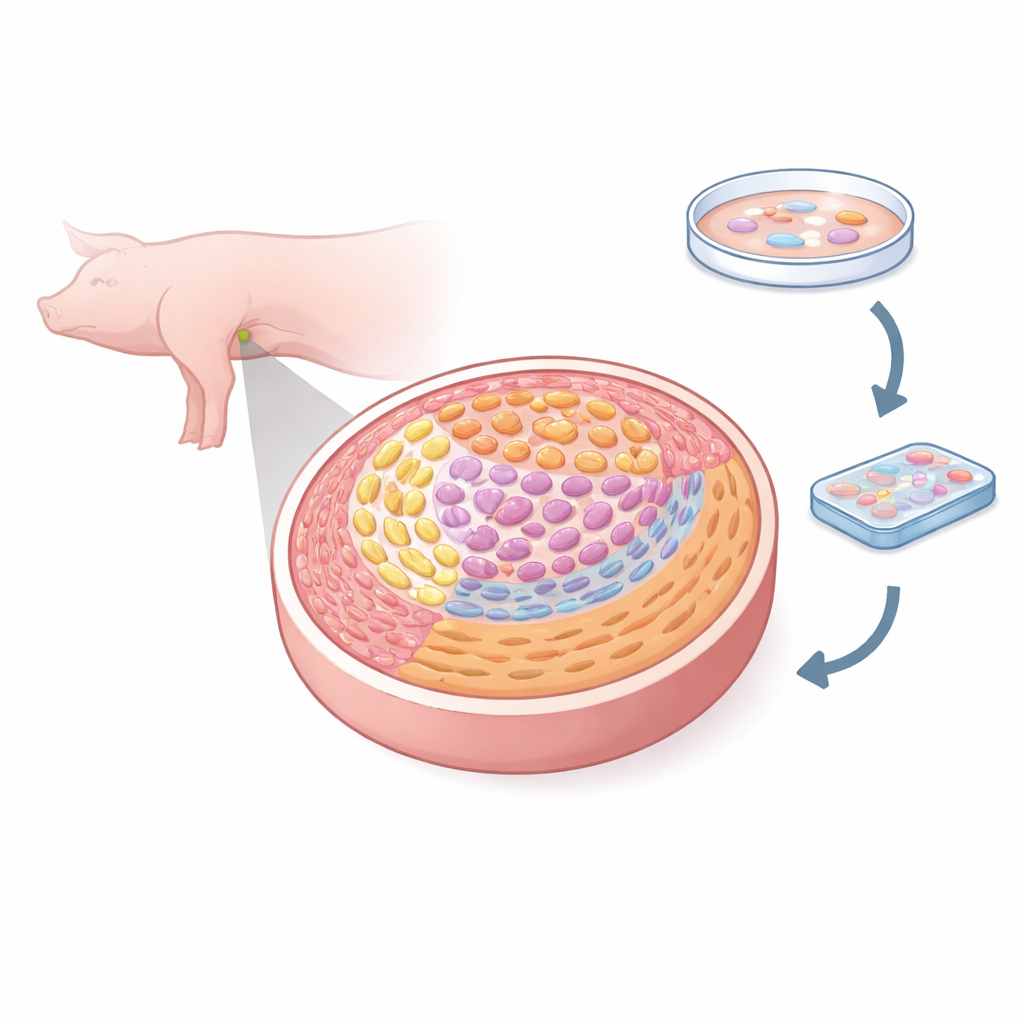
Suivre la naissance des futurs ovules
Au sein de la population de cellules germinales, l’équipe a identifié trois stades principaux : des cellules germinales primordiales en division, des cellules ressemblant à des ovocytes réagissant à un signal lié à la vitamine A appelé acide rétinoïque, et des cellules ayant engagé la méiose, la division spéciale qui réduit le nombre de chromosomes de moitié. En suivant l’activité génique au long d’un « pseudotemps » développemental, ils montrent que les jours E24–E50 chez le porc couvrent le trajet complet depuis l’arrivée des cellules germinales primordiales jusqu’aux précurseurs d’ovules précoces entrant en méiose. En parallèle, ces cellules subissent d’importantes modifications épigénétiques — des marques chimiques sur l’ADN et les histones sont effacées ou remodélisées, réinitialisant les cellules germinales pour leur rôle futur, tandis qu’une marque répressive clé, H3K27me3, disparaît progressivement à mesure que les cellules se déterminent en ovocytes.
Les cellules de soutien forment des voisinages en couches
L’ovaire n’est pas qu’un sac de cellules germinales ; c’est une communauté stratifiée où les cellules de soutien créent les voisinages qui guident le développement des ovules. L’étude montre que trois groupes apparentés de cellules de soutien — les cellules de l’épithélium de surface et deux vagues de pré‑granulosa — sont disposés en couches distinctes de la corticale externe vers l’intérieur. Au fil du temps, une vague s’installe principalement dans la médulla (région centrale), tandis que la deuxième vague reste plus proche des cellules germinales dans la corticale et la corticale interne. Ces schémas correspondent à ce qui est observé dans les ovaires fœtaux humains, suggérant un plan profondément conservé. D’autres cellules somatiques se répartissent également en zones distinctes : les cellules interstitielles remplissent une grande partie de la médulla et s’étendent fortement aux stades ultérieurs, tandis que les cellules endothéliales s’organisent en structures semblables à des vaisseaux près des cellules germinales, fournissant probablement nutriments et signaux.
Les signaux qui indiquent aux cellules germinales de devenir ovules
Pour comprendre comment les cellules environnantes communiquent avec les cellules germinales, les auteurs ont modélisé les signalisations intercellulaires en s’appuyant sur des paires ligand‑récepteur connues. Ils ont trouvé qu’une voie de développement bien connue, pilotée par des molécules BMP (notamment BMP2, BMP4 et GDF5), est centrale pour pousser les cellules germinales primordiales vers l’identité d’ovocyte et l’entrée en méiose. Ces signaux BMP sont principalement produits par la deuxième vague de pré‑granulosa et par un sous‑ensemble de cellules interstitielles, qui entourent les cellules germinales dans la corticale. À mesure que les cellules germinales progressent des stades réactifs à l’acide rétinoïque vers la méiose, la signalisation BMP s’intensifie et active des gènes en aval marquant l’activation de la voie. Comparés aux souris et aux humains, les porcs semblent maintenir l’activité BMP pendant une fenêtre plus longue, ce qui suggère des stratégies spécifiques à l’espèce pour constituer le réservoir d’ovules.
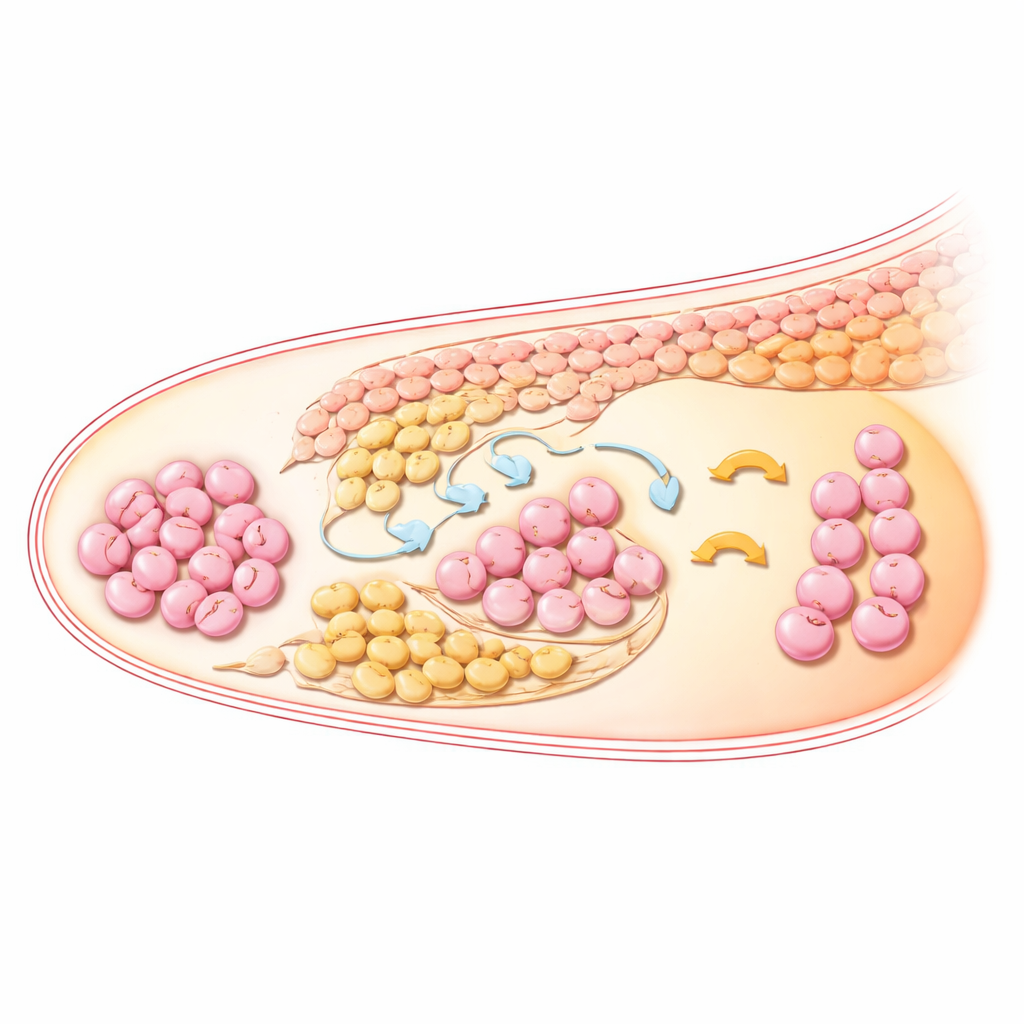
Comment ce travail oriente la production d’ovules en laboratoire
Les auteurs concluent que les ovaires porcins précoces contiennent une niche soigneusement stratifiée où deux vagues de pré‑granulosa, des cellules interstitielles en expansion et des vaisseaux sanguins voisins coopèrent pour façonner le devenir des cellules germinales. Leur atlas identifie la signalisation BMP, ainsi que les voies WNT, NOTCH et liées à la matrice, comme des ingrédients clés de la recette qui transforme les cellules germinales primordiales en précurseurs d’ovules prêts pour la méiose. Pour un public non spécialiste, la conclusion est que nous disposons désormais d’une image beaucoup plus claire et spatialement précise de la façon dont les premiers ovules se forment dans une espèce qui rapproche fortement de l’humain. Ce plan servira à aider les scientifiques à concevoir des systèmes in vitro plus fidèles pour cultiver des ovocytes humains, à améliorer les traitements de la reproduction et à affiner les stratégies d’élevage pour les grands animaux.
Citation: He, P., Xia, W., Chen, T. et al. A spatiotemporal transcriptomic atlas of porcine (Sus scrofa) female early gonadal development. Commun Biol 9, 487 (2026). https://doi.org/10.1038/s42003-026-09932-0
Mots-clés: développement de l’ovaire, cellules germinales, transcriptomique spatiale, signalisation BMP, modèle porcin