Clear Sky Science · de
Ein spatiotemporales Transkriptom‑Atlas der frühen weiblichen Gonadenentwicklung beim Schwein (Sus scrofa)
Warum frühe Eizellentwicklung wichtig ist
Schon bevor ein weibliches Säugetier geboren wird, werden seine künftigen Eizellen in winzigen Organen, den Gonaden, angelegt. Zu verstehen, wie diese frühesten Stadien ablaufen, ist entscheidend, um Unfruchtbarkeit zu behandeln, die Tierzucht zu verbessern und sichere Methoden für im Labor gezüchtete Eizellen zu entwickeln. Diese Studie erstellt eine detaillierte „Karte in Raum und Zeit“ darüber, wie frühe Eizellvorläufer in den Ovarien von Schweineembryonen entstehen und sich organisieren — ein wichtiges Modell für den Menschen, da die Entwicklung beim Schwein unserer ähnlich ist.
Aufbau einer zellulären Karte in Raum und Zeit
Die Forschenden nutzten eine hochaufgelöste Methode namens räumliche Transkriptomik, die Tausende Gene erfasst und gleichzeitig die Position jeder Zelle im Gewebe bewahrt. Sie untersuchten weibliche Schweinegonaden an fünf entscheidenden Embryonaltagen, von der Ankunft der Keimzellen bis zum Beginn der speziellen Zellteilung, die Eizellen hervorbringt. Durch die Analyse von über 50.000 kleinen Gewebe‑Pixeln klassifizierten sie acht Hauptzelltypen, darunter Keimzellen, mehrere Arten von Stütz‑/Begleitzellen, Interstitiumzellen, Gefäßendothelzellen und mesenchymale Zellen an Grenzflächen. Damit konnten sie ein fein abgestuftes Atlasbild malen, das zeigt, wie jeder Zelltyp positioniert ist und wie sich diese Positionen während der Ovarbildung verändern.
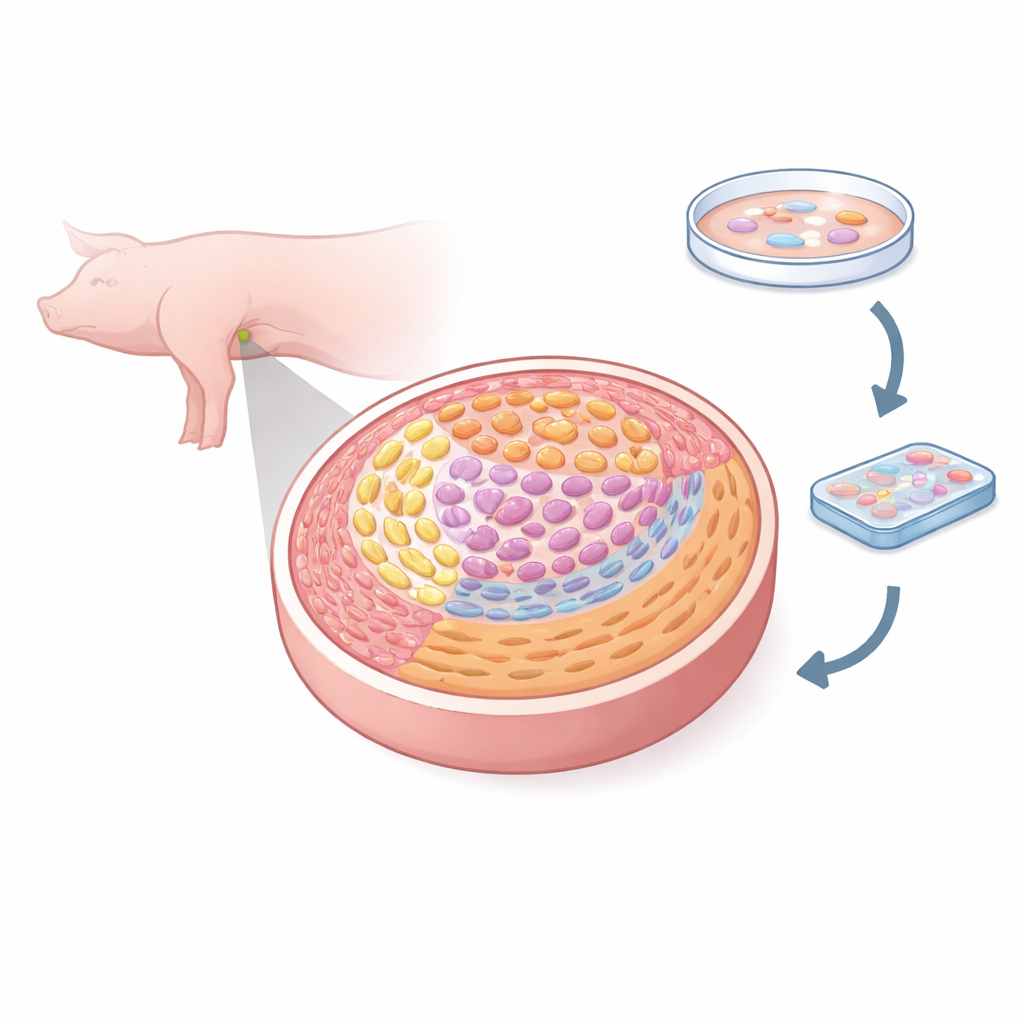
Die Entstehung künftiger Eizellen verfolgen
Innerhalb der Keimzellpopulation identifizierte das Team drei Hauptstadien: teilende primordiale Keimzellen, eizellähnliche Zellen, die auf ein vitamin‑A‑verwandtes Signal namens Retinsäure reagieren, und Zellen, die in die Meiose eingetreten sind, die spezielle Teilung, die die Chromosomenzahl halbiert. Durch das Verfolgen der Genaktivität entlang eines Entwicklungs‑„Pseudotimes“ zeigten sie, dass die Tage E24–E50 im Schweineembryo die gesamte Reise von frisch eingetroffenen primordiale Keimzellen zu frühen Eizellvorläufern, die in die Meiose eintreten, abdecken. Gleichzeitig durchlaufen diese Zellen weitreichende epigenetische Veränderungen — chemische Markierungen an DNA und Histonen werden entfernt oder umgestaltet, wodurch die Keimzellen für ihre künftige Rolle neu programmiert werden, während eine wichtige repressive Markierung, H3K27me3, allmählich verschwindet, wenn die Zellen sich zur Eizelle verpflichten.
Stütz‑/Begleitzellen bilden geschichtete Nachbarschaften
Das Ovar ist nicht nur ein Verband von Keimzellen; es ist eine geschichtete Gemeinschaft, in der Stütz‑/Begleitzellen die Nachbarschaften schaffen, die die Eizellentwicklung steuern. Die Studie zeigt, dass drei verwandte Gruppen von Begleitzellen — Oberflächenepithelzellen und zwei Wellen von Prä‑Granulosazellen — klar geschichtet von der äußeren Rinde (Kortex) nach innen angeordnet sind. Im Laufe der Zeit besiedelt eine Welle überwiegend das Mark (Medulla), während die zweite Welle näher an den Keimzellen in der Rinde und Innenrinde verbleibt. Diese Muster entsprechen den Beobachtungen in menschlichen fetalen Ovarien und deuten auf einen stark konservierten Bauplan hin. Andere somatische Zellen ordnen sich ebenfalls in getrennte Zonen: Interstitiumzellen füllen einen Großteil der Medulla und nehmen in späteren Stadien stark zu, während Endothelzellen sich in gefäßähnlichen Strukturen in der Nähe der Keimzellen organisieren, vermutlich um Nährstoffe und Signale zu liefern.
Signale, die Keimzellen zur Eizellenbildung anweisen
Um zu verstehen, wie die umliegenden Zellen mit Keimzellen kommunizieren, modellierten die Autorinnen und Autoren die Zell‑zu‑Zell‑Signalgebung anhand bekannter Ligand‑Rezeptor‑Paare. Sie fanden heraus, dass ein gut bekannter Entwicklungsweg, der von BMP‑Molekülen (insbesondere BMP2, BMP4 und GDF5) gesteuert wird, zentral dafür ist, primordiale Keimzellen in Richtung Eizell‑Identität und Meiose zu treiben. Diese BMP‑Signale werden hauptsächlich von der zweiten Welle der Prä‑Granulosazellen und einer Untergruppe von Interstitiumzellen produziert, die sich in der Rinde um Keimzellen legen. Während die Keimzellen vom retinsäure‑sensitiven zum meiotischen Stadium fortschreiten, nimmt die BMP‑Signalgebung zu und schaltet nachgeschaltete Gene an, die die Aktivierung des Weges markieren. Im Vergleich zu Maus und Mensch scheinen Schweine BMP‑Aktivität über ein längeres Zeitfenster aufrechtzuerhalten, was auf artspezifische Strategien zur Bildung des Eizellbestands hinweist.
Wie diese Arbeit auf im Labor gezüchtete Eizellen hindeutet
Die Autorinnen und Autoren schließen daraus, dass frühe Schweineovare eine sorgfältig geschichtete Nische enthalten, in der zwei Wellen von Prä‑Granulosazellen, expandierende Interstitiumzellen und nahegelegene Blutgefäße kooperativ das Schicksal der Keimzellen formen. Ihr Atlas hebt die BMP‑Signalgebung zusammen mit WNT-, NOTCH‑ und matrix‑bezogenen Signalwegen als Schlüsselzutaten des Rezeptes hervor, das primordiale Keimzellen in eizellbereite Vorläufer für die Meiose verwandelt. Für Nicht‑Fachleute lautet die Kernaussage: Wir haben nun ein viel klareres, räumlich präzises Bild davon, wie frühe Eizellen in einer dem Menschen sehr ähnlichen Art entstehen. Dieser Bauplan wird Forschenden helfen, treuere Labor‑Systeme zur Kultivierung menschlicher Eizellen zu entwerfen, reproduktionsmedizinische Behandlungen zu verbessern und Zuchtstrategien bei Nutztieren zu verfeinern.
Zitation: He, P., Xia, W., Chen, T. et al. A spatiotemporal transcriptomic atlas of porcine (Sus scrofa) female early gonadal development. Commun Biol 9, 487 (2026). https://doi.org/10.1038/s42003-026-09932-0
Schlüsselwörter: Ovarentwicklung, Keimzellen, räumliche Transkriptomik, BMP‑Signalgebung, Schweinmodell