Clear Sky Science · fr
Synthèse, activités antioxydantes et antimicrobiennes, étude de docking moléculaire de nouveaux dérivés de la pyrimidine
Nouvelles armes contre les germes coriaces
La résistance aux antibiotiques et les infections fongiques difficiles à traiter rendent de nouveau des maladies autrefois banales plus dangereuses. Cette étude décrit une famille de petites molécules nouvellement synthétisées, conçues à la fois pour neutraliser des microbes nuisibles et pour éliminer des espèces oxydantes « rouillées » dans notre organisme. En combinant la chimie organique classique avec des simulations informatiques modernes, les chercheurs identifient un composé phare qui cible une enzyme bactérienne clé tout en montrant une forte activité antioxydante, ouvrant la voie à de futurs médicaments capables de combattre l’infection sur plusieurs fronts à la fois.
Construction d’un échafaudage chimique polyvalent
L’équipe s’est concentrée sur les pyrimidines, une classe de molécules en anneau déjà présente dans de nombreux médicaments et dans notre propre ADN. À partir d’un bloc de base simple appelé chalcone, ils ont enchaîné une série de réactions pour construire des anneaux plus complexes, fusionnés et contenant du soufre et de l’azote. Cette stratégie a généré une petite bibliothèque de composés apparentés, étiquetés 3 à 11, chacun portant des groupes latéraux légèrement différents. Ces changements subtils de forme et de composition chimique visaient à ajuster la force d’interaction des molécules avec des cibles biologiques telles que des enzymes bactériennes ou des espèces oxygénées instables impliquées dans les dommages cellulaires.
Tester le pouvoir antioxydant
Pour déterminer si ces composés pouvaient neutraliser des radicaux libres nocifs, les scientifiques ont utilisé un test courant de laboratoire basé sur un colorant violet connu sous le nom de DPPH. Lorsqu’un antioxydant cède un électron ou un atome d’hydrogène à ce colorant, la solution s’éclaircit, et le degré d’atténuation révèle la puissance de l’antioxydant. Plusieurs des nouvelles molécules ont montré une activité notable, mais trois — appelées 5, 9a et surtout 11 — se sont distinguées. Aux doses testées, elles ont réduit le signal du colorant presque aussi bien que, ou mieux que, l’antioxydant synthétique largement utilisé BHT. Le composé 11 a nécessité une concentration encore plus faible que le témoin pour diminuer de moitié le niveau de radicaux, ce qui en fait le capteur de radicaux le plus puissant de la série.
Combattre bactéries et champignons
Le même ensemble de molécules a ensuite été mis au défi contre un petit panel de microbes pathogènes : deux bactéries communes, Escherichia coli et Bacillus subtilis, et deux champignons problématiques, Aspergillus niger et Candida albicans. Dans des tests sur boîte de Pétri, des solutions des composés ont diffusé à travers un agar contenant ces organismes. Des halos clairs autour des puits ont montré où la croissance était inhibée. La plupart des composés ont produit des zones d’inhibition modérées, mais encore une fois 5, 9a et 11 furent exceptionnels, traçant de larges et fortes zones d’inhibition contre les quatre espèces. Dans certains cas, les performances du composé 11 se rapprochaient de celles de médicaments standard tels que la streptomycine pour les bactéries et la cycloheximide pour les champignons, suggérant qu’il pourrait constituer un amont prometteur pour un nouvel antimicrobien à large spectre.
Observer une molécule s’agripper à sa cible
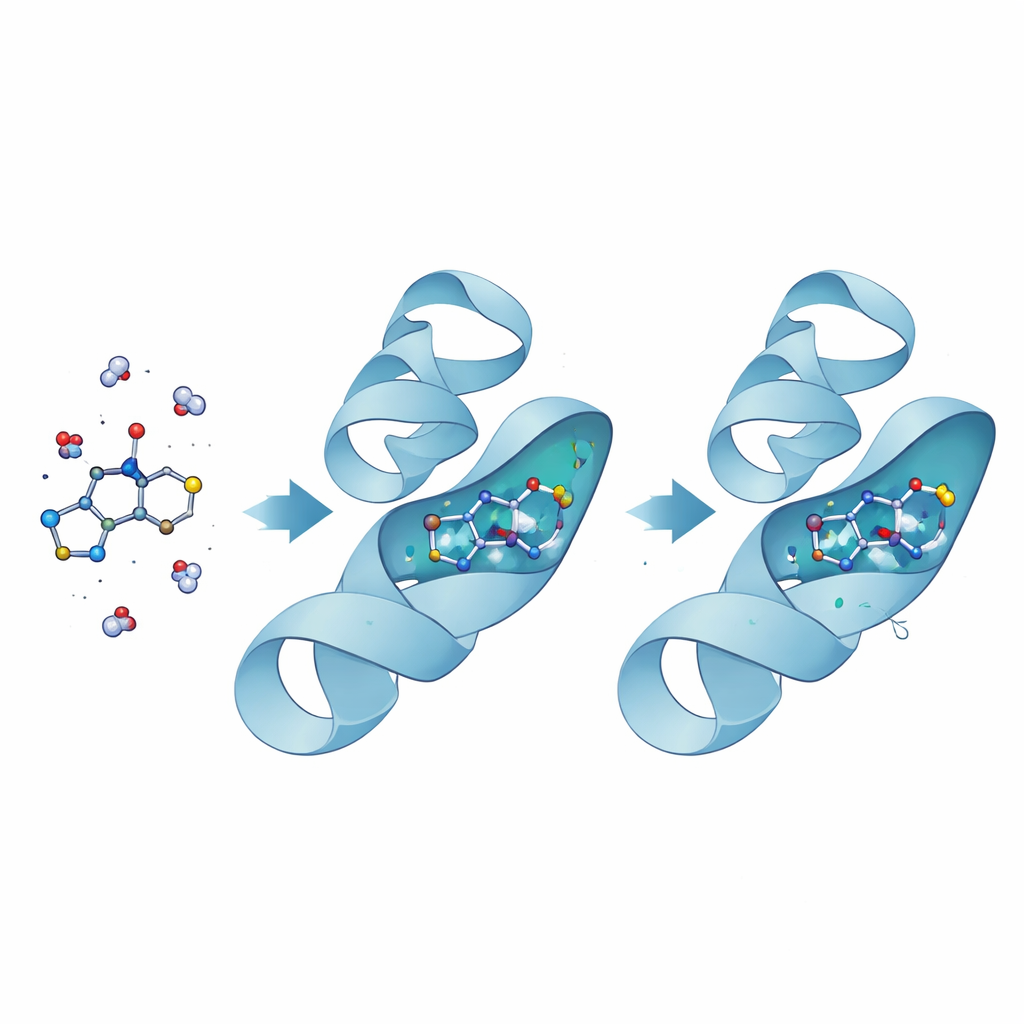
Pour comprendre pourquoi le composé 11 était si efficace contre les bactéries, les chercheurs se sont tournés vers la modélisation informatique de son interaction avec l’ADN girase, une enzyme clé qui aide l’ADN bactérien à se condenser et se décondense. Des calculs de docking ont d’abord positionné la molécule dans la poche consommant de l’énergie de l’enzyme, où elle semblait s’emboîter parfaitement. De longues simulations de dynamique moléculaire détaillées ont ensuite suivi le comportement du complexe sur plusieurs dizaines de nanosecondes de temps virtuel. Une fois le composé 11 lié, la structure de l’enzyme est devenue légèrement plus compacte et moins instable, en particulier autour du site actif, indiquant une prise ferme et stabilisante. Les calculs d’énergie de liaison ont montré que les forces attractives entre le médicament et la protéine dépassaient confortablement le coût énergétique d’évincer les molécules d’eau, confirmant une interaction forte et favorable.
Pourquoi cela importe pour les médicaments futurs
Pris ensemble, la chimie, les essais en laboratoire et les simulations informatiques dressent un tableau cohérent. En façonnant soigneusement des anneaux à base de pyrimidine, l’équipe a créé des molécules qui non seulement neutralisent des radicaux nocifs mais s’attachent aussi fermement à une enzyme bactérienne vitale. Le composé 11, en particulier, combine un comportement antioxydant puissant avec une activité antibactérienne et antifongique comparable à celle des médicaments existants, étayée par une explication claire au niveau atomique de son mode d’action. Bien que ces molécules en soient encore à un stade expérimental précoce, elles illustrent comment la synthèse, le criblage biologique et la modélisation numérique peuvent accélérer la recherche de nouveaux traitements qui s’attaquent à la fois à l’infection et aux dommages oxydatifs.
Citation: Khalaf, H.S., El-Rashedy, A.A., Abd El-Gwaad, A.A. et al. Synthesis, antioxidant and antimicrobial activities, molecular docking study of new pyrimidine derivatives. Sci Rep 16, 12354 (2026). https://doi.org/10.1038/s41598-026-45654-3
Mots-clés: dérivés de pyrimidine, agents antimicrobiens, antioxydants, inhibiteurs de l'ADN girase, conception de médicaments