Clear Sky Science · de
Synthese, antioxidative und antimikrobielle Aktivitäten, Molekulardocking‑Studie neuer Pyrimidin‑Derivate
Neue Waffen gegen hartnäckige Keime
Antibiotikaresistenzen und schwer behandelbare Pilzinfektionen machen einst routinemäßige Krankheiten wieder gefährlicher. Diese Studie beschreibt eine Familie neu entworfener kleiner Moleküle, die sowohl schädliche Mikroben entwaffnen als auch schädliche „rostähnliche“ Chemikalien in unserem Körper neutralisieren sollen. Durch die Kombination klassischer organischer Chemie mit modernen Computersimulationen identifizieren die Forschenden eine besonders vielversprechende Verbindung, die ein wichtiges bakterielles Enzym trifft und zugleich starke antioxidative Eigenschaften zeigt — ein Hinweis auf künftige Arzneimittel, die Infektionen auf mehreren Ebenen zugleich bekämpfen könnten.
Aufbau eines vielseitigen chemischen Gerüsts
Das Team konzentrierte sich auf Pyrimidine, eine Klasse ringförmiger Moleküle, die bereits in vielen Arzneistoffen und sogar in unserer eigenen DNA vorkommen. Ausgehend von einem einfachen Baustein namens Chalcon führten sie eine Reihe von Reaktionen durch, um komplexere, kondensierte Ringe mit Schwefel und Stickstoff zu erzeugen. Diese Strategie lieferte eine kleine Bibliothek verwandter Verbindungen, bezeichnet mit 3 bis 11, die jeweils leicht unterschiedliche Seitenketten tragen. Diese subtilen Änderungen in Form und chemischer Zusammensetzung sollten steuern, wie stark die Moleküle mit biologischen Zielstrukturen wie bakteriellen Enzymen oder reaktiven Sauerstoffspezies interagieren können, die mit Zellschädigung in Verbindung stehen.
Überprüfung der antioxidativen Wirkung
Um zu prüfen, ob diese Verbindungen schädliche freie Radikale neutralisieren können, verwendeten die Forschenden einen gebräuchlichen Labortest auf Basis eines violetten Farbstoffs namens DPPH. Wenn ein Antioxidans diesem Farbstoff ein Elektron oder ein Wasserstoffatom spendet, verblasst die Lösung, und der Grad des Verblassens zeigt die Potenz des Antioxidans an. Mehrere der neuen Moleküle zeigten deutliche Aktivität, doch drei — bezeichnet als 5, 9a und insbesondere 11 — hoben sich hervor. In den getesteten Konzentrationen reduzierten sie das Signal des Farbstoffs beinahe so gut wie oder besser als das weit verbreitete synthetische Antioxidans BHT. Verbindung 11 benötigte eine noch geringere Konzentration als die Vergleichssubstanz, um den Radikalspiegel halbieren, was sie zum stärksten Radikalfänger der Reihe macht.
Kampf gegen Bakterien und Pilze
Dasselbe Set von Molekülen wurde anschließend gegen ein kleines Panel krankheitserregender Mikroorganismen getestet: zwei häufige Bakterien, Escherichia coli und Bacillus subtilis, sowie zwei problematische Pilze, Aspergillus niger und Candida albicans. In Petrischalenversuchen durften Lösungen der Verbindungen durch mit diesen Organismen durchsetzte Agarplatten diffundieren. Klare Hemmhöfe um die Vertiefungen zeigten, wo das Wachstum blockiert wurde. Die meisten Verbindungen erzeugten mäßige Hemmzonen, doch wiederum waren 5, 9a und 11 außergewöhnlich und bildeten breite, starke Zonen gegen alle vier Spezies. In einigen Fällen entsprach die Leistung von Verbindung 11 nahezu der Standardmedikamente wie Streptomycin für Bakterien und Cycloheximid für Pilze, was darauf hindeutet, dass sie als vielversprechender Leitstoff für ein neues Breitbandantimikrobiummittel dienen könnte.
Beobachtung, wie ein Molekül sein Ziel umklammert
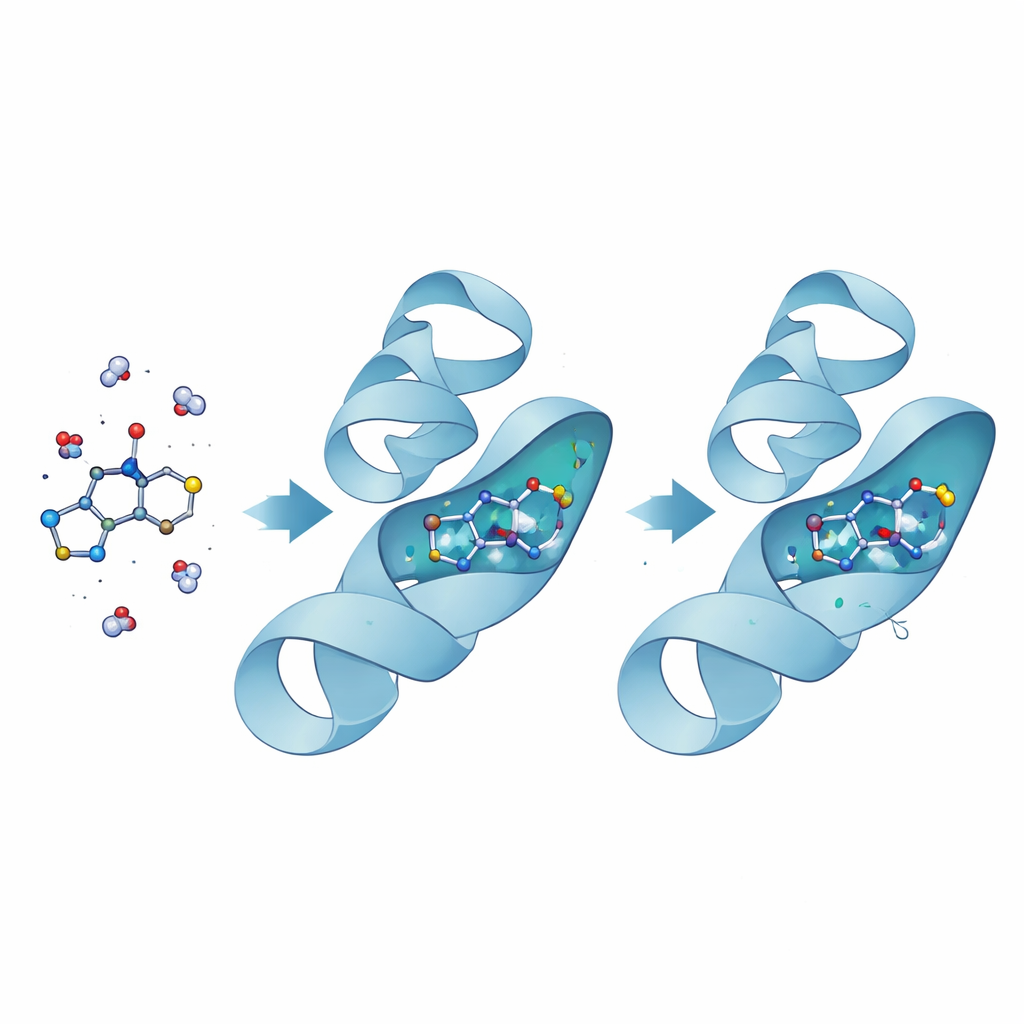
Um zu verstehen, warum Verbindung 11 gegen Bakterien so wirksam war, wandten sich die Forschenden der Computermodellierung ihrer Wechselwirkung mit der DNA‑Gyrase zu, einem Schlüsselenzym, das die DNA von Bakterien auf- und abwickelt. Docking‑Berechnungen positionierten das Molekül zunächst in der energieverbrauchenden Tasche des Enzyms, wo es offenbar gut hineinpasste. Lange, detaillierte Molekulardynamik‑Simulationen verfolgten dann das Verhalten des Komplexes über mehrere zehn Nanosekunden virtueller Zeit. Mit gebundener Verbindung 11 wurde die Struktur des Enzyms leicht kompakter und weniger wackelig, insbesondere in der Umgebung des aktiven Zentrums, was auf einen festen und stabilisierenden Griff hindeutet. Berechnungen der Bindungsenergie zeigten, dass die attraktiven Kräfte zwischen Wirkstoff und Protein die energetischen Kosten für das Verdrängen von Wassermolekülen deutlich überwiegen, was eine starke, günstige Wechselwirkung bestätigt.
Warum das für zukünftige Arzneimittel wichtig ist
Zusammengefasst zeichnen Chemie, Labortests und Computersimulationen ein stimmiges Bild. Durch die sorgfältige Gestaltung pyrimidinbasierter Ringe schuf das Team Moleküle, die nicht nur schädliche Radikale binden, sondern auch fest an ein lebenswichtiges bakterielles Enzym andocken. Insbesondere Verbindung 11 vereint starke antioxidative Eigenschaften mit antibakterieller und antimykotischer Potenz auf dem Niveau bestehender Medikamente und liefert eine klare atomare Erklärung für ihren Wirkmechanismus. Obwohl sich diese Moleküle noch in einem frühen, experimentellen Stadium befinden, demonstrieren sie, wie die Kombination von Synthese, biologischer Prüfung und digitaler Modellierung die Suche nach neuen Behandlungen beschleunigen kann, die zugleich Infektionen und oxidative Schäden bekämpfen.
Zitation: Khalaf, H.S., El-Rashedy, A.A., Abd El-Gwaad, A.A. et al. Synthesis, antioxidant and antimicrobial activities, molecular docking study of new pyrimidine derivatives. Sci Rep 16, 12354 (2026). https://doi.org/10.1038/s41598-026-45654-3
Schlüsselwörter: Pyrimidin‑Derivate, antimikrobielle Mittel, Antioxidantien, DNA‑Gyrase‑Inhibitoren, Wirkstoffdesign