Clear Sky Science · fr
Dynamiques de la chromatine au locus Klf4 dans des cellules pluripotentes de souris
Comment l’ADN se déplace à l’intérieur des cellules vivantes
Au cœur de chacune de nos cellules, de longs brins d’ADN se replient et se torsadent pour former une structure compacte appelée chromatine. La façon dont cette chromatine oscille et dérive dans le noyau a de l’importance, car des segments d’ADN éloignés doivent souvent se rencontrer pour activer ou réprimer des gènes. Cette étude examine si l’activation d’un gène modifie réellement le mouvement de la portion d’ADN correspondante, en prenant pour cas test le gène clé des cellules souches Klf4 dans des cellules de souris vivantes.
Observer le voisinage d’un seul gène
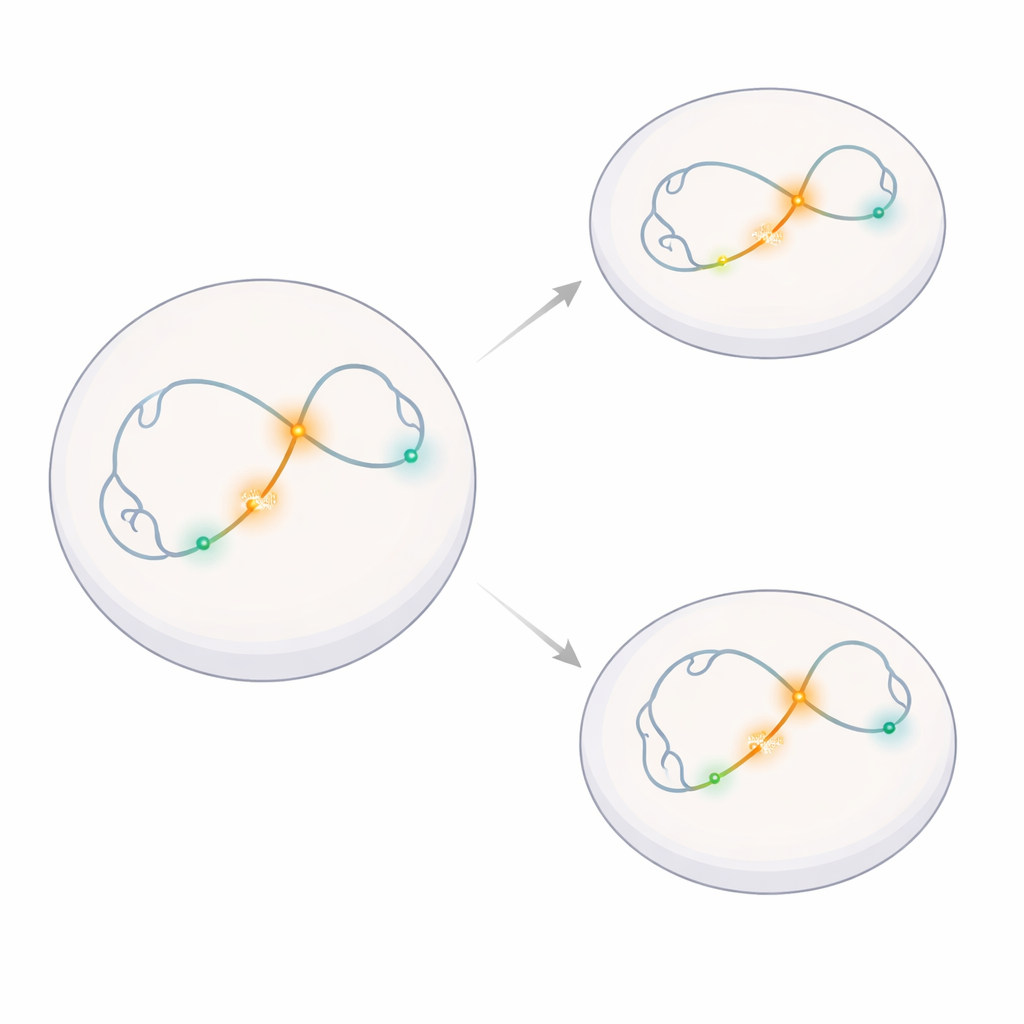
Les chercheurs se sont concentrés sur une petite région du génome contenant Klf4, un gène important pour maintenir les cellules souches dans un état précoce et flexible, et son voisin proche Rad23b, un gène « d’entretien » de routine. Ils ont modifié des cellules souches embryonnaires de souris pour que de minuscules marqueurs fluorescents s’attachent à cinq sites choisis le long de ce voisinage : le principal centre de contrôle de Klf4 (un super-enhancer), le site de départ du gène Klf4, le site de départ du gène Rad23b, et deux régions voisines d’ADN qui ne régulent pas activement des gènes. Cela leur a permis de suivre le mouvement de ces points précis dans des cellules vivantes au fil du temps grâce à une microscopie à haute vitesse.
Éteindre un gène sans changer sa danse
Pour tester si l’activité génique influence le mouvement, l’équipe a exploité une transition bien connue chez les cellules souches. Dans les cellules souches embryonnaires « naïves », Klf4 est fortement actif et contribue à maintenir leur capacité à donner de nombreux types cellulaires. Lorsque ces cellules sont poussées vers un état de type épiblastique — un stade plus avancé — le principal enhancer est chimiquement silencieux et l’expression de Klf4 chute fortement. Les scientifiques ont confirmé que cet interrupteur génétique s’opérait comme prévu, tandis que Rad23b restait actif dans les deux états cellulaires, et que l’insertion de leur système de marquage fluorescent n’altérait pas de manière mesurable l’activité génique normale.
Mesurer la dérive subtile de l’ADN
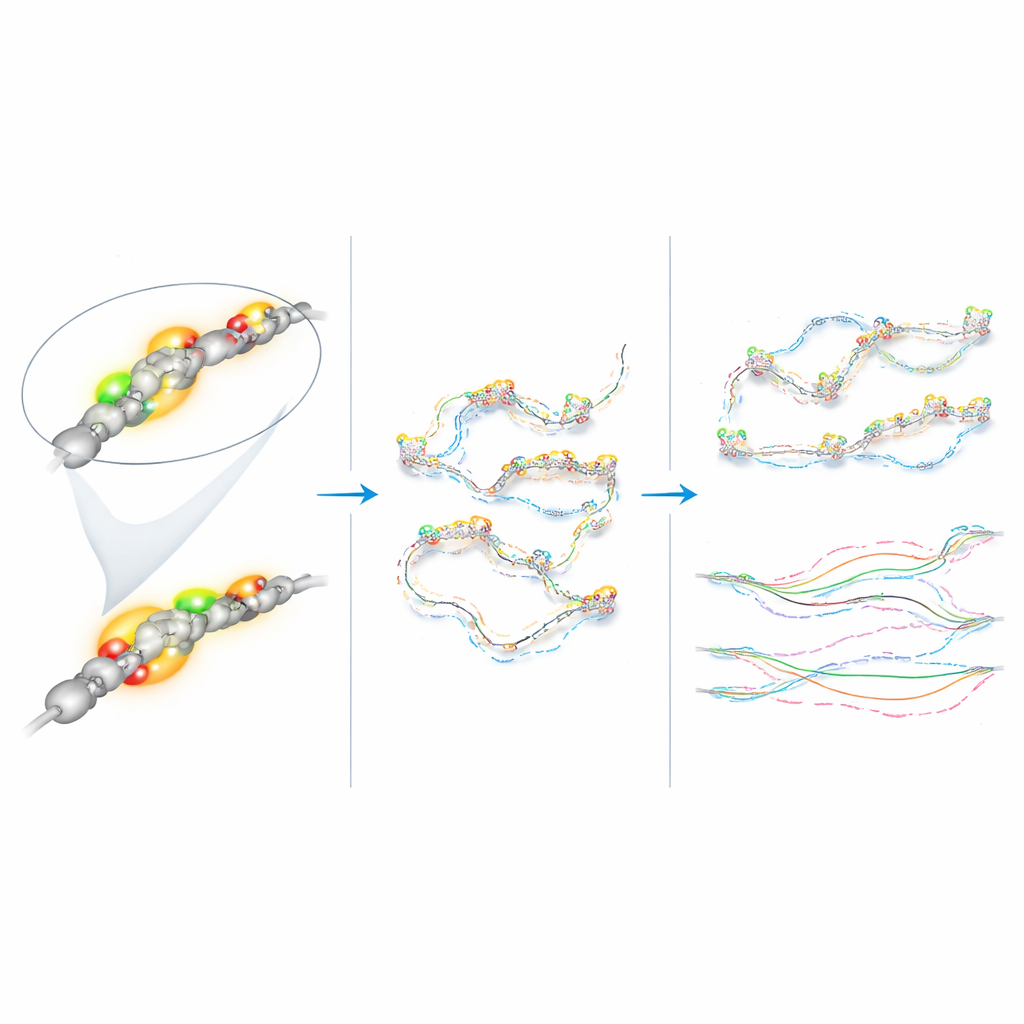
À l’aide d’un logiciel de suivi automatisé et d’analyses personnalisées, les chercheurs ont converti les positions changeantes de chaque point fluorescent en mesures quantitatives du mouvement. Les cinq régions marquées se déplaçaient toutes de manière « subdiffusive » : au lieu d’errer librement comme de la fumée dans l’air, leurs trajectoires étaient contraintes, comme si elles se déplaçaient dans un environnement élastique et encombré. De manière cruciale, le super-enhancer et le promoteur de Klf4 ne se comportaient pas différemment des deux régions témoins voisines, et leur mobilité était essentiellement la même que Klf4 soit actif dans les cellules naïves ou majoritairement éteint dans les cellules de type épiblastique. Cela remet en cause l’idée selon laquelle la transcription — l’acte de lire un gène en ARN — modifie automatiquement la confinement ou la mobilité de ce segment d’ADN.
Un voisin qui bouge vite
Une exception a émergé. Le promoteur du gène d’entretien voisin Rad23b montrait systématiquement un mouvement plus rapide que tous les points d’observation de Klf4 dans les deux états cellulaires. Même au sein d’un segment relativement petit du génome, des segments d’ADN séparés de seulement quelques centaines de milliers de bases pouvaient se mouvoir très différemment. Les auteurs ont également détecté des changements subtils de mouvement pour l’une des régions témoins au fur et à mesure de la maturation des cellules, ce qui suggère que des modifications plus larges du paysage chromatinien global — et pas seulement l’état marche/arrêt d’un gène seul — peuvent altérer la manière dont l’ADN dérive dans le noyau.
Ce que cela signifie pour le contrôle des gènes
En réunissant ces observations, l’étude suggère que le simple fait d’activer ou d’éteindre un gène ne reconfigure pas nécessairement de manière marquée les déplacements locaux de son ADN. Pour le domaine Klf4, la transcription active n’a pas rendu ses éléments de contrôle clés nettement plus confinés ou plus mobiles que des portions voisines de chromatine. En revanche, le mouvement de la chromatine semble dépendre d’un mélange de contexte local, d’une organisation chromosomique plus large et des propriétés particulières de gènes individuels comme Rad23b. Pour le lecteur, la conclusion est que la régulation des gènes ne se réduit pas à actionner des commutateurs ; elle dépend aussi de la façon dont les fragments d’ADN vagabondent et se rencontrent — et ces errances peuvent rester étonnamment stables, même lorsque l’activité des gènes change.
Citation: van Staalduinen, J., Kabbech, H., Yavuz, S. et al. Chromatin dynamics of the Klf4 locus in mouse pluripotent cells. Sci Rep 16, 10941 (2026). https://doi.org/10.1038/s41598-026-45230-9
Mots-clés: dynamiques de la chromatine, régulation des gènes, cellules souches, Klf4, imagerie de cellules vivantes